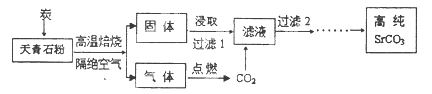
1������� Ԫ���ȣ�Sr��λ�����ڱ���5���ڵ�IIA�塣̼���ȣ�SrCO3�����㷺���ڲ�ɫ���ӻ����������߹ܡ�������ʯ����Ҫ�ɷ�ΪSrSO4�������������ʣ�Ϊԭ����ȡ�ߴ�̼���ȵġ����ս�ȡ�������ֹ�������ʾ�����¡�
��1��д����Ԫ����ͬ���3����Ԫ�ص�ԭ�ӽṹʾ��ͼ��?��
��2�������������±����У���0.5mol SrSO4��ֻ��S����ԭ��ת����4mol���ӡ�д���÷�Ӧ�Ļ�ѧ����ʽ��?��
��3����ȡ�ߴ�̼���ȹ����У������Ҵ�����HOCH2CH2NH2����ΪCO2���ռ����Ҵ���ˮ��Һ�������ԣ���NH3����ˮԭ�����ƣ���ԭ����?�������ӷ���ʽ��ʾ����
��4���������й���2֮���г��ӵȶಽ�������������������?��
��5��������ʪ������һ����ȡ̼���ȵķ�����������ʯ��ĩ��̼������Һ��ϣ�70oC�¼���1��2h��һϵ�в������õ�̼���ȡ���Ҫ��ӦΪ��
 SrSO4��s��+CO
SrSO4��s��+CO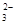 ��aq��? SrCO3��s��+SO
��aq��? SrCO3��s��+SO ��aq��
��aq��
[��֪��70oCʱ��Ksp��SrSO4��=3��3��10��7��Ksq��SrCO3��=1��1��10��10]
������Ӧ��ƽ�ⳣ��K=?��
��6��ͨ��������ʪ�����õ���̼���ȴ��Ƚϵͣ����ܵ�ԭ����?��дһ�֣���
�ο��𰸣���14�֣���1��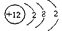 ��2�֣�?
��2�֣�?
��2��SrSO4+4C SrS+4CO����3�֣�?
SrS+4CO����3�֣�?
��3��HOCH2CH2NH2+H2O HOCH2CH2NH3++OH����3�֣�?
HOCH2CH2NH3++OH����3�֣�?
��4��ϴ�ӡ���ɣ�2�֣�?
��5��3��103��2�֣�?
��6������������ʯ��ԭ�еIJ��������ʣ���SrSO4(s)+CO32��(aq) SrCO3(s)+SO42��(aq)�ǿ��淴Ӧ��SrCO3�бض�����SrSO4����2�֣�
SrCO3(s)+SO42��(aq)�ǿ��淴Ӧ��SrCO3�бض�����SrSO4����2�֣�
�����������1����3���ڵ�IIA��Ԫ��Ϊþ���˵����Ϊ+12��������Ӳ�ṹΪ282����2�����������֪����Ԫ�صĻ��ϼ���+6��Ϊ��2�����ݵ��ӡ�ԭ���غ��֪���÷�ӦʽΪSrSO4+4C SrS+4CO������3��NH3+H2O
SrS+4CO������3��NH3+H2O NH3?H2O
NH3?H2O NH4++OH�����������Կ�֪��HOCH2CH2NH2+H2O
NH4++OH�����������Կ�֪��HOCH2CH2NH2+H2O HOCH2CH2NH3++OH������4������֮����Ҫϴ�ӳ�������ȥ�������������Ŀ����Ȼ���ٸ����ȥˮ�֣���5���������⣬K=
HOCH2CH2NH3++OH������4������֮����Ҫϴ�ӳ�������ȥ�������������Ŀ����Ȼ���ٸ����ȥˮ�֣���5���������⣬K=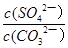 =
=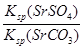 =
= =3��103����6��SrSO4(s)+CO32��(aq)
=3��103����6��SrSO4(s)+CO32��(aq) SrCO3(s)+SO42��(aq)�ǿ��淴Ӧ��SrCO3�бض�����SrSO4�Ȳ��������ʡ�
SrCO3(s)+SO42��(aq)�ǿ��淴Ӧ��SrCO3�бض�����SrSO4�Ȳ��������ʡ�
�����Ѷȣ�һ��
2������� ����ѧ��ѡ��2����ѧ�뼼������15�֣�
 ��ش��ȼҵ���������⣺
��ش��ȼҵ���������⣺
 ��1���������ռ��ǵ��ʳ��ˮʱ���չ̶��ı���k�������ȣ����ɵIJ�Ʒ��������k��_______��Ҫ��������ʽ�ͽ����;
��1���������ռ��ǵ��ʳ��ˮʱ���չ̶��ı���k�������ȣ����ɵIJ�Ʒ��������k��_______��Ҫ��������ʽ�ͽ����;
 ��2��ԭ�ϴ����г�������ɳ��Ca2����Mg2����Fe3����SO42�������ʣ����뾫�ƺ���ܹ����ʹ�á�����ʱ����������ˮ���˺�Ҫ������Լ��ֱ�Ϊ��Na2CO3����HCl�����ᣩ��BaCl2����3���Լ����ӵĺ���˳����______________������ţ�
��2��ԭ�ϴ����г�������ɳ��Ca2����Mg2����Fe3����SO42�������ʣ����뾫�ƺ���ܹ����ʹ�á�����ʱ����������ˮ���˺�Ҫ������Լ��ֱ�Ϊ��Na2CO3����HCl�����ᣩ��BaCl2����3���Լ����ӵĺ���˳����______________������ţ�
 ��3���ȼҵ�Ǹߺ��ܲ�ҵ��һ�ֽ�������ȼ�ϵ������ϵ��¹��տ��Խڣ��磩��30�����ϡ������ֹ�������У�������ϵĴ�����ת����ϵ����ͼ��ʾ�����еĵ缫δ��������õ�����Ĥ��ֻ����������ͨ����?
��3���ȼҵ�Ǹߺ��ܲ�ҵ��һ�ֽ�������ȼ�ϵ������ϵ��¹��տ��Խڣ��磩��30�����ϡ������ֹ�������У�������ϵĴ�����ת����ϵ����ͼ��ʾ�����еĵ缫δ��������õ�����Ĥ��ֻ����������ͨ����?

 ��ͼ��X��__?___���ѧʽ���������Ƚ�ͼʾ������������������a����b���Ĵ�С_________;
��ͼ��X��__?___���ѧʽ���������Ƚ�ͼʾ������������������a����b���Ĵ�С_________;
 �ڷֱ�д��ȼ�ϵ��B�������������Ϸ����ĵ缫��Ӧ������______; ������_____;
�ڷֱ�д��ȼ�ϵ��B�������������Ϸ����ĵ缫��Ӧ������______; ������_____;
 ��������Ƶ���Ҫ�ڣ��磩��֮�����ڣ�д��2����____________��____________��
��������Ƶ���Ҫ�ڣ��磩��֮�����ڣ�д��2����____________��____________��
�ο��𰸣���15�֣���1��k=M(Cl2)/2 M(NaOH)=71/80=1:1.13��0.89��2�֣�
��2���ۢ٢ڣ�2�֣�?��3����Cl2��1�֣�?a��С��b��?��2�֣�
��O2+4e-+2H2O��4OH-?��2�֣�?H2��2e-+2OH-��2H2O ��2�֣�
��ȼ�ϵ�ؿ��Բ���������ĵĵ��ܣ�2�֣�������߲�����Һ��Ũ�ȣ�2�֣������ܺģ�����������Ҳ���֣�
�����������1�����Ե缫��ⱥ��ʳ��ˮ�ķ���ʽΪ2NaCl��2H2O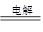 2NaOH��H2����Cl2, �������ݷ���ʽ��֪�������������Ƶ����ʵ���֮����1�U2����������֮���ǣ�k=M(Cl2)/2 M(NaOH)=71/80=0.89��
2NaOH��H2����Cl2, �������ݷ���ʽ��֪�������������Ƶ����ʵ���֮����1�U2����������֮���ǣ�k=M(Cl2)/2 M(NaOH)=71/80=0.89��
��2�����ڳ�ȥSO42��ʱҪ����������Ȼ�����Һ�����������Ȼ�����Ҫ̼���Ƴ�ȥ��������ȷ�IJ���˳���Ǣۢ٢ڡ�
��3����������ȼ�ϵ����ʧȥ���ӵ�������������Y����������X��������������ȼ�ϵ���е�����Ĥֻ����������ͨ������ȼ�ϵ�������������õ����Ӳ���OH�������Է�Ӧ���������Ƶ�Ũ�����ߣ���a��С��b����
�ڸ���������ʧȥ���ӣ����������õ����ӣ����Ե缫��Ӧʽ�ֱ�ΪH2��2e-+2OH-��2H2O ��O2+4e-+2H2O��4OH- ��
�۸���װ���ص㼰��Ӧ���̿�֪��������Ƶ��ŵ���ȼ�ϵ�ؿ��Բ���������ĵĵ��ܣ���߲�����Һ��Ũ�ȣ������ܺĵȡ�
�����Ѷȣ�һ��
3��ѡ���� ���н�����ұ�������õ�ⷨ��ұ������
A����
B��ͭ
C����
D��Ǧ
�ο��𰸣�C
�����������ⷨһ������ұ���Ƚϻ��õĽ����������ƺ����ȣ��ʱ���Ĵ�ѡ��C����Fe��Zn��Cu��Pb���еȻ��ý������Ȼ�ԭ��������C��CO��H2����ԭ����ԭұ����
���������⿼���˽�����ұ�������ڶԻ�ѧ����֪ʶ�Ŀ��飬���Ҫ���գ�����Hg��Ag�Ȳ����ý����������ﲻ�ȶ��������ֽ⣬һ������ȷֽⷨұ����V��Cr��Mn��W�ȸ��۵����һ�������ȷ�Ӧ�����ĸ�����ұ���������Ѷ����С�
�����Ѷȣ�һ��
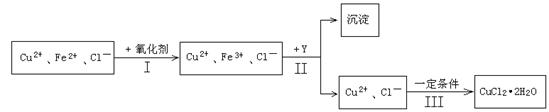
4������� ��15�֣�ij���ú�����������FeCl2��CuCl2��Һ�Ʊ�������CuCl2��2H2O����, Ϊ���ͳɱ��Ҳ���ɿ�����Ⱦ���ⶨʵ�鲽�����£�
һЩ�����������������PH
��������
| PH
|
��ʼ����
| ������ȫ
|
Fe2+
| 7.6
| 9.6
|
Fe3+
| 2.7
| 3.7
|
Cu2+
| 4.4
| 4.6
|
��ѧ�Լ��۸��
�ش��������⣺
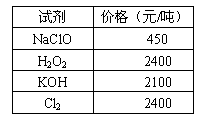
��1��������У���Fe2+ת��ΪFe3+���ѡ�������������е�________������ĸ����
A��H2O2? B��NaClO? C��KOH? D��Cl2
�÷�Ӧ�����ӷ���ʽΪ____________________________________________��
��2���ڲ�����У��ټ���Y��Ŀ����Ϊ�˵�����Һ������Դ�ʹFe3+������ȫ��Y����ѡ�����������е�________________������ĸ����
A��NaOH? B��CuO? C��Cu��OH��2? D��Cu2��OH��2CO3
�ڽ����뺣�ڴ����γ�ɳ��ԭ���ǽ�ˮ�еĽ�������ˮ�еĵ���ʷ����۳�����������г��������ʵ������Ƴɽ��������μ���ϡ������ܿ�����������_________��
��3�������Ӧ���Ƶ�ʵ�������� ________________________??��
�ο��𰸣���15�֣�ÿ��3�֣���1��A? 2Fe2+ + H2O2 + 2H+ = 2Fe3+ + 2H2O
��2���� BCD?�����к��ɫ�������֣������μ�������Һ�����ܽ�û�ɫ��Һ
��3������Һ�ڽϵ��¶��¼��������������壬ͬʱͨ���Ȼ��������ֹˮ�⡣
�����������1�������ڷ�Ӧ�в��������µ����ʣ�˫��ˮ�Ļ�ԭ�������ǣ����Դ�ѡA��
��2����ͬ���ڷ�Ӧ�в��������µ����ʣ������������Ʋ���ѡ�ã�BCD���ǿ��Եģ���ѡBCD��
�������ǵ���ʣ���ʹ������������۳�������������������������Ϊ������ǿ�ᣬ�����ܼ���
�ܽ���������������������������ˮ��
��3���Ȼ�ͭˮ�������ԣ�ˮ�������ȵģ����Լ��ȴٽ�ˮ�⣬���Ҫ�Ʊ��Ȼ�ͭ���壬Ӧ�����ڽϵ��¶��¼��������������壬ͬʱͨ���Ȼ��������ֹˮ�⡣
�����Ѷȣ�һ��
5������� ��ѧ��������й�����
��������ͨ��������Ҫԭ���Ǵ��ʯ��ʯ��______��
�ڸ����������лᷢ���绯ѧ��ʴ���为���ĵ缫��Ӧ��______��
�������нϸߵ�ǿ�Ⱥͻ�ѧ�ȶ��ԣ�������______�ṹ��
�ο��𰸣���������ͨ������ԭ�ϣ�ʯ��ʯ ���� ʯӢ���ʴ�Ϊ��ʯӢ��
�ڸ�����ʧȥ����ת���ɶ��������ӵ缫��Ӧʽ��Fe-2e-=Fe2+���ʴ�Ϊ��Fe-2e-=Fe2+��
�������Ӽ���пռ���״�ṹ���ʴ�Ϊ�����ͣ�����״����������״������
���������
�����Ѷȣ�һ��