1、实验题 (16分)某化学兴趣小组在进行钠在空气中燃烧的实验,请写出钠在氧气中燃烧的化学方程式:?。实验后,同学们发现除了得到黄色物质外,产物中还有黑色物质。兴趣小组的同学对产生的黑色固体物质进行实验探究。
查阅资料:
工业上采用铁环作阴极电解得到金属钠。实验室中金属钠的标签主要内容如下:
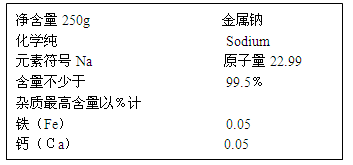
提出猜想:
猜想1:钠附着煤油,煤油的不完全燃烧可以生成碳单质;猜想2:?与钠反应也可以生成碳单质;
猜想3:?;?猜想4:……
设计实验方案,验证猜想:
实验目的
| 实验步骤
| 实验现象
| 结论
|
验证猜想1
| 将一小块钠从煤油中直接取出加热燃烧
取出一小块切去表皮并擦干净煤油的钠加热燃烧
| ?
?
?
?
?
?
| 黑色物质中含
有碳单质
|
验证猜想3
| ?
?
?
?
| ?
?
?
?
| 黑色物质中
含有铁元素
|
思考与交流:
同学们了解到金属钠在石棉网上燃烧,与石棉网作用也可以生成含铁的黑色物质,请你评价钠在石棉网上燃烧探究其在空气中燃烧产物是否合理并说明原因:?。
请设计实验验证猜想2(不要求写具体操作过程):?。
参考答案:2Na+O2 Na2O2;空气中的二氧化碳;金属钠中含有的铁也可能生成黑色物质;带煤油的钠燃烧产生黑色物质较多(或不带煤油的钠燃烧不产生或产生黑色物质少);取生成的黑色物质加足量硝酸溶解,滴加KSCN溶液;溶液变红色。不合理,石棉网中含有的铁元素以及空气中含有的碳元素均可能影响实验产物的鉴定。取两个坩埚各放入一小块切去表皮并擦干净煤油的钠,一个在除去CO2的空气中加热,另一个在空气中加热燃烧,观察燃烧产物的差别。
Na2O2;空气中的二氧化碳;金属钠中含有的铁也可能生成黑色物质;带煤油的钠燃烧产生黑色物质较多(或不带煤油的钠燃烧不产生或产生黑色物质少);取生成的黑色物质加足量硝酸溶解,滴加KSCN溶液;溶液变红色。不合理,石棉网中含有的铁元素以及空气中含有的碳元素均可能影响实验产物的鉴定。取两个坩埚各放入一小块切去表皮并擦干净煤油的钠,一个在除去CO2的空气中加热,另一个在空气中加热燃烧,观察燃烧产物的差别。
本题解析:钠在氧气中燃烧的化学方程式是2Na+O2 Na2O2;猜想2:CO2与Na反应也可以生成碳单质;猜想3:金属钠中含有的杂质铁也可能生成黑色物质;验证猜想1:将一小块钠从煤油中直接取出加热燃烧,带煤油的钠燃烧产生黑色物质较多;取出一小块切去表皮并擦干净煤油的钠加热燃烧,或不带煤油的钠燃烧不产生或产生黑色物质少。证明在黑色物质中含有碳单质。验证猜想3:取生成的黑色物质加足量硝酸溶解,滴加KSCN溶液;溶液变红色。黑色物质中含有铁元素。思考与交流:钠在石棉网上燃烧探究其在空气中燃烧产物是不合理的。原因是石棉网中含有的铁元素以及空气中含有的碳元素均可能影响实验产物的鉴定。实验验证猜想2的操作是取两个坩埚各放入一小块切去表皮并擦干净煤油的钠,一个在除去CO2的空气中加热,另一个在空气中加热燃烧,观察燃烧产物的差别。
Na2O2;猜想2:CO2与Na反应也可以生成碳单质;猜想3:金属钠中含有的杂质铁也可能生成黑色物质;验证猜想1:将一小块钠从煤油中直接取出加热燃烧,带煤油的钠燃烧产生黑色物质较多;取出一小块切去表皮并擦干净煤油的钠加热燃烧,或不带煤油的钠燃烧不产生或产生黑色物质少。证明在黑色物质中含有碳单质。验证猜想3:取生成的黑色物质加足量硝酸溶解,滴加KSCN溶液;溶液变红色。黑色物质中含有铁元素。思考与交流:钠在石棉网上燃烧探究其在空气中燃烧产物是不合理的。原因是石棉网中含有的铁元素以及空气中含有的碳元素均可能影响实验产物的鉴定。实验验证猜想2的操作是取两个坩埚各放入一小块切去表皮并擦干净煤油的钠,一个在除去CO2的空气中加热,另一个在空气中加热燃烧,观察燃烧产物的差别。
本题难度:一般
2、实验题 某化学兴趣小组用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体和胆矾晶体,以探索工业废料的再利用。其实验方案如下图所示。

(1)过滤用的仪器已有:滤纸、铁架台、铁圈和烧杯,还需要的玻璃仪器是__________。
(2)由滤液A制AlCl3溶液有途径I和途径Ⅱ两种,你认为合理的是_________,理由是_____________。
(3)从滤液E中得到绿矾的实验操作是_________。
(4)按环保要求,写出用滤渣F制备胆矾的各步反应的化学方程式___________________。
(5)有同学提出可将方案中最初溶解合金的烧碱改为盐酸,重新设计方案,也能得到三种物质,你认为后者的方案是否更合理_________,理由是______________________。
参考答案:(1)漏斗、玻璃棒
(2)Ⅱ;途径I制得的AlCl3 溶液中含有大量的NaCl,而途径Ⅱ能制得纯净的AlCl3溶液
(3)蒸发、浓缩、冷却结晶
(4) 2Cu+O2 = 2CuO;CuO+H2SO4 = CuSO4+H2O;CuSO4+5H2O = CuSO4・5H2O
(5)不合理;后者操作步骤多,消耗试剂量大,实验时间长
本题解析:
本题难度:一般
3、选择题 下列实验方案合理的是( )
A.鉴别甲烷和乙烯:分别点燃,观察火焰的颜色及是否有黑烟
B.检验酒精中的少量水:向酒精中加入足量生石灰
C.制备氯乙烷(C2H5Cl):将乙烷和氯气的混合气放在光照条件下反应
D.验证某RX是碘代烷,把RX与烧碱水溶液混合加热后,将溶液冷却后再加入硝酸银溶液观察是否出现黄色沉淀
参考答案:A、甲烷中的含碳量小于乙烯中的含碳量,所以乙烯燃烧会出现黑烟,但是甲烷不会,故A正确;
B、酒精中是否有水可以用无水硫酸铜检验,水可以使之变蓝,故B错误;
C、乙烷和氯气的混合气放在光照条件下反应的产物是混合物,最多的是氯化氢,故C错误;
D、验证某RX是碘代烷的方法:把RX与烧碱水溶液混合加热后,加入硝酸酸化,再将溶液冷却后再加入硝酸银溶液观察是否出现黄色沉淀,故D错误.
故选A.
本题解析:
本题难度:一般
4、选择题 下列实验的异常情况的原因分析不正确的是
选项
| 实验内容
| 实验的异常情况
| 原因分析
|
A
| 制备Fe(OH)2
| 观察不到白色沉淀
| 可能原料中的Fe2+被氧化或未隔绝空气
|
B
| 蒸发结晶
| 蒸发皿破裂
| ?酒精灯灯芯碰到热的蒸发皿底部或蒸发到剩少量液体时继续加热
|
C
| 分离水和CCl4
| 打开分液漏斗活塞后,下层液体难以流出
| 没有装漏斗上塞子拔掉或玻璃塞上凹槽与漏斗口侧面的小孔没有对齐
|
D
| 点燃法除去CO2中的CO杂质
| 无法点燃
| CO的着火点较高
参考答案:D
本题解析:D.点燃法除去CO2中的CO杂质,无法点燃的原因在于氧气很少,二氧化碳很多,二氧化碳不支持燃烧;正确操作为,通过灼热的氧化铜粉末。
本题难度:简单
5、实验题 (12分)实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子组成。取w g该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气。按下图所示装置进行实验。回答下列问题:
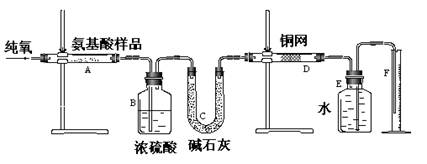
(1)实验开始时,首先通入一段时间的氧气,其理由是_?;
(2)以上装置中需要加热的仪器有______(填写字母),操作时应先点燃________处的酒精灯。
(3)A装置中发生反应的化学方程式是__________________?___________________。
(4)D装置的作用是??。
(5)实验中测得氮气的体积为V mL(标准状况),为确定此氨基酸的分子式,还需要的有关数据有_?__。
A.生成二氧化碳气体的质量
B.生成水的质量
C.通入氧气的体积
D.氨基酸的相对分子质量
参考答案:(12分)
(1)排尽体系中的N2_;
(2) AD ?D
(3) 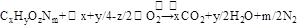
(4) 吸收未反应的氧气,保证最终收集的气体为N2
(5) ABD
本题解析:(1)注意由于装置中存在N2,则会影响对燃烧后产生N2体积的测量,所以需要充入氧气(2)A中物质需燃烧则加热? D中炽热的铜网才能除去氧气而达到吸收未反应的氧气则需加热?由于开始需通入氧气而要用炽热铜网除氧气则要先加热(3)由有机物燃烧的性质可知其产物,再由原子守恒配平即可,且注意条件的标注,(5)由质量守恒可知氨基酸的质量应为碳原子质量加氢原子质量加氧原子和氮原子的质量,由生成二氧化碳气体的质量可知其碳原子的质量,同理可知氢和氮的质量,由总质量减去已知原子的质量则知氧原子的质量,同时可以知道其各自的物质的量,由总质量除以摩尔质量可知有机物的物质的量,则可分别算出xyzm的值
本题难度:一般
|