1、选择题 下列说法正确的是( )
A.工业上用C还原Al2O3产生Al
B.氯水能使红色花瓣褪色
C.常温下,硅与浓HNO3反应放出NO2
D.Fe(OH)2溶于NaOH溶液
参考答案:B
本题解析:
本题难度:一般
2、选择题 把一定量的铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的浓度恰好相等。则已反应的Fe3+和未反应的Fe3+的物质的量之比为?(?)
A.1:1
B.1:2
C.2:3
D.3:2
参考答案:C
本题解析:
Fe +2Fe3+=3Fe2+
1? 2? 3
从上述离子方程式得,若反应2molFe3+(即已反应的Fe3+),生成3molFe2+而所得溶液中Fe2+和Fe3+的溶度恰好相等,即未反应的Fe3+的物质的量为3mol所以答案2:3,故选C。3+和Fe2+的转换的计算
点评:本题考查Fe3+和Fe2+的转换的计算,只需列出反应方程式,通过假设即可算出,不难理解。
本题难度:一般
3、填空题 现有Fe、Cu组成的合金,其中Cu、Fe的总物质的量为a mol,Cu的物质的量分数为x;研成粉末后,全部投入含b mol HNO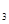 的稀溶液中,微热使其充分反应,且硝酸的还原产物只有NO,试回答下列问题:
的稀溶液中,微热使其充分反应,且硝酸的还原产物只有NO,试回答下列问题:
(1)若剩余的残渣只有Cu,则溶液中含有的金属离子为__________。(写出所有可能情况)
(2)当溶液中金属离子只有Fe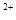 、Cu
、Cu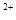 时,则b的取值范围是(用a、x表示)___________。
时,则b的取值范围是(用a、x表示)___________。
(3)当x=0.5,溶液中Fe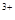 与Fe
与Fe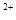 的物质的量相等时,在标准状况下共产生672 mL气体。则a=____________、b=_____________。
的物质的量相等时,在标准状况下共产生672 mL气体。则a=____________、b=_____________。
参考答案:(1)? Fe2+或Fe2+、Cu2+ (2分)
(2) 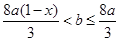 ?(2分)
?(2分)
(3)? a=0.04mol? b=0.12mol (2分)
本题解析:(1) Cu、Fe的混合物与稀硝酸反应,金属可能有剩余,可能没有剩余.金属可能有剩余时,根据共存可知,剩余金属有两种情况:
①剩余Fe、Cu,当有Fe剩余时,溶液中能与Fe反应的Fe3+、Cu2+都不存在,所以溶液中只有Fe2+;
②只剩余Cu,溶液中一定不存在与Cu反应的Fe3+,根据离子共存,溶液可能只有Fe2+;
③通过②知,溶液中还可能存在的离子是Fe2+、Cu2+;
④当固体没有剩余时,可能存在的情况是:当Fe恰好与硝酸反应生成Fe2+,Cu恰好与硝酸生成Cu2+,所以溶液中存在的离子是Fe2+、Cu2+;
⑤通过④知,固体没有剩余时,生成的Fe3+部分反应,根据离子共存,溶液中存在的离子可能的Fe2+、Fe3+、Cu2+;
⑥通过④、⑤知,固体没有剩余时,铁、铜全部被氧化成离子,根据离子共存,溶液中存在的离子可能是Cu2+、Fe3+;
有如下情况:
残留固体成分
Fe、Cu
Cu
Cu
--
--
__
溶液中的金属离子
Fe2+
Fe2+
Fe2+、Cu2+
Fe2+、Cu2+
Fe2+、Fe3+、Cu2+
Cu2+、Fe3+
?
(2)当溶液金属离子只有Fe2+、Cu2+时,说明Cu恰好完全反应或者有剩余,而HNO3和Fe则完全反应(否则的话,如果有硝酸剩余,则Fe2+则会被进一步氧化为Fe3+;如果有Fe剩余,则会和Cu2+继续反应)
3Cu+8HNO3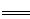 3Cu(NO3)2+2NO↑+4H2O
3Cu(NO3)2+2NO↑+4H2O
ax?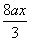
3Fe? +? 8HNO3 3Fe(NO3)2+2NO↑+ 4H2O?
3Fe(NO3)2+2NO↑+ 4H2O?
a(1-x)?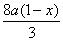
总耗用硝酸量:n(HNO3)=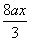 +
+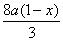 ?=
?=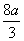
所以: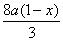 <b≤
<b≤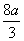
(3)当溶液中为Fe3+、Fe2+时,说明Cu、Fe完全反应(如果未完全反应,则Cu和Fe会和Fe3+反应),并且HNO3也完全反应没有剩余(如果有硝酸剩余,则Fe2+则会被进一步氧化为Fe3+)溶液中Fe3+、Fe2+的物质的量相等,说明有一半Fe变为Fe3+,一半变为Fe2+
当x=0.5,nFe3+=nFe2+? V(NO)=0.672L
则nFe3+=nFe2+="0.25a" mol? nCu = 0.5amol
此时3Fe+8HNO3 3Fe(NO3)2+2NO↑+4H2O?①
3Fe(NO3)2+2NO↑+4H2O?①
3Cu+8HNO3 3 Cu (NO3)2+2NO+4H2O?②
3 Cu (NO3)2+2NO+4H2O?②
3Fe(NO3)2+4HNO3 3Fe(NO3)3+NO+2H2O?③
3Fe(NO3)3+NO+2H2O?③
反应均发生了,且无反应物剩余。
3Fe?+? 8HNO3 3Fe(NO3)2+2NO↑+4H2O?①?
3Fe(NO3)2+2NO↑+4H2O?①?
0.5a? 0.5a×8/3? 0.5a? 0.5a×2/3
3Cu+8HNO3? ?3 Cu (NO3)2+2NO↑+4H2O?②?
?3 Cu (NO3)2+2NO↑+4H2O?②?
0.5a? 0.5a×8/3? 0.5a? 0.5a×2/3?
3Fe(NO3)2+4HNO3 ?3Fe(NO3)3+NO+2H2O?③
?3Fe(NO3)3+NO+2H2O?③
0.25a? 0.25a ×4/3? 0.25a
0.5a×2/3 +0.5a×2/3 + 0.25a×1/3 =0.672L/22.4L・mol-1=0.03mol
解得:a="0.04" mol?
b=" 0.5a×8/3" + 0.5a×8/3+0.25a ×4/3="3a=3×0.04" mol ="0.12" mol
本题难度:一般
4、填空题 已知氯化铁溶液跟铜反应生成氯化铜和氯化亚铁。电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是?,证明Fe3+存在的现象是?。
(2)写出FeCl3溶液与金属铜发生反应的离子方程式(1分):?
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:
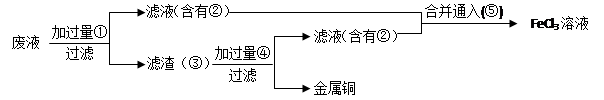
A.请写出上述实验中加入或生成的有关物质的化学式:
①?,②?,④?,
B.请写出含有②的滤液与⑤反应的离子方程式(1分):?
该反应中氧化剂为?还原剂为?。
参考答案:(9分)(1)KSCN;溶液呈红色 ;(2) 2Fe3++Cu=2Fe2++Cu2+
(3) A.①Fe ,②FeCl2,④HCl? B. 2Fe2+ + Cl2 ="=" 2Fe3+ + 2Cl-;Cl2;FeCl2
本题解析:(1)铁离子能和KSCN溶液发生显色反应,溶液显红色,所以检验溶液中Fe3+存在的试剂是能和KSCN溶液。
(2)氯化铁能和氧化金属铜,反应的离子方程式是2Fe3++Cu=2Fe2++Cu2+。
(3)要从废液中回收金属铜,则需要加入还原剂铁粉,即①是Fe。过滤后生成的滤液是氯化亚铁,即②是氯化亚铁。而滤渣中含有铜和剩余的铁,则需要加入稀盐酸溶解铁,即④是HCl。滤液中含有氯化亚铁,要转化为氯化铁,则需要通入氯气将氯化亚铁氧化生成氯化铁即可。
点评:该题是高考中的常见题型,属于中等难度的试题,试题综合性强,注重能力的培养。该类试题,综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。
本题难度:一般
5、填空题 铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式:?。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、
负极,并写出电极反应式。
正极反应:?。
负极反应:?。
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10 mol・L-1,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤?。
?
| 氢氧化物开始沉淀时的pH
| 氢氧化物沉淀
完全时的pH
|
Fe3+
Fe2+
| 1.9
7.0
| 3.2
9.0
|
Cu2+
| 4.7
| 6.7
|
提供的药品:Cl2 浓H2SO4 NaOH溶液 CuO Cu
|
?
(4)某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显。请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀。有关反应的化学方程式?;?;劣质不锈钢腐蚀的实验现象?。
参考答案:(1)2Fe3++Cu=2Fe2++Cu2+
(2)装置图
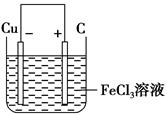
正极反应:Fe3++e-=Fe2+(或2Fe3++2e-=2Fe2+)
负极反应:Cu=Cu2++2e-(或Cu-2e-=Cu2+)
(3)①通入足量氯气将Fe2+氧化成Fe3+;②加入CuO调节溶液的pH至3.2~4.7;③过滤[除去Fe(OH)3]
(4)CuO+H2SO4=CuSO4+H2O? CuSO4+Fe=FeSO4+Cu?不锈钢表面有紫红色物质生成
本题解析:(2)根据2Fe3++Cu=2Fe2++Cu2+氧化还原反应和原电池的工作原理进行设计,铜作负极,石墨作正极,FeCl3作电解质溶液。
(3)先通入足量Cl2将Fe2+氧化成Fe3+,Cl2+2Fe2+=2Fe3++2Cl-,再加入CuO来调节溶液的pH至3.2~4.7,使Fe3+转化为Fe(OH)3沉淀,过滤达到除去CuCl2溶液中Fe3+和Fe2+的目的。
(4)根据题中信息,选两种药品为CuO,浓H2SO4,水。
CuO+H2SO4=CuSO4+H2O
Fe+CuSO4=Cu+FeSO4
现象为:不锈钢表面有紫红色物质生成。
本题难度:一般