1、选择题 在含Al3+、Fe3+、Fe2+、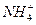 的稀溶液中,加入足量Na2O2固体,充分作用后,再加入过量稀盐酸,完全反应,离子数目基本不变的是 (? )
的稀溶液中,加入足量Na2O2固体,充分作用后,再加入过量稀盐酸,完全反应,离子数目基本不变的是 (? )
A.Al3+
B.Fe3+
C.Fe2+
D.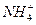
参考答案:A
本题解析:在整个过程中,Al3+的有关反应有:
Al3++4OH-====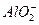 +2H2O
+2H2O
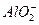 +4H+Al3++2H2O
+4H+Al3++2H2O
本题难度:一般
2、填空题 (6分)铁和铜作为常见金属,在生活中有着广泛的应用。
(1)硫酸铁在工业上可用于电化浸出黄铜矿精矿工艺。精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S。(CuFeS2中S为-2价)则下列说法正确的是?(选填序号);
a.从物质分类的角度看,黄铜矿属于合金
b.反应中,所有铁元素均被还原
c.反应中,CuFeS2既作氧化剂又作还原剂
d.当转移1mol电子时,46 g CuFeS2参加反应
(2)实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为:4CuI + Hg = Cu2HgI4 + 2Cu,以上反应中的氧化剂为______; CuI可由Cu2+与I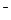 直接反应制得,请配平下列反应的离子方程式:?Cu2+ + ?I
直接反应制得,请配平下列反应的离子方程式:?Cu2+ + ?I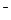 ?― ?CuI + ?I
?― ?CuI + ?I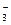
参考答案:(1)d?(2)CuI?2 ?Cu2+ + ?5 ?I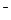 ?=?2 ?CuI + ?1 ?I
?=?2 ?CuI + ?1 ?I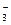
本题解析:略
本题难度:一般
3、计算题 (6分)铜是生命必需的元素,也是人类最早使用的金属之一,铜的生产和使用对国计民生各个方面产生了深远的影响。在化学反应中,铜元素可表现为0价、+1价、+2价。
(1)在西汉古籍中曾有记载:曾青得铁则化为铜〔即:曾青(CuSO4)跟铁反应生成铜〕,试写出该反应的离子方程式:____________________________________。
(2)尽管铜比铁较为稳定,但铜器表面经常会生成铜锈〔即:铜绿,化学式Cu2(OH)2CO3〕,其中生成铜绿的反应物除铜外还有O2、CO2和H2O。试写出保护铜制品的方法:________________________________________。
(3)铜钱在历史上曾经是一种广泛流通的货币。试从物理性质和化学性质的角度分析为什么铜常用于制造货币。(铜的熔点是1 183.4 ℃,铁的熔点是1 534.8 ℃)
参考答案:(1)Fe+Cu2+====Fe2++Cu
(2)在干燥空气中保存
(3)铜的化学性质比较稳定,不易被腐蚀,铜的熔点比较低,容易冶炼铸造成型
本题解析:湿法冶金我们在初中学过,防止铜器的生锈由防止铁生锈类比得出,根据铜的一些性质可以回答出第(3)问。
本题难度:简单
4、选择题 要检验久置的FeSO4溶液是否含有Fe2(SO4)3,应选用的试剂是
A.NH4SCN溶液
B.KI溶液
C.氨水
D.Fe粉
参考答案:A
本题解析:略
本题难度:一般
5、计算题 (10分)使250 mL密度为1.1 g・cm-3、质量分数为24.5%的硫酸跟铁屑充分反应。计算:
(1)此硫酸中H2SO4的物质的量浓度。
(2)生成H2的体积(标准状况)。
(3)将生成的硫酸亚铁配制成400? mL溶液,此溶液中硫酸亚铁的物质的量浓度是多少?
参考答案:(1)2.75 mol・L-1
(2)15.4 L
(3)1.73 mol・L-1
本题解析:(1)c= ="2.75" mol・L-1。
="2.75" mol・L-1。
(2)n(H2SO4)="2.75" mol・L-1×0.250 L="0.688" mol
根据Fe+H2SO4====FeSO4+H2↑即知生成的氢气也为0.688 mol,在标准状况下的体积为0.688 mol×22.4 L・mol-1="15.4" L。
(3)从(2)中可以求出硫酸亚铁也是0.688 mol,则c(FeSO4)= ="1.73" mol・L-1。
="1.73" mol・L-1。
本题难度:简单