1������� ��1��ͭ����������ʹ�õĽ���֮һ��������ұ��ͭ��һ����Ӧ��
Cu2S+2Cu2O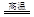 6Cu+SO2
6Cu+SO2
�÷�Ӧ�б�������Ԫ����?������Ӧ��ת��1mol���ӣ��õ�Cu?mol��?
��2���������ַ����������Ʊ�CuSO4��
����һ��2Cu+O2 2CuO��CuO+H2SO4=CuSO4+H2O
2CuO��CuO+H2SO4=CuSO4+H2O
��������Cu+2H2SO4��Ũ�� CuSO4+SO2��+2H2O
CuSO4+SO2��+2H2O
�ټ���ij����������CuSO4����ѡ��һ�ַ�������˵�����ɣ�?
?��
����ͬѧ��Ϊ�����ɵ���������ͭ���ַ������ĵ�������ͬ����Ϊ��Ӧ����ͭת��ΪCuSO4������Ϊ����˵��?�����ȷ������ȷ������ԭ����?
?��
�ο��𰸣���1��S������(1��)? 1? (1��)?
��2���ٷ���һ(1��)������ԭ�������ʸߣ��Ի�����ȾС(1��)?
�ڲ���ȷ? (1��)?��Ӧ������ﲻ��ȫ��ͬ���ʷ�Ӧ����ЧӦ��ͬ�����ĵ�����Ҳ��ͬ(2��)
�����������1�����ϼ����ߵ�Ԫ����S�����ϼ۽��͵�ֻ��Cu ��Cu�ӣ�1�۵�0�ۣ���ת��1mole��ʱ�õ�1molCu?
��2�����ɷ���ʽ��֪���ɵ�����CuSO4�������������һ�٣��ҷ���һ����Ⱦ���ʴ�Ϊ������һ������ԭ�������ʸߣ��Ի�����ȾС��
����Ӧ�з�Ӧ������ﲻ��ȫ��ͬ���ʷ�Ӧ����ЧӦ��ͬ�����ĵ�����Ҳ��ͬ���ʲ���ȷ
�����Ѷȣ�һ��
2��ѡ���� �����йؽ���Ԫ�ؼ��仯����˵������ȷ����
A������������Ӧ�����������������ᷴӦ������������
B��ͭ�ڳ�ʪ�Ŀ��������������ɫ�������Ҫ�ɷ��Ǽ�ʽ̼��ͭ
C���������ƺ������ƾ�������ˮ��������̼��Ӧ�������ɵIJ��ﲻ��ȫ��ͬ
D�������������ֱ�����������ͼ���Һ��Ӧ��������������һ����ͬ
�ο��𰸣�D
���������A����������ǿ�����ԣ������Ƿ��������ᣬ�������������Ӧ�����������������ᷴӦ�����������ӣ�A����ȷ��B��ͭ�ڳ�ʪ�Ŀ����������ⱻ��ʴ����ɫ�������Ҫ�ɷ��Ǽ�ʽ̼��ͭ[Cu2(OH)2CO3]��B��ȷ��C���������Ǽ����������ˮ��Ӧ�����������ƣ���CO2��Ӧ����̼���ƻ�̼�����ɡ��������Ʋ��Ǽ����������ˮ��Ӧ�����������ƺ���������CO2��Ӧ����̼���ƺ�������C��ȷ��D����������Ӧ���ɵ������������������ᷴӦ��һ������������������ϡ���ᷴӦ����NO�����Ե����������ֱ�����������ͼ���Һ��Ӧ����������������һ����ͬ��D����ȷ����ѡD��
�����Ѷȣ�һ��
3������� ��ҵ������������Ҫ�ɷ���A1203������������Fe203��SiO2����ȡұ������ԭ������������������ͼ��ͼ��
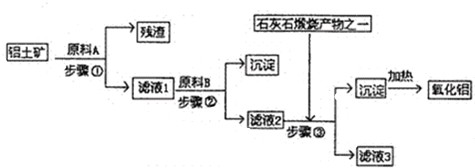
��1��ԭ��A��������______������ٷ�Ӧ�����ӷ���ʽ��______��
��2����Һ1��Ҫ�����Թ���ԭ��B��ԭ��B�Ļ�ѧʽ��______������ڷ�Ӧ�����ӷ���ʽ�ǣ�______��
��3������۵����ӻ�ѧ����ʽ�ǣ�______��
��4������٢ڢ۵IJ�������______����������ƣ���Ҫ����Al��OH��?3�����Ƿ���ȫ�ķ�����______��
��5�����ʡȥ����٣����ܽ��������ǴӼ���ԭ��B��ʼ����������������ȡ��ʲôӰ�죿______��
�ο��𰸣��ɹ������̿�֪�����ͨ���Ϊ������̼�����ɵij���Ϊ����������������Һ2����AlO2-�������Ӧ�����������ƣ�������Һ1�к���Al3+�������ӦΪ�������ᣬ��ȥSiO2��
��1��������������֪������ټ������ᣬ��ȥSiO2������ԭ��AΪ���ᣬ
���������ᷴӦ���ӷ���ʽΪAl2O3+6H+=2Al3++3H2O�������������ᷴӦ���ӷ���ʽΪFe2O3+6H+=2Fe3++3H2O��
�ʴ�Ϊ��Al2O3+6H+=2Al3++3H2O��Fe2O3+6H+=2Fe3++3H2O��
��2������ټ���������ᣬ��Һ1�к���Al3+��Fe3+��H+�ȣ�Ӧ�����������ƣ���ȥ�����ӣ���������ת��ΪAlO2-����ӦΪ?H++OH-=H2O��Fe3++3OH-=Fe��OH��3����Al3++4OH-=AlO2-+2H2O��
�ʴ�Ϊ��NaOH��?H++OH-=H2O��Fe3++3OH-=Fe��OH��3��Al3++4OH-=AlO2-+2H2O��
��3����Һ2����AlO2-�������ͨ�������̼����AlO2-��Ӧ���ɵij���Ϊ����������
��Ӧ��ѧ����ʽΪNaAlO2+CO2+2H2O=Al��OH��3��+NaHCO3��
�ʴ�Ϊ��NaAlO2+CO2+2H2O=Al��OH��3��+NaHCO3��
��4���ɹ������̿�֪����٢ڢ۵IJ������ǹ��ˣ�����Al��OH��?3�����Ƿ���ȫ��ֻҪ������Һ3���Ƿ���AlO2-���ɣ�ȡ��Һ3���ϲ���Һ��ͨ�������̼�������ֻ��ǣ���˵����������ȫ���������ֻ��ǣ���˵��������ȫ��
�ʴ�Ϊ�����ˣ�ȡ��Һ3���ϲ���Һ��ͨ�������̼�������ֻ��ǣ���˵����������ȫ���������ֻ��ǣ���˵��������ȫ��
��5������NaOH��Һ�ܽ����������в���SiO2�ܽ���NaOH��Һ�����ɹ����ƣ�ͨ�������̼�����ɹ�����������ʹ�����Ƶõ�Al2O3����SiO2���ʣ�
�ʴ�Ϊ������NaOH��Һ�ܽ����������в���SiO2�ܽ���NaOH��Һ�����ɹ����ƣ����ʹ�����Ƶõ�Al2O3����SiO2���ʣ�
���������
�����Ѷȣ�һ��
4������� (10��)����0.8 mol��ϡ��������������22.4 g�����ۣ����跴Ӧ��Ϊ�����Ρ�
��һ��Ϊ��Fe��HNO3(ϡ)�D��Fe(NO3)3��NO����H2O
��1��д���������η�����Ӧ�����ӷ���ʽ��
��һ�Σ�?��
�ڶ��Σ�?��
��2����ȷ�����������η�Ӧ�У��������۵����ʵ�������Һ����Ԫ�ش��ڵ���ʽ�Ĺ�ϵ
?
?
?��
��3����ͼ�л�����Һ��Fe2����Fe3����NO�����ʵ�����������۵����ʵ����仯�Ĺ�ϵͼ��(������Ϊ�������۵����ʵ���������������Һ�����ӵ����ʵ���)��
�ο��𰸣���1��Fe��4H����NO��Fe3����NO����2H2O? 2Fe3����Fe��3Fe2��
��2���ټ���Fe��Ϊ0��0.2 molʱ��������ʽΪFe3����
�ڼ�������Ϊ0.2��0.3 molʱ��������ʽΪFe2����Fe3����
�ۼ�Fe��Ϊn(Fe)��0.3 molʱ��������ʽΪFe2����
��3����ͼ�� 
�����������1����һ�ε����ӷ���ʽΪ��Fe��4H����NO��Fe3����NO����2H2O���ڶ��μ����Fe�Ὣ���ɵ�Fe3+��ԭ��Fe2+�����ӷ���ʽΪ2Fe3����Fe��3Fe2����
��2����һ����0.8mol������������0.2mol������Fe3+0.2mol���ڶ�����������0.1mol������Fe2+0.3mol�����Ե����ۼ���������0.2molС��0.3molʱ������Fe3+������Fe2+��
��3���˹��̵�ͼ��Ϊ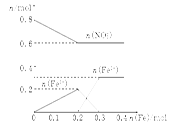
�����������ѶȽϴ���Ҫ����ѧ������������Fe�Ĵ��ڷ�ʽ��
�����Ѷȣ�һ��
5��ѡ���� �����йؽ������仯�����˵����ȷ����?
[? ]
A�����ڹ��ڳ����²�����������Ӧ����������Ʒ����һ���Ŀ���ʴ���ܣ���һ��Ӧ�ù㷺�Ľ�������
B����FeCl3��Һ�е������KI��Һ����Һ����ɫ
C������ɫʯ����Һ�м��������Na2O2��ĩ������Һ��Ϊ��ɫ�������ݲ���
D��װ���Ŵ�ʹ�õ����Ͻ���ϵ�Ӳ�ȱ���С���۵������
�ο��𰸣�B
���������
�����Ѷȣ���