1、选择题 下列实验操作正确的是( )
A.测定某浓度盐酸的pH时,先将pH试纸用蒸馏水湿润
B.蒸馏时,将温度计的水银球插入蒸馏烧瓶中液面以下
C.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.中和滴定时,锥形瓶必须洗净并烘干后才能使用
2、选择题 下列实验操作与预期实验目的或所得实验结论一致的是
[? ]
实验操作?
实验目的或结论
A.
某钾盐溶于盐酸,产生能使澄清石灰水变浑浊
的无色无味气体
说明该钾盐是K2CO3
B.
向含有少量FeCl3的CuCl2溶液中加入足量Cu粉,
搅拌一段时间后过滤
除去CuCl2溶液中少量FeCl3的,
提纯CuCl2溶液
C.
常温下,向饱和Na2CO3溶液中通入过量CO2,
溶液变浑浊
说明常温下NaHCO3溶解度比
Na2CO3溶解度小
D.
C2H5OH与浓硫酸在170℃共热,将制得的气体
直接通入酸性KMnO4溶液
检验制得气体是否为乙烯
3、选择题 下列各项中“操作或现象”能达到预期“实验目的”的是
A.A
B.B
C.C
D.D
4、选择题 海藻中含有丰富的、以离子形式存在的碘元素。下图是实验室从海藻里提取碘的流程的一部分。
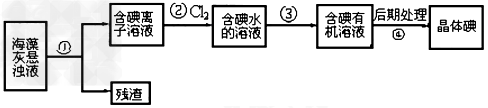
下列判断正确的是
[? ]
A.步骤①、③的操作分别是过滤、萃取?
B.可用淀粉溶液检验步骤②的反应是否进行完全 ?
C.步?骤③中加入的有机溶剂是裂化汽油或乙醇 ?
D.步骤④的操作是过滤
5、简答题 为测定碳酸钙纯度(设所含杂质为SiO2),同学们设计了如下两个实验方案:
【方案I】
(1)组装发生并测定生成气体体积的实验装置,并检验气密性;
(2)称取碳酸钙样品Wg;
(3)加入过量盐酸;
(4)收集并测定生成的气体体积VmL.
问题I-1:如果称量样品时,砝码底部有一处未被实验者发现的残缺,那么测定的碳酸钙的纯度会______(填“偏高、偏低、无影响”).
问题I-2:在方框中画出测定生成的气体体积的装置简图.
【方案II】
(1)称取碳酸钙样品Wg;
(2)在锥形瓶中用Cmol/L盐酸VmL(过量)溶解样品;
(3)加入甲基橙作指示剂,再用浓度为C1mol/L的标准氢氧化钠溶液滴定过量的盐酸,用去氢氧化钠溶液V1毫升.(已知甲基橙的变色范围是pH=3.1~4.4)
问题II-1:未滤去不溶物SiO2,对测定结果是否有影响?(填有或无)______;
理由是______.
问题II-2:碳酸钙纯度表达式______.
【方案评价】
你认为以上两个方案中,最好的方案是______,
另一个方案不够好的理由是______.
