1、选择题 如果发现了原子序数为116的元素,对它的描述正确的是(? )
①位于第7周期?②是非金属元素?③最外电子层含有6个电子?④没有放射性?⑤属于氧族元素?⑥属于卤素
A.①③⑤
B.①③⑥
C.②④⑥
D.②③⑤
参考答案:A
本题解析:116号元素位于第7周期ⅥA族,属于氧族元素,为金属元素,具有放射性。
本题难度:简单
2、填空题 (11分)
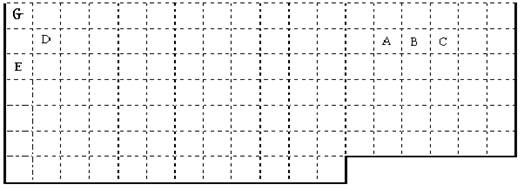
根据信息回答下列问题:
(1)?上表中实线是元素周期表的部分边界,请你用实线标出表的上边界,并把符合下列要求的元素的元素符号标在表中对应位置处。
① 最高价氧化物的水化物碱性最强(放射性元素除外)。?
② 电负性最大。?
③ 第一电离能对大。
(2)F元素的原子核外有25个运动状态不同的电子,F元素是?(名称),F2+的未成对电子数是_____ ,与F之具有相同最高正价的另一同周期元素的单质在常温下的状态为?。(填固态、液态、气态)
(3)列举一种由A、C、E、G四种元素组成的盐?。
(4)D的最高价氧化物对应的水化物属两性化合物,证明这一结论的有关离子方程式为_______________________________、_____________________________
(5)元素M基态原子中次外层有5个未成对电子而最外层只有一个电子; MCl3能与B和C的氢化物共同形成配位数为6的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。MCl3形成的配合物的化学式为_____? ___(用具体元素符号表示)。
参考答案:(1)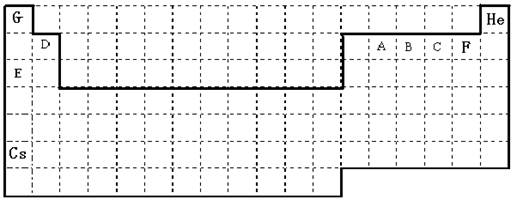
(2)锰? 5?液态?(3)NaHCO3等有机羧酸的钠盐均可(合理答案均军给分)
(4)Be(OH)2+2H+===Be2++2H2O? Be(OH)2+2OH-===BeO+2H2O
(5)[Cr(NH3)4(H2O)2]Cl3
本题解析:(1)考查元素周期表的结构。最高价氧化物的水化物碱性最强Cs,电负性最大是F,第一电离能最大的稀有气体He。
(2)F元素的原子核外有25个运动状态不同的电子,所以F元素是锰元素。根据构造原理可知,F2+的未成对电子数是5. 与锰具有相同最高正价的另一同周期元素是溴元素,其单质在常温下是液态。
(3)A、C、E、G四种元素分别是C、O、Na、H,所以该盐可以是碳酸氢钠或醋酸钠等。
(4)氢氧化物具有两性,则既能和酸反应生成盐和水,也能和碱反应生成盐和水。
(5)元素M基态原子中次外层有5个未成对电子而最外层只有一个电子,则M是铬元素。氨气和水的物质的量之比为2∶1,三个氯离子位于外界,所以结构简式为[Cr(NH3)4(H2O)2]Cl3。
本题难度:一般
3、选择题 短周期元素X、Y、Z、W在元素周期表中的相对位置如图6所示,其中W原子的最外层电子数是最内层电子数的3倍。下列判断正确的是
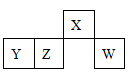
A.原子半径:rW>rZ>rY>rX
B.含Y元素的盐溶液一定显酸性
C.最简单气态氢化物的热稳定性:Z>W
D.X与氢元素组成的离子化合物XH5与水反应可产生两种气体
参考答案:D
本题解析:由题干信息可知W是硫,X是氮,Y是铝,Z是硅。A中同一周期从左到右原子半径依次是减小的,一般而言,原子的电子层数越多原子半径就越大,正确顺序为rY> rZ>rW>rX,错误;B是铝元素,其铝离子的盐溶液显酸性,其偏铝酸根离子的盐溶液显碱性,错误;C同一周期从到右非金属性增强,最简单气态氢化物的热稳定性也相应增强,应该是W>Z,错误;D 中XH5实际上是氢化铵NH4H,与水反应后生成氨气和氢气,正确;
本题难度:一般
4、选择题 短周期元素A、B、C,原子序数依次递增。已知:A、C同主族,而且三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半。下列叙述正确的是?(?)
A.原子半径:A<B<C?
B.沸点:A的氢化物低于C的氢化物
C.常温下,B的硫酸盐溶液pH<7?
D.5.6 g铁与足量的C化合,转移0.3 mol电子
参考答案:C
本题解析:略
本题难度:一般
5、选择题 根据元素周期律判断,下列递变规律不正确的是?(?)
A.Na、Mg、Al的金属性依次减弱
B.HCl、HBr、HI的稳定性依次增强
C.HclO4、H2SO4、H3PO4的酸性依次减弱
D.Li、Na、K分别与水反应的剧烈程度依次增强
参考答案:B
本题解析:Na、Mg、Al的金属性依次减弱,同周期元素自左至右金属性渐弱,故说法正确。
本题难度:一般