1、选择题 核外电子层结构相同的一组粒子是( )。
A.Mg2+、Al3+、Cl-、Ne
B.Na+、F-、S2-、Ar
C.K+、Ca2+、S2-、Ar
D.Mg2+、Na+、Cl-、S2-
参考答案:C
本题解析:C项粒子均为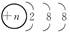 结构。
结构。
本题难度:一般
2、填空题 现有部分前36号元素的性质或原子结构如下表:
元素编号
| 元素性质或原子结构
|
R
| 基态原子的最外层有3个未成对电子,次外层有2个电子
|
S
| 单质能与水剧烈反应,所得溶液呈弱酸性
|
T
| 基态原子3d轨道上有1个电子
|
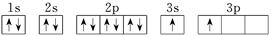
X
| 
|
?
(1)R元素的第一电离能要大于其同周期相邻的元素,原因是____________________________________。
R原子的结构示意图是?。
(2)S元素的最常见化合价为________,原因是________________________________________。
(3)T元素原子的价电子构型为________。
(4)X的电子排布图违背了____________。用X单质、碱金属盐及碱土金属盐等可以做成焰火。燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:_________________________________。
参考答案:(1)原子的2p轨道半充满,能量低,稳定 (2分)示意图略(1分)
(2)-1(1分)? F的电负性最大,只能得电子(2分) (3)3d14s2(1分)
(4)能量最低原理(1分)电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量(2分)
本题解析:基态原子的最外层有3个未成对电子,次外层有2个电子,这说明R是第二周期元素,则R是氮元素;单质能与水剧烈反应,所得溶液呈弱酸性,则S是F元素;基态原子3d轨道上有1个电子,则根据构造原理可知,T是21号元素钪元素;X的核外电子数是12个,实验X是Mg元素。
(1)由于氮元素原子的2p轨道半充满,能量低,稳定性强,所以氮元素的第一电离能要大于其同周期相邻的元素。氮元素是第二周期第ⅤA族元素,所以R原子的结构示意图是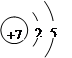 。
。
(2)由于F的电负性最大,属于第ⅦA族元素,只能得到1个电子,所以常见化合价是-1价。
(3)根据构造原理可知钪元素原子的价电子构型为3d14s2。
(4)由于3s能级的能量低于3p能级的能量,所以核外电子首先排满3s,然后在排3p能级。因此根据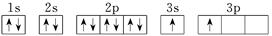 可知,电子排布图违背了能量最低原理。由于电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量,所以碱金属盐及碱土金属盐等可以做成焰火。
可知,电子排布图违背了能量最低原理。由于电子从能量较高的轨道跃迁到能量较低的轨道时,以光的形式释放能量,所以碱金属盐及碱土金属盐等可以做成焰火。
本题难度:一般
3、选择题 如图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是
A.Y的氢化物比R的氢化物稳定
B.原子半径大小顺序是Z>Y>X
C.Y、R形成化合物的化合物YR2能使KMn O4溶液褪色
O4溶液褪色
D.X、Z可形成化合物XZ3,且该化合物属离子化合物
参考答案:C
本题解析:略
本题难度:一般
4、填空题 表示原子结构常用的化学用语有:原子结构示意图、核外电子排布式、轨道表示式、电子式等。选择其中最详尽描述核外电子运动状态的方式来表示氧元素原子核外电子的运动状态?;氧元素原子核外有?种不同能量的电子;
参考答案: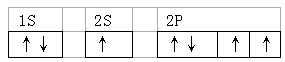 ?,3种
?,3种
本题解析:能最详尽描述核外电子运动状态的是轨道表达式,则根据构造原理可知,氧元素原子核外电子的轨道表达式是 。同一能层上的电子其能量是相同的,所以氧元素原子核外有3种不同能量的电子。
。同一能层上的电子其能量是相同的,所以氧元素原子核外有3种不同能量的电子。
点评:该题是基础性试题的考查,难度不大。试题紧扣教材,基础性强,侧重对学生基础知识的巩固,同时兼顾对学生能力的培养。
本题难度:一般
5、选择题 元素的原子结构决定其性质和在周期表中的位置。下列叙述正确的是
A.多电子原子中,在离核较近的区域内运动的电子能量较高
B.原子核外电子的数目越多,电子的运动状态就越多
C.轨道表示式,是对原子核外电子运动状态最完美的描述
D.所有元素原子的最外层电子数都等于该元素的最高化合价
参考答案:B
本题解析:A、离核较近的区域能量较低,多电子原子中,能量高的电子在离核较远的区域内运动,故A错误;B、核外电子没有运动状态相同的电子,核外有几个电子就有几种运动状态不同的电子,故B正确; C、轨道表示式不能像电子云那样形象表示电子在一定区域运动,故C错误;D、O元素、F元素一般没有正化合价,故D错误,答案选B。
本题难度:一般