1、选择题 甲酸和乙酸都是弱酸,当它们的浓度均为0.10mol/L时,甲酸中的c(H+)约为乙酸中c(H+)的3倍.现有两种浓度不等的甲酸溶液a和b,以及0.10mol/L的乙酸,经测定它们的pH从大到小依次为a、乙酸、b.由此可知( )
A.a的浓度必小于乙酸的浓度
B.a的浓度必大于乙酸的浓度
C.b的浓度必小于乙酸的浓度
D.b的浓度必大于乙酸的浓度
参考答案:A
本题解析:
本题难度:简单
2、选择题 下列叙述正确的是( )
A.在醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b
B.pH=3的盐酸与pH=11的氨水等体积混合,混合溶液呈酸性
C.等体积等浓度的氢氧化钠与醋酸混合:c(Na+)=c(CH3COO-)
D.若1?mL?pH=1的盐酸与100?mL?NaOH溶液混合后,溶液的pH=7则NaOH溶液的pH=11
参考答案:D
本题解析:
本题难度:简单
3、选择题 相同条件下,等体积、等pH的醋酸溶液和盐酸分别加水稀释后,溶液的pH仍相同,则所得溶液的体积为下列的
A.仍相同
B.醋酸溶液的大
C.盐酸的大
D.无法判断
参考答案:B
本题解析:
本题难度:一般
4、选择题 用水稀释 时,溶液中随着水量的增加而减小的是
时,溶液中随着水量的增加而减小的是
A.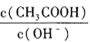
B.
C.c(H+)和c( OH-)的乘积
D.OH-的物质的量
参考答案:A
本题解析:A.加水稀释促进酸电离,氢离子浓度、酸浓度、酸根离子浓度都降低,但氢离子浓度减小的量小于酸分子减小的量,所以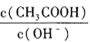 减小,故A正确;
减小,故A正确;
B.加水稀释促进酸电离,酸浓度、酸根离子浓度都降低,但酸根离子浓度减小的量小于酸分子减小的量,所以氢氧根离子浓度增大,则 增大,故B错误;
增大,故B错误;
C.温度不变,水的离子积常数不变,故C错误;
D.加水稀释促进酸电离,氢离子浓度降低,但氢氧根离子浓度增大,故D错误;
故选A。
点评:本题考查了弱电解质的电离,易错题,注意加水稀释时溶液中各种微粒浓度的变化,虽然促进弱电解质电离,但加入水的量远远大于弱电解质电离的量,为易错点。
本题难度:一般
5、选择题 A、B两种酸溶液的pH都是2,各取1mL分别加水稀释成1000 mL,其pH的变化如图所示,则下列判断正确的是
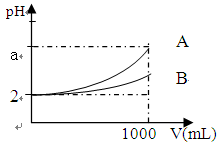
A.原酸溶液的浓度c(A)=c(B)
B.原酸溶液的浓度c(A)>c(B)
C.若a=5,则A为强酸,B为弱酸
D.若2<a<5,则A、B都是弱酸,酸性A<B
参考答案:C
本题解析:根据图像可知,在稀释过程中,B溶液的pH变化程度小于A溶液中pH的变化程度,这说明在稀释过程中B中一定存在电离平衡,可以继续电离出氢离子,所以B酸的酸性弱于A酸的酸性,A、B、D选项均是错误的,选项C正确,答案选C。
点评:该题是中等难度的试题,试题综合性强,难易适中,有利于培养学生的逻辑推理能力和抽象思维能力,特别是灵活运用基础知识解决实际问题的能力。该题关键是明确弱电解质电离平衡的特点,以及外界条件是如何影响电离平衡的。
本题难度:一般