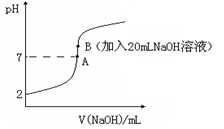
1、填空题 (14分)氢氟酸(HF)是一元弱酸,在水溶液中的电离方程式为:HF H++F-。25℃下,向20mL0.2mol?L-1的氢氟酸中滴加0.2mol?L-1的NaOH溶液时,溶液的pH变化如图所示。
H++F-。25℃下,向20mL0.2mol?L-1的氢氟酸中滴加0.2mol?L-1的NaOH溶液时,溶液的pH变化如图所示。
已知:电离度(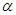 )和电离平衡常数(K)一样,可以用来衡量弱电解质在稀溶液中的电离能力,
)和电离平衡常数(K)一样,可以用来衡量弱电解质在稀溶液中的电离能力, 。
。
请回答下列问题:
(1)在氢氟酸的稀溶液中,通过改变以下条件能使氢氟酸的电离度[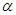 (HF)]增大的是_______,可使氢氟酸的电离平衡常数[Ka(HF)] 增大的是_______。
(HF)]增大的是_______,可使氢氟酸的电离平衡常数[Ka(HF)] 增大的是_______。
a.升高温度? b.向溶液中滴入2滴浓盐酸? c.加入少量NaF固体? d.加水稀释
(2)在此温度下,氢氟酸的电离平衡常数Ka(HF)为:__??(保留两位有效数字),电离度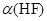 约为___?_%。
约为___?_%。
(3)已知在此温度下:
H+(aq)+OH-(aq)=H2O(1)? △H=-a kJ?mol -1;
?HF(aq)  ?H+(aq)+F-(aq)? △H=+b kJ?mol -1
?H+(aq)+F-(aq)? △H=+b kJ?mol -1
则该过程中和反应的热化学方程式为:________________________________??;在忽略F-水解的情况下,反应达到B点时,滴加过程中所释放的热量为________kJ(用只含a、b的式子表示)。
(4)下列有关图中各点微粒浓度关系正确的是_______________。
a.在A处溶液中:c(F―)+c(HF)="0.2" mol?L-1?
b.在B处溶液中:c(H+)+c(HF)= c(OH―)
c.在B处溶液中:c(Na+)>c(F―)>c(H+)>c(OH―)?
d.在A和B处溶液中都符合: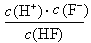 = Ka(HF)
= Ka(HF)
2、选择题 在相同温度时,100mL0.01mol/L的醋酸溶液与10mL 0.1mol/L的醋酸溶液相比较,下列数值中,前者大于后者的是
[? ]
A.H+的物质的量
B.醋酸的电离常数
C.中和时所需NaOH的量
D.CH3COOH的物质的量
3、选择题 强弱电解质的本质区别是 ( )
A.导电能力
B.相对分子质量
C.电离程度
D.溶解度