1������� ʵ����498mL0.200mol/L��CuSO4��Һ��ʵ�����õ�������������Һ������д���пհף�
��1�����ȡ��������______g��
��2����ʵ���õ��Ļ������������ձ�����ƽ�����롢���ӣ���ҩ�ף���ȱ�ٵ�������______��______��______��
��3�����������ʹ������ҺŨ��ƫ�͵��ǣ�����ţ�______��
a������ʱ����b��δϴ���ձ�
c��������ˮʱ�����������˿̶���
d������ʱ��Ʒ������λ�÷ŷ���1g���������룩
e���������ij�16.0g��ˮCuSO4���ƣ�
�ο��𰸣���1��ʵ����498mL 0.200mol/L��CuSO4��Һ��ʵ����û��498mL����ƿ��Ӧ��ѡ��500mL����ƿ��ʵ�����Ƶ���500mL 0.200mol/L��CuSO4��Һ����Ҫ����ͭ�����ʵ���Ϊ��0.200mol/L��0.5L=0.1mol����Ҫ����ͭ���������Ϊ��250g/mol��0.1mol=25.0g��
�ʴ�Ϊ��25.0g��
��2�����Ƶ���500mL 0.200mol/L��CuSO4��Һ��һ������ƽ��������ҩ��ȡҩƷ�����ձ����ܽ⣬�ò��������裬��ȴ��ת�Ƶ�500mL����ƿ�У����ò�����������ת����ϣ�����������ˮϴ���ձ���������2��3�β���ϴ��Һȫ��ת�Ƶ�����ƿ�У��ټ���������ˮ������ˮ��Һ�����̶���1��2cmʱ�����ý�ͷ�ιܵμӣ�ʹ��Һ�İ�Һ�����͵��������ƽ������ƿ�����������µߵ�ҡ�ȣ�������Ҫ������Ϊ����ƽ��ҩ�ס���ͷ�ιܡ��ձ�����������500mL����ƿ�����Ի�ȱ�ٵ�����Ϊ��500mL����ƿ������������ͷ�ιܣ�
�ʴ�Ϊ��500mL����ƿ������������ͷ�ιܣ�
��3��a������ʱ���ӣ����¼��������ˮ���ƫС������c=nV�ɵã����Ƶ���ҺŨ��ƫ�ߣ���a����
b��δϴ���ձ����������Ƶ���Һ�����ʵ����ʵ���ƫС������c=nV�ɵã����Ƶ���ҺŨ��ƫ�ͣ���b��ȷ��
c��������ˮʱ�����������˿̶��ߣ��������Ƶ���Һ���ƫ����c=nV�ɵã����Ƶ���ҺŨ��ƫ�ͣ���c��ȷ��
d������ʱ��Ʒ������λ�÷ŷ���1g���������룩�����³��������ʵ�����ƫС�����Ƶ���Һ�����ʵ����ʵ���ƫС������c=nV�ɵã����Ƶ���ҺŨ��ƫС����d��ȷ��
e���������ij�16.0g��ˮCuSO4���ƣ����ʵ����ʵ������䣬����c=nV�ɵã����Ƶ���ҺŨ�Ȳ��䣬��e����
��ѡbcd��
���������
�����Ѷȣ�һ��
2��ѡ���� ��NAΪ�����ӵ�������ֵ������˵����ȷ����
A�����³�ѹ�£�14 g ��N2��CO��ɵĻ�����庬�е�ԭ����ĿΪNA
B��78 g ������C="C" ˫������ĿΪ3NA
C��1 L 1 mol��L-1��NaClO ��Һ�к���ClO������ĿΪNA
D����״���£�6.72 L NO2��ˮ��ַ�Ӧת�Ƶĵ�����ĿΪ0.1NA
�ο��𰸣�A
���������A����ȷ�����³�ѹ�£�14 g ��N2��CO��ɵĻ�����庬�е�ԭ����ĿΪ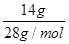 ��2NA=NA
��2NA=NA
B������ȷ����������C="C" ˫����C������ȷ��1 L 1 mol��L-1��NaClO ��Һ��ClO�DҪˮ�⣬����ClO����������NAD������ȷ��3NO2��H2O=2HNO3��NO,��״���£�6.72 L NO2��ˮ��ַ�Ӧת�Ƶĵ�����ĿΪ0.2NA��ѡA��
�����Ѷȣ�һ��
3��ѡ���� ��NA�ǰ����ӵ���������ֵ������˵������ȷ���ǡ�
A��1 mol Al3�����еĺ��������Ϊ3NA
B��1 mol Cl2������������Ӧ��ת�Ƶĵ�����Ϊ3NA
C��10 L pH��1��������Һ�к��е�H����Ϊ2NA
D��10 L pH��13��NaOH��Һ�к��е�OH����ΪNA