1、选择题 人们把能对抗外来少量酸、碱或稍加稀释而引起溶液pH发生明显变化的作用叫做缓冲作用,具有缓冲作用的溶液叫缓冲溶液.缓冲溶液往往由弱酸与其对应的盐、多元弱酸与其对应的次级盐、弱减与其对应的盐组成.下列各组溶液不能形成缓冲溶液的是
A.CH3COOH与CH3COONa形成的溶液
B.NaHCO3与Na2CO3形成的溶液
C.Na2SO4与H2SO4形成的溶液
D.NH3・H2O与NH4Cl形成的溶液
参考答案:C
本题解析:
本题难度:一般
2、填空题 (6分)下列盐溶液能发生水解的用离子方程式表示,不能发生水解的写“不发生水解”字样,并说明溶液的酸碱性
K 2CO3 , 溶液呈 性;
Na2SO4 , 溶液呈 性;
CuCl2 , 溶液呈 性。
参考答案:CO32-+H2O=HCO3-+OH-,碱; 不发生水解,中; Cu2++2H2O=Cu(OH)2+2H+,酸
本题解析:
试题解析:K2CO3是强碱弱酸盐,水解后水溶液都呈碱性,水解离子方程式为 CO32-+H2O=HCO3-+OH-;Na2SO4是强酸强碱盐,不水解,溶液呈中性;CuCl2是强酸弱碱盐,水解后溶液呈酸性,水解离子方程式为:Cu2++2H2O=Cu(OH)2+2H+.
考点:盐类水解的规律
本题难度:一般
3、填空题 硫元素的含氧酸盐在工业上用途广泛,完成下列填空。
工业上用Na2SO3溶液处理工业尾气中的SO2,下表数据表示反应过程中 随pH变化的关系:
随pH变化的关系:

| 91:9
| 1:1
| 9:91
|
室温下pH
| 8.2
| 7.2
| 6.2
|
(1)简述 = 1时,溶液pH= 7.2的原因:___________________;若用0.20 mol/L 的NaOH溶液(反应前后溶液体积不变)吸收SO2,若反应后溶液呈中性,则
= 1时,溶液pH= 7.2的原因:___________________;若用0.20 mol/L 的NaOH溶液(反应前后溶液体积不变)吸收SO2,若反应后溶液呈中性,则
c (HSO3-) + 2c (SO32-) =" _______" mol/L 。
(2)已知:Ki1(H2SO3)> Ki(HAc) > Ki2(H2SO3) > Ki2(H2CO3),要使NaHSO3溶液中c(Na+):c(HSO3-)接近1:1,可在溶液中加入少量____________。
a.H2SO3溶液 b.NaOH溶液 c.冰醋酸 d.Na2CO3
(3)实验室通过低温电解KHSO4溶液制备过二硫酸钾K2S2O8,写出熔融KHSO4的电离方程式:__________________________________________。
(4)S2O82-有强氧化性,还原产物为SO42-,硫酸锰(MnSO4)和过硫酸钾(K2S2O8)两种盐溶液在银离子催化下可发生反应,得到紫红色溶液。书写此反应的化学方程式: 。
(5)已知:S2O32-有较强的还原性,实验室可用I-测定K2S2O8样品的纯度:反应方程式为:
S2O82-+2I-→2SO42-+I2 ……① I2+2S2O32-→2I-+S4O62-……②
S2O82-、S4O62-、I2氧化性强弱顺序:__________________________。
(6)K2S2O8是偏氟乙烯(CH2=CF2)聚合的引发剂,偏氟乙烯由CH3―CClF2气体脱去HCl制得,生成0.5 mol偏氟乙烯气体要吸收54 kJ的热,写出反应的热化学方程式_______。
参考答案:(1)HSO3-的电离程度与SO32-的水解程度相近(1分) 0.2 mol/L(2分)
(2)a c(2分)
(3)KHSO4 →K+ + HSO4- (1分)
(4)5K2S2O8 + 2MnSO4 + 8H2O→ 4K2SO4 + 2KMnO4 + 8H2SO4(2分)
(5)S2O82- > I2 > S4O62- (2分)
(6)CH3―CClF2(g) → CH2=CF2(g) + HCl(g)
本题解析:
本题难度:一般
4、选择题 在一定条件下发生下列反应,其中属于盐类水解反应的是
[? ]
A.NH4++2H2O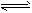 NH3・H2O+H3O+
NH3・H2O+H3O+
B.HCO3-+ H2O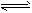 H3O+ + CO32-
H3O+ + CO32-
C.HS-+H+=== H2S
D.Cl2+H2O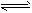 H++Cl-+HClO
H++Cl-+HClO
参考答案:A
本题解析:
本题难度:简单
5、选择题 香草醛是一种食品添加剂,可由愈创木酚作原料合成,合成路线如下:

下列说法正确的是( )
A.反应1→2属于加成反应,且生成的化合物2具有一个手性碳原子
B.化合物2在一定条件下可发生消去反应
C.检验制得的香草醛中是否混有化合物3,可用氯化铁溶液
D.等物质的量四种化合物分别与足量NaOH反应,消耗NaOH物质的量之比1:3:2:4
参考答案:A.反应1

2中,反应物全部转化为生成物,为加成反应,2中
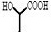
连接-OH的C原子连接4个不同的原子或原子团,为手性碳原子,故A正确;
B.醇羟基邻位C原子上没有H原子,不能发生消去反应,而酚羟基邻位上的H为苯环上的H原子,结构稳定,C-H键不易断裂,不能发生消去反应,故B错误;
C.香草醛和化合物3中都含有酚羟基,加入氯化铁溶液都呈紫色,不能鉴别,故C错误;
D.物质的量分别为1mol的四种化合物分别与足量NaOH反应,1消耗NaOH1mol,2消耗NaOH2mol,3消耗NaOH2mol,4消耗NaOH1mol,消耗NaOH物质的量之比为1:2:2:1,故D错误.
故选A.
本题解析:
本题难度:简单