|
|
|
高考化学必考知识点《盐类水解的原理》典型例题(九)
2019-07-04 02:04:08
【 大 中 小】
|
1、选择题 下列各溶液中CH3COO-的数量关系,正确的是
①0.1 mol・L-1 CH3COOH溶液25 mL
②0.05 mol・L-1 CH3COOH溶液50 mL
③0.1 mol・L-1 CH3COONa溶液25 mL
④0.05 mol・L-1 CH3COONa溶液50 mL
A.①<②<③<④
B.①<②<④<③
C.④<③<②<①
D.③<④<①<②
2、选择题 将物质的量浓度都是0.1mol/L的某弱酸HX溶液与NaX溶液等体积混合,下列说法错误的是( )
A.若混合后溶液中c(Na+)
|
3、选择题 现有a?mol/L?NaX和b?mol/L?NaY两种盐溶液.下列说法不正确的是(若是溶液混合,则忽略混合时的体积变化)( ? )
A.若a=b且pH(NaX)>pH(NaY),则酸性HX>HY
B.若a=b且c(X-)=c(Y-)+c(HY),则酸性HX>HY
C.若a>b且c(X-)=c(Y-),则酸性HX<HY
D.若a=0.1mol/L且两溶液等体积混合,则c(X-)+c(HX)=0.1mol/L
4、选择题 化学用语是学习化学的重要工具,下列化学用语中正确的是
A.Na2S的水解:S2-+ 2H2O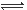 H2S + 2OH- H2S + 2OH-
B.NaHCO3的电离:NaHCO3 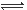 Na + + H+ + CO32- Na + + H+ + CO32-
C.HSO3-的电离:HSO3- 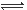 H+ + SO32- H+ + SO32-
D.钢铁的电化学腐蚀的负极反应式:Fe-3e-Fe3+
|
5、填空题 回答下列问题:
(1)有一种溶液除H+、OH-外,还有Na+、SO42-和Cl-,测得三种离子的浓度分别是0.01 mol・L-1、0.0035 mol・L-1和 0.004 mol・L-1,该溶液的pH为______________ 。
(2) NH4Cl溶液显酸性,试用离子方程式表示这一反应_________________ 。
(3)液氨类似于水的电离,试写出液氨的电离方程式___________________;在液氨中加入NH4Cl,则平衡将向__________移动。
(4)pH相同的氨水和氢氧化钠溶液,分别用蒸馏水稀释至原来体积的m倍和n倍,稀释后两溶液的pH仍相同,则m____n(选填“>”“<”或“=”);若改用pH相同的盐酸和硫酸溶液,进行上述操作,则m________n(选填“>” “<”或“=”)。