1、填空题 (4分)(1)原电池是一种把 转化为 的装置。
(2)铜-锌-稀硫酸电池中,负极的电极反应式是 。
2、选择题 电子表所用电池的电极材料为Zn与Ag2O,电解质溶液为KOH溶液,电极反应为:Zn+2OH--2e-=Zn(OH)2;? Ag2O+H2O+2e-=2Ag+2OH-
总反应为:Zn+Ag2O+H2O=2Ag+Zn(OH)2,下列判断正确的是
A.锌为正极,氧化银为负极
B.锌发生氧化反应,氧化银发生还原反应
C.使用过程中,电流由Zn沿导线流向Ag2O
D.工作时,正极区的pH变小
3、选择题 燃料电池的基本组成为电极、电解质、燃料和氧化剂。此种电池的能量利用率可高达80%,产物污染也少。下列有关燃料电池说法错误的是(?)
A.氨气燃料电池的电解质常用KOH溶液,其负极电极反应为:2NH3-6e-+6OH-=N2+6H2O
B.碱性甲烷燃料电池的正极反应为:O2+2H2O+4e-=4OH-
C.燃料电池负极燃料失电子,发生还原反应
D.除纯氧外,空气中的氧气也可以作氧化剂
4、选择题 下列烧杯中盛放的都是稀硫酸,在铜电极上能产生大量气泡的是(? )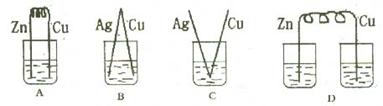
5、填空题 原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献.
(1)现有如下两个反应:A.NaOH+HCl=NaCl+H2O,B.Zn+H2SO4=ZnSO4+H2↑判断能否设计成原电池A.______B.______.(填“能”或“不能”)
(2)由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生原电池腐蚀,一段时间后某电极产生3.36L标准状况下的气体.
①负极是______(填“锌”或“铜”),发生______反应(填“氧化”或“还原”);
②正极的电极反应式为______;
③产生这些气体共需转移电子______mol.