1��ѡ���� ͨ��һ���εĸ�ϰ������Ϊ����˵����ȷ����
A����������ԭ��Ӧ�У�һ��Ԫ�ر�������ͬʱһ������һ��Ԫ�ر���ԭ
B����ԭ���װ���У�һ��Ҫ�����������Բ�ͬ�Ľ�����Ϊ�缫����
C���ڻ������У����ǵ���ʾ��Ƿǵ����
D�����ڿ��淴Ӧ���¶�������÷�Ӧ��ƽ�ⳣ��һ������
�ο��𰸣�C
���������A����������ԭ��Ӧ����һ��Ԫ�ؼ��������ֱ���ԭ������B��ȼ�ϵ���в���Ҫ����Ҫ�������Ե缫������C���������Ϊ����ʺͷǵ���ʣ���ȷ��D���¶����ߣ�ƽ�������ȷ����ƶ���ƽ�ⳣ����������Ҳ���ܼ�С������
�����Ѷȣ�һ��
2��ѡ���� �ճ����øɵ�صĵ缫�ֱ�Ϊ̼����пƤ���Ժ�״NH4Cl��ZnCl2������ʣ����м���MnO2��������H2�����缫��Ӧ�ɼ�Ϊ��Zn-2e-=Zn2+��2NH4++2e-=2NH3+H2��NH3�����ڽ��Zn2+�����������������ж�����˵������ȷ���ǣ�������
A���ɵ����ZnΪ������̼Ϊ����
B���ɵ�ع���ʱ��������Zn�������·����̼��
C���ɵ�س�ʱ������ʹ��ʱ��װ��״�����������ʴ����
D���ɵ�ؿ���ʵ�ֻ�ѧ������ܵ�ת���͵�����ѧ�ܵ�ת��
�ο��𰸣�A���ɵ���нϻ��õĽ���п���������ϲ����õĵ���ķǽ���̼����������A����
B���ɵ�ع���ʱ������������̼�����·����п����B����
C��NH4Cl��ZnCl2����ǿ��������ˮ������ԣ����Ըɵ�س�ʱ������ʹ��ʱ��װ��״�����������ʴ��������C��ȷ��
D���ɵ����һ�ε�أ����Բ���ʵ�ֵ�����ѧ�ܵ�ת������D����
��ѡC��
���������
�����Ѷȣ���
3��ѡ���� ����˵����ȷ���ǣ�������
A����ԭ��ع���ʱ����Һ�е����������ƶ�
B���ö��Ե缫���ij��Һ���������ֱ�ֻ��H2��O2���ɣ����һ��ʱ�����Һ��Ũ�ȿ��ܼ�С
C��Ҫʹ�����CuSO4��Һ��ԭ���������м���Cu��OH��2����
D�������������ֱ����Դ�ĸ������������������ӵ������ϣ����Է�ֹ��������ʴ
�ο��𰸣�ԭ��ع���ʱ����Һ���������������ƶ������������ƶ�����A����
B���ö��Ե缫���ij��Һ���������ֱ�ֻ��H2��O2���ɣ�ʵ���ϵ�����ˮ���ܼ����������٣����Ե��һ��ʱ�����Һ��Ũ������B����
C���������ͭ��Һʱ����������������������������ͭ��Ҫ��ʹ��Һ��ԭӦ��������ͭ����C����
D�������������ֱ����Դ�ĸ������������������ӵ������ϣ������������������������������Կ��Է�ֹ��������ʴ����D��ȷ��
��ѡD��
���������
�����Ѷȣ���
4��ѡ���� �~���ؿ�����Ϊ���������ṩ��Դ�����ط�Ӧ�ɼ�Ϊ��2Li + I2?= 2LiI�������й�˵����ȷ����
A��I2����������Ӧ
B����缫Ϊ�õ�ص�����
C��������ӦΪ��Li �C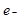 = Li+
= Li+
D���õ�طŵ�ʱ��ѧ��ת��Ϊ����
�ο��𰸣�BD
������������ܷ�Ӧʽ��֪�����ϼ����ߵ�����������������������������������Եⷢ�����ǻ�ԭ��Ӧ��ԭ����ǽ���ѧ��ת��Ϊ���ܵ�װ�ã����Դ�ѡBD
�����Ѷȣ�һ��
5��ѡ���� X��Y��Z��M�������ֽ���Ԫ�ء�����X��Z�õ������ӷ���ϡ������ʱ,X�ܽ�,Z�����������ų��������Y2+��Z2+���ӹ������Һʱ,Y����������֪M2+���ӵ�������ǿ��Y2+���ӡ��������ֽ����Ļ����ǿ������˳��Ϊ
A��M>Z>X>Y
B��X>Y>Z>M
C��X>Z>Y>M
D��X>Z>M>Y
�ο��𰸣�C
�������������X��Z�õ������ӷ���ϡ������ʱ,X�ܽ�,Z�����������ų����������X>Z�������Y2+��Z2+���ӹ������Һʱ,Y���������������Z>Y��M2+���ӵ�������ǿ��Y2+���ӣ��������Y>M��������X>Z>Y>M��C��ȷ��
�����Ѷȣ�һ��