1、选择题 下列关于电解的叙述中,正确的是( )
①电解是把电能转变成化学能?
②电解是把化学能转变成电能
③电解质溶液导电是化学变化,金属导电是物理变化
④不能自发进行的氧化还原反应,通过电解可以实现
⑤任何水溶液电解时,必将导致氧化还原反应.
A.②③④
B.①②③④
C.①②④
D.①③④⑤
参考答案:①电解时通电条件下发生化学反应,阳极发生氧化反应,阴极发生还原反应,电能转变成化学能,故①正确;
②电解时通电条件下发生化学反应,阳极发生氧化反应,阴极发生还原反应,电能转变成化学能,故②正确;
③电解质溶液导电是阴阳离子在两个电极发生的氧化还原反应,金属导电是电子的定向移动是物理变化,故③正确;
④不能自发进行的氧化还原反应,依据离子放电顺序设计成电解池,通过电解可以实现,故④正确;
⑤电解的实质是发生氧化还原反应,任何水溶液电解时多会发生氧化还原反应.故⑤正确;
综上所述:①③④⑤正确;
故选D.
本题解析:
本题难度:简单
2、选择题 将0.2 mol AgNO3、0.4 mol Cu(NO3)2、0.6 mol KCl溶于水,配成100 mL溶液,用石墨电极电解一段时间后,若在一极析出0.3 mol Cu,试计算另一极上产生的气体体积(标准状况)。
参考答案:5.6 L
本题解析:三种物质溶于水时,AgNO3与KCl反应后溶液中含有0.2 mol KNO3、0.4 mol Cu(NO3)2和0.4 mol KCl。当有0.3 mol Cu生成时,先后发生反应:
Cu2++2Cl- Cu+Cl2↑①
Cu+Cl2↑①
2Cu2++2H2O 2Cu+O2↑+4H+②
2Cu+O2↑+4H+②
在阳极上先后生成Cl2和O2。n(Cl2)=1/2n(KCl)=(1/2)×0.4 mol=0.2 mol,根据电子守恒有:0.3 mol×2=0.2 mol×2+4n(O2),解得n(O2)=0.05 mol,所以阳极共产生气体体积为:(0.2 mol+0.05 mol )×22.4 L・mol-1=5.6 L。
本题难度:一般
3、填空题 近期因“召回门”而闹的沸沸扬扬的丰田Prius属第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮。汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态。
(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,每生成1 mol水蒸气放热569.1 kJ。则该反应的热化学方程式为__________________。
(2)混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解液。镍氢电池充放电原理示意如图,
其总反应式是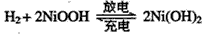
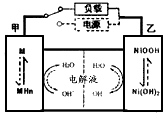
根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH将___________(填“增大”、“不变”或“减小”),该电极的电极反应式为___________________________。
(3)汽车尾气中的一氧化碳是大气污染物,可通过如下反应降低其浓度:
CO(g)+1/2O2(g) CO2(g)。
CO2(g)。
①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如下表所示。请填写表中的空格。
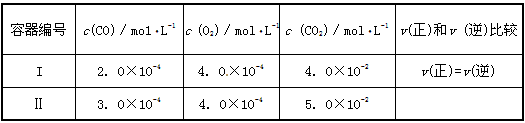
②相同温度下,某汽车尾气中CO、CO2的浓度分别为1.0×10-5mol・L-1和1.0×10-4mol・L-1。若在汽车的排气管上增加一个补燃器,不断补充O2并使其浓度保持为1.0×10-4mol・L-1,则最终尾气中CO的浓度为
_________mol・L-1。
参考答案:(1)C8H18(l)+25/2O2(g) =8CO2(g)+9H2O(g) △H=-5121.9 kJ・mol-1
(2)增大;NiOOH+H2O+e-=Ni(OH)2+OH-
(3)①v(正)>v(逆);②1.1×10-6
本题解析:
本题难度:困难
4、选择题 关于下列图示的说法中正确的是?(?)
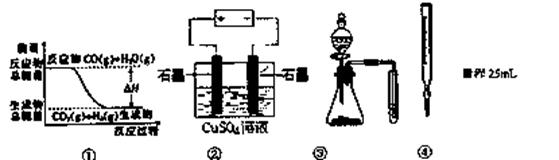

A.图①表示可逆反应“CO(g)+H2O(g) CO2(g)+H2(g)”中的△H大于0
B.图②为电解硫酸铜溶液的装置,一定时间内两电极产生单质的物质的量之比一定为1:1
C.图③实验装置可完成比较乙酸、碳酸、苯酚酸性强弱的实验
D.图④量取0.10 mol・L-1KMnO4溶液20.00mL
参考答案:C
本题解析:略
本题难度:一般
5、选择题 下图装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,下列说法中正确的是
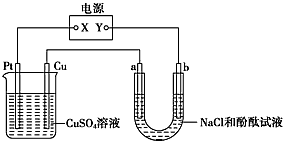
[? ]
A.X是正极,Y是负极
B.X是负极,Y是正极
C.CuSO4溶液的pH值逐渐增大
D.CuSO4溶液的pH值保持不变
参考答案:A
本题解析:
本题难度:一般