1������� I�����ܵĴ洢������Ӧ�õ���Ҫƿ������λ�⻯��������廯������Ŀǰ�����õ���Ҫ������ϡ�
��1��Ti��BH4��2��һ�ֹ���Ԫ�����⻯�ﴢ����ϡ��ڻ�̬Ti2+�У�����ռ�ݵ�����ܲ����Ϊ?�����ܲ���е�ԭ�ӹ����Ϊ?��
��2��Һ���Ǹ������ʣ������ܵ��������壬���� ʵ�ִ�������⡣����˵����ȷ����?��
ʵ�ִ�������⡣����˵����ȷ����?��
a��NH3�����е�ԭ�ӵĹ���ӻ���ʽΪsp2�ӻ�
b��NH+4��PH+4��CH4��BH-4��ClO��4��Ϊ�ȵ�����
c����ͬѹǿʱ��NH3�ķе��PH3�ķе��
d��[Cu��NH3��4]2+�����У�Nԭ������λԭ��
��3����֪NF3��NH3�Ŀռ乹����ͬ����NF3������Cu2+�γ������ӣ���ԭ����?��
II���Ȼ����������еij��õ�ζƷ��Ҳ�ǽṹ��ѧ���о����Ӿ���ʱ���õĴ�����侧���ṹ��ͼ��ʾ��

��1�����Ȼ��ƾ�����Na+���������ڵ�Cl��֮��ľ���Ϊr�����Na+������ν��ڵ�C1������Ϊ?����Na+������ν��ڵ�Cl��֮��ľ���Ϊ?��
��2����֪���Ȼ��ƾ�����Na+�İ뾶Ϊ��a pm��Cl���İ뾶Ϊb pm�������ھ�
�����ǽ��ܽӴ��ģ������Ȼ��ƾ��������ӵĿռ�������Ϊ?�����ú�a��b��ʽ��Ԭʾ��
��3�����ײ��ϵı���ԭ��ռ��ԭ�����ı����ܴ��������������������ʵ�ԭ����ij�Ȼ��ƿ�����״Ϊ�����壬�߳�Ϊ�Ȼ��ƾ�����10��������Ȼ��ƿ����б���ԭ��ռ��ԭ�����İٷֱ�Ϊ?��
�ο��𰸣���1��M��1�֣�? 9��2�֣�?
��2��cd��2�֣�?
��3��N��F��H����Ԫ�صĵ縺��ΪF > N >H����NF3�У����õ��Ӷ�ƫ��F��ƫ��Nԭ�ӣ�ʹ�õ�ԭ���ϵŵ��Ӷ�������Cu2���γ���λ����2�֣�
��1��8��2�֣�?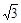 r��2�֣�?
r��2�֣�?
��2�� ��2�֣�?
��2�֣�?
��3��26�� ��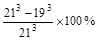 ��2�֣�
��2�֣�
�����������1��Tiԭ�Ӻ�����22�����ӣ����̬ԭ�ӵĺ�������Ų�ʽΪ1s22s22p63s23p63d24s2���ڻ�̬Ti2+�У���������Ų�ʽΪ1s22s22p63s23p63d2����Ӧ�ܲ�ֱ��ΪK��L��M������������ߵ��������M�㣬���ܲ���s��p��d�����ܼ���s�ܼ���1�������p�ܼ���3�������d�ܼ���5����������Թ���9��ԭ�ӹ����
��2��a��NH3������Nԭ�Ӻ���3�����õ��ӶԺ�һ���µ��Ӷԣ�������۲���Ӷ���4������sp3�ӻ����ʴ���
b���ȵ�������ָ������ͬ������Ŀ��ԭ����Ŀ�ķ��ӻ����ӣ�NH4+��PH4+��CH4��BH4-��ClO4��ԭ����Ŀ��ͬ��������Ŀ��ͬ�����Բ��ܻ�Ϊ�ȵ����壬�ʴ���
c����ͬѹǿʱ�������к��������PH3�в������������NH3�е��PH3�ߣ�����ȷ��
d����[Cu��NH3��4]2+�����У�Nԭ���ṩ�µ��Ӷԣ�����Nԭ������λԭ�ӣ�����ȷ��
����ѡcd ��?
��3��N��F��H����Ԫ�صĵ縺�ԣ�F��N��H������NH3�й��õ��Ӷ�ƫ��N������NF3�У����õ��Ӷ�ƫ��F��ƫ��Nԭ�ӣ��ʴ�Ϊ��F�ĵ縺�Ա�N��N-F�ɼ����Ӷ���Fƫ�ƣ�����NF3��Nԭ�Ӻ˶���¶Ե��ӵ�����������ǿ�������γ���λ������NF3������Cu2+�γ������ӣ�����N��F��H����Ԫ�صĵ縺�ԣ�F��N��H����NF3�У����õ��Ӷ�ƫ��F��ƫ��Nԭ��ʹ�õ�ԭ���ϵŶԵ���������Cu2+�γ���λ��������
��1���Ȼ��ƾ����У�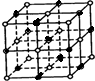 ����ͼ�п��Կ����������������ĺ�����λ�ã��������ڶ��������λ�ã�Na+������ν��ڵ�C1����Ҳ����ͼ�о������������е�8������С��Ȧ ������Ϊ8������Na+������ν��ڵ�Cl��֮��ľ���Ҳ���DZ߳�Ϊr��С���������Խ��ߣ�Ҳ����
����ͼ�п��Կ����������������ĺ�����λ�ã��������ڶ��������λ�ã�Na+������ν��ڵ�C1����Ҳ����ͼ�о������������е�8������С��Ȧ ������Ϊ8������Na+������ν��ڵ�Cl��֮��ľ���Ҳ���DZ߳�Ϊr��С���������Խ��ߣ�Ҳ����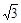 r ��
r ��
��2������Ϊ����������һ���Ȼ��ƾ�������4��Na����Cl�������������ı߳���2(a��b)pm�������8(a��b)3pm3��һ��Na�������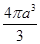 pm3��һ��Cl�������
pm3��һ��Cl������� pm3��4��Na����Cl�������
pm3��4��Na����Cl������� pm3���Ȼ��ƾ��������ӵĿռ�������Ϊ
pm3���Ȼ��ƾ��������ӵĿռ�������Ϊ ��100%��
��100%�� ��
��
��3����NaCl�ľ���ͼ��֪��NaCl�ľ���Ϊ��������ṹ�������������ֻ��һ��Na���������������Ӷ���������������ϣ��߳�Ϊ�Ȼ��ƾ����߳���10�����Ȼ��ƿ�������ԭ����Ϊ21�������������ڲ�����ԭ����Ϊ19����������������Ե��������ϸ�����ȥ��һ��ԭ�ӣ����������߳��൱���Ǽ�����2��������19�������Ը��Ȼ��ƿ����б���ԭ��ռ��ԭ�����İٷֱ�Ϊ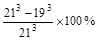 ��26����������һ�ֱȽ�ֱ�����˵Ľⷨ�� �����������е���ԭ����Ϊn3��nΪ����ԭ������ ��˱߳�Ϊ�Ȼ��ƾ����߳���10�����Ȼ��ƿ�������ԭ����Ϊ213�������ڲ�����ԭ����Ϊ193���൱�ڽ��������һ�㣩������������ԭ����Ϊ213-193������ԭ��ռ��ԭ�����İٷ�����
��26����������һ�ֱȽ�ֱ�����˵Ľⷨ�� �����������е���ԭ����Ϊn3��nΪ����ԭ������ ��˱߳�Ϊ�Ȼ��ƾ����߳���10�����Ȼ��ƿ�������ԭ����Ϊ213�������ڲ�����ԭ����Ϊ193���൱�ڽ��������һ�㣩������������ԭ����Ϊ213-193������ԭ��ռ��ԭ�����İٷ�����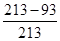 =26%��
=26%��
�����Ѷȣ�һ��
2��ѡ���� A��B��C��D���Ƕ�����Ԫ�أ�ԭ�Ӱ뾶��D��C��A��B����֪A��Bͬ���ڣ�A��Cͬ���壬Cԭ�Ӻ��ڵ�����������A��Bԭ�Ӻ��ڵ�������֮�ͣ�Cԭ��������������Dԭ��������������3��������˵������ȷ���ǣ�������
A��B��C��D����Ԫ����ɵĻ�����Ļ�ѧʽΪD2CB2
B��A��C��Ԫ�ش���Ԫ�����ڱ��еĵڢ�A��
C��B��C��D����Ԫ�صļ����ӵİ뾶��С˳��Ϊ��C��D��B
D��B��D��Ԫ�ؿ��γ��������ӻ������������������֮�Ⱦ�Ϊ1��2
�ο��𰸣�A��B��C��D���Ƕ�����Ԫ�أ�����ԭ�Ӱ뾶D��C��A��B����A��Bͬ���ڣ�A��Cͬ���壬��֪A��B��C��D�����ڱ��еĴ������λ��Ϊ��
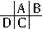
��Cԭ����������Aԭ������+8��Cԭ�Ӻ��ڵ�����������A��Bԭ�Ӻ��ڵ�������֮�ͣ���Bԭ������Ϊ8����BΪ��Ԫ�أ�
Cԭ��������������Dԭ��������������3������D������������Ϊ1����CΪ��Ԫ�أ�AΪ��Ԫ�أ�DΪ��Ԫ�أ���D������������Ϊ2����CΪ��Ԫ�أ�AΪ��Ԫ�أ��������⣮
����AΪ��Ԫ�أ�BΪ��Ԫ�أ�CΪ��Ԫ�أ�DΪ��Ԫ�أ�
A��BΪ��Ԫ�أ�CΪ��Ԫ�أ�DΪ��Ԫ�أ�B��C��D����Ԫ����ɵĻ�����Ļ�ѧʽΪNaAlO2����A����
B��AΪ��Ԫ�أ�CΪ��Ԫ�أ�������������Ϊ3����Ԫ�ش���Ԫ�����ڱ��еĵڢ�A�壬��B����
C��B��C��D����Ԫ�صļ����ӷֱ�ΪO2-��Al3+��Na+���������Ӻ�������Ų���ͬ���˵����Խ�����Ӱ뾶ԽС������O2-��Na+��Al3+����C����
D��BΪ��Ԫ�أ�DΪ��Ԫ�أ�B��D��Ԫ����ɵ����ӻ�����Na2O��Na2O2�����������ӵĸ����ȶ�Ϊ1��2����D��ȷ��
��ѡD��
���������
�����Ѷȣ���
3��ѡ���� ��֪H-Cl���ļ���Ϊ431.4kJ/mol�����й��ڼ��ܵ�������ȷ���ǣ�������
A��ÿ����2molH-Cl���ų�431.4kJ����
B��ÿ����1molH-Cl������431.4kJ����
C��ÿ����1molH-Cl���ų�431.4kJ����
D��ÿ����1molH-Cl������431.4kJ����
�ο��𰸣���֪H-Cl���ļ���Ϊ431.4kJ/mol������Ҫ��1 molH-Cl����Ҫ����431.4kJ������Ҫ�γ�1 molH-Cl����Ҫ�ų�431.4kJ������
��ѡB��
���������
�����Ѷȣ���
4��ѡ���� S2Cl2�ǹ㷺������ҵ������������S2Cl2��һ�ֳȻ�ɫ��Һ�壬��ˮ��ˮ�⣬��������ʹƷ����ɫ�����壬��ṹ��H2O2���ƣ�����˵��������ǣ�������
A��S2Cl2�����е�����Sԭ�Ӿ���sp3�ӻ�
B��S2Cl2��H2O��Ӧ�Ļ�ѧ����ʽ����Ϊ��2S2Cl2+2H2O=SO2��+3S��+4HCl
C��S2Br2��S2Cl2�ṹ���ƣ��۷е�S2Br2��S2Cl2
D��S2Cl2�����е�SΪ+1�ۣ��Ǻ��м��Լ��ͷǼ��Լ��ķǼ��Է���
�ο��𰸣�A��S2Cl2������ÿ��Sԭ�Ӽ۲���Ӷ���=2+2=4�����Բ�ȡsp3�ӻ�����A��ȷ��
B��S2Cl2�е���Ԫ��Ϊ�м��̬��+1�ۣ����ڷ�Ӧ������һ�������ߵ�+4�ۣ�����SO2����һ���ֽ��͵�0�ۣ�����S��������������ԭ��Ӧԭ������B��ȷ��
C��S2Br2��S2Cl2�����ڷ��Ӿ��壬���Ӿ����У�������Խ�����۷е�Խ�ߣ������۷е㣺S2Br2��S2Cl2����C��ȷ��
D��S2Cl2�Ľṹ������H2O2�Ľṹ��ΪCl-S-S-Cl�����е�S-SΪ�Ǽ��Լ���S-Cl��Ϊ���Լ���������������IJ��غϣ������Ǽ��Է��ӣ���D����
��ѡD��
���������
�����Ѷȣ�һ��
5�������
��֪Ԫ��A��B��C��D��E��F����ǰ��������ԭ��������������A��p�ܼ���������s�ܼ���һ�룬C�Ļ�̬ԭ��2p�����2��δ�ɶԵ��ӣ�C��D�γɵĻ�������C�������ϼۣ�E��M���������N���������4����F���ڲ����ܲ��������������������Ϊ1��
��ش��������⡣
��1��Cԭ�ӻ�̬ʱ�����Ų�ʽΪ?��
��2��B��C����Ԫ�ص�һ������Ϊ?��?(��Ԫ�ط��ű�ʾ)���Խ�����ԭ�� ?��
��3����дһ����AB�����ӻ�Ϊ�ȵ����������?��
��4��B��C�γɵ���ԭ�������ӵ����幹��Ϊ?������Bԭ�ӵ��ӻ�������?��
��5��F(OH)2������ˮ�������ڰ�ˮ��д�������ڰ�ˮ�����ӷ���ʽ?��
��6��D��E�γɵĻ�����ľ����ṹ��ͼ���仯ѧʽΪ?����EDE= ?��E����λ����?����֪������ܶ�Ϊ��g��cm-3�������ӵ�����ΪNA�����߳�a=?cm��(�æѡ�NA�ļ���ʽ��ʾ)

�ο��𰸣���1��1s22s22p4��
��2��N��O����ԭ�Ӻ���2p�Dz㴦�ڰ�����Ľ��ȶ��ṹ������ʧȥ���ӣ��ʵ�һ�����ܱ���ԭ�Ӵ�
��3��C22- ��O22+��
��4��ƽ�������Σ�sp2��
��5��Cu(OH)2+4NH3��H2O = Cu(NH3)42+ + 2OH- + 4H2O[��Cu(OH)2+4NH3 = Cu(NH3)42+ + 2OH-]��
��6��CaF2? 109��28��? 8?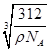
���������Ԫ��A��B��C��D��E��F����ǰ�����ڣ���ԭ��������������A��p�ܼ���������s�ܼ���������һ�룬P�ܼ�����2�����ӣ���A��CԪ�أ�C�Ļ�̬ԭ��2p�����2��δ�ɶԵ��ӣ���CΪC��OԪ�أ�ԭ������С��B��CΪOԪ�أ�B��ԭ����������A��С��C������B��NԪ�أ�C��D�γɵĻ�������C�������ϼۣ���D�ķǽ����Դ���C������D��FԪ�أ�E��M���������N���������4����ԭ����������FԪ�أ�Eԭ������С��29������Eԭ��������������2��N��Ϊ2��M���������8�����Ԫ����CaԪ�أ�F���ڲ����ܼ����������������������Ϊ1����F��CuԪ�ء�
��1��C��OԪ�أ���ԭ�Ӻ�����8�����ӣ���̬ԭ�Ӻ�������Ų�ʽΪ��1s22s22p4��
��2��B��NԪ�أ�C��OԪ�أ�ԭ�ӹ����������Ӵ���ȫ����ȫ�ա�����ʱԭ�����ȶ�����ԭ�Ӻ���2p�Dz㴦�ڰ�����Ľ��ȶ��ṹ������ʧȥ���ӣ��ʵ�һ�����ܱ���ԭ�Ӵ�
��3��ԭ�Ӹ�����ȡ��۵�������ȵ�����Ϊ�ȵ����壬��CN-���ӻ�Ϊ�ȵ��������CO��C22-��O22+��
��4��B��C�γɵ���ԭ��������Ϊ��������ӣ�����������м۲���ӶԸ���=3+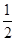 ?(5+1?3��2)=3���Ҳ����µ��Ӷԣ�������ռ乹��Ϊƽ�������Σ�Nԭ�Ӳ���sp2�ӻ���
?(5+1?3��2)=3���Ҳ����µ��Ӷԣ�������ռ乹��Ϊƽ�������Σ�Nԭ�Ӳ���sp2�ӻ���
��6���þ�����Fԭ�Ӹ���=8����ԭ�Ӹ���=8��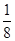 +6��
+6��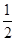 =4�����Ը�ԭ�Ӻͷ�ԭ�Ӹ���֮��=4��8=1��2�����仯ѧʽΪ��CaF2����ԭ�ӵ���λ����8�������߳�=
=4�����Ը�ԭ�Ӻͷ�ԭ�Ӹ���֮��=4��8=1��2�����仯ѧʽΪ��CaF2����ԭ�ӵ���λ����8�������߳�= cm=
cm=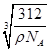 cm��
cm��
�����Ѷȣ�һ��