1�������� Ϊ�ⶨijͭ���Ͻ�ijɷ֣���30.0g�Ͻ�����80mL13.5mol/L��ŨHNO3�У����Ͻ���ȫ�ܽ���ռ�������6.72L(��״��)���������Һ��pH=0�����跴Ӧ����Һ�������Ϊ80mL���Լ��㣺
(1)����ԭ��HNO3�����ʵ�����
(2)�Ͻ���Ag������������
�ο��𰸣�
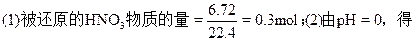
[H+]=1mol��L��
���ԣ��μӷ�Ӧ��HNO3�����ʵ���=(13.5-1)��0.08=1mol��
�裺�Ͻ�Agxg����Cu(30-x)g��
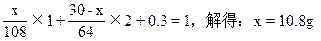
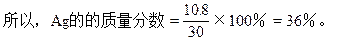
����������������ؼ����ڰ���Cu��Ag��ŨHNO3��Ӧ�����У�������ŨHNO3ϡ�͵ļ���ʵ�ʣ������漰�ķ�Ӧ���ĸ���
Ag+2HNO3(Ũ)====AgNO3+NO2��+H2O? (1)
Cu+4HNO3(Ũ)====Cu(NO3)2+2NO2��+2H2O? (2)
3Ag+HNO3(ϡ)====3AgNO3+NO��+2H2O? (3)
3Cu+8HNO3(ϡ)====3Cu(NO3)2+2NO��+4H2O? (4)
��ȡ�Է�Ӧ��ϵ��ʼ̬����̬������������������غ㷨��ɻ��ʮ�ּ�ݵļ��㡣
�۲��ĸ���ѧ����ʽ�����ѿ���������ԭ��HNO3��ת����NO��NO2������Nԭ�����غ����������ԭ����������ʵ�������NO��NO2���ʵ���֮�͡�����֪��NO��NO2���������������ñ���ԭ��HNO3������
��HNO3�����÷���������HNO3�������ʵ������ڱ���ԭHNO3��ֻ���������õ�HNO3���ʵ���֮�͡��ɻ�ѧʽAgNO3��Cu(NO3)2���ɽ�ֻ�����õ�HNO3����Ag��Cu�����ʵ�������������
n(HNO3)====n(NO+NO2)+n(Ag)+2n(Cu)
�ݴ˿ɼ�ݵ����Ag������������
�����Ѷȣ�һ��
2��ѡ���� ������Ϊm g��������ͭ�۵Ļ�������100mL 4mol��L��1 HNO3��Һ(����)����ַ�Ӧ�����û�ԭ����Ϊ0.05mol NO������������Һ�м���������NaOH��Һ��������ȫ�����������Ϊ
A��5.52g
B��(m+6.8)g
C��(m+2.55)g
D��(m+12.0)g
�ο��𰸣�C
������������û�ԭ����Ϊ0.05mol NO������ת�Ƶĵ���������0.15mol��������ͭ�۹�ʧȥ0.15mol���ӣ���0.15mol������ɣ�����Ҫ���0.15mol���������ӣ���������Ϊ������ͭ�۵�����mg+0.15mol���������ӣ���Ϊ(m+2.55)g����ѡC��
�����Ѷȣ���
3��ѡ���� �����ڿ����е��������ʣ����������ʻ�ɫ����
A��Ũ����
B���Ȼ�������Һ
C���屽
D���廯��
�ο��𰸣�B
�������������ȶ����ڿ����зֽ�(����ԭ��NO2)����NO2�����ɵ�NO2���������Ի�ɫ��Fe2�����ȶ����ڿ����б�����������Fe3�����Ի�ɫ�������ڿ����в��ȶ����������Էۺ�ɫ�����屽�������廯�����ȶ����ֽ���Ժ�ɫ����ԭ�����廯������ԭ����������ĩ��
�����Ѷȣ���
4������� ��14�֣����Ը������������Ĺ�ҵ��ҺΪԭ�������������Ĺ�������(���ֲ�����������)��
��.�ӷ�Һ���ᴿ���ᾧ��FeSO4��7 H2O��
H2O��
��.��FeSO4��7H2O���Ƴ���Һ��
��.FeSO4��Һ���Թ�����NH4HCO3��Һ��ϣ��õ���FeCO3����Һ��
��.����Һ���ˣ���90 ����ˮϴ�ӳ����������õ�FeCO3���塣
��.����FeCO3���õ�Fe2O3���塣
��֪��NH4HCO3����ˮ�зֽ⡣
(1)���У�����������м��ȥ��Һ�е�Fe3�����÷�Ӧ�����ӷ���ʽ��_________________��
(2)���У����һ�����ᣬ���������?�����û�ѧƽ��ԭ���������������________________________________________________________________________��
(3)���У�����FeCO3�����ӷ���ʽ��___________________________________________
��FeCO3��Һ��ʱ�䱩¶�ڿ����У����в��ֹ�������Ϊ���ɫ���ñ仯�Ļ�ѧ����ʽ��_______________________________________��
(4)���У�ͨ������SO���жϳ����Ƿ�ϴ�Ӹɾ�������SO�IJ�����__________
________________________________________________________________________��
(5)��֪����FeCO3�Ļ�ѧ����ʽ��4FeCO3��O22Fe2O3��4CO2��������464.0  kg��FeCO3���õ�316.8 kg��Ʒ������Ʒ������ֻ��FeO����ò�Ʒ��Fe2O3��������________kg��(Ħ������/g��mol��1��FeCO3 116 Fe2O3 160 FeO 72)
kg��FeCO3���õ�316.8 kg��Ʒ������Ʒ������ֻ��FeO����ò�Ʒ��Fe2O3��������________kg��(Ħ������/g��mol��1��FeCO3 116 Fe2O3 160 FeO 72)
�ο��𰸣�

�����������
�����Ѷȣ�һ��
5������� ͭ��һ���������ϵ�dz����е���ɫ�����������£�Cu2+����Һ���ȶ���Cu+�����������������绯��Ӧ��2Cu+=Cu2++Cu�������+1��ͭ�Ļ�������������磺Cu20��Cul��CuCl��CuH �ȡ�
��1����CuCl2��Һ����μ������KI��Һ�����ܷ����ķ�Ӧ�У�
2Cu2++4I-=2CuI������ɫ��+I2; 2Cu2++4I-+2Cl-=CuCl������ɫ��+I2
��֪��������Ksp(CuCl)=1.20��10-6(mol/L)2; Ksp(CuI)=5.06��10-12(mol/L)2���ɴ��ƶ�������Ӧ������Ҫ������Ļ�ѧʽ��______��
��2����CuH�м������ϡHC1�����������ɣ��÷�Ӧ�����ӷ���ʽΪ______��
��3������ͭ����Cu2S��FeS�ۺϳɺ�Cu 18%��20%��һ�����ʣ������ۼ������{���´����������ͭ�е�Cu2S������ΪCu2O�����ɵ�Cu2O��Cu2S��Ӧ���ɴ�ͭ������������Ӧ�Ļ�ѧ����ʽ�ֱ���______��______��
��4�������£���0.20 mol ? L-1����ͭ��Һ�м�������������Һ������dz��ɫ������ͭ����������Һ��pH = 6ʱ��c(Cu2+)=______mol.L?1��[��֪��Ksp(CuI)=2.2��10-20(mol/L)3]
��5����0.80 gCuSO4 ? 5H2O��Ʒ���ȷֽ⣬����ˮ�����й����������¶ȵı仯����ͼ��ʾ��

��ȷ��110��Cʱ�������ʵĻ�ѧʽ____________����Ҫ��д���ƶϹ��̣�
�ο��𰸣���14�֣�
��1��CuI��2�֣�
��2��2CuH+2H+= Cu2++ Cu+2H2����2�֣�
��3��2Cu2S��3O2 2Cu2O��2SO2��2�֣���2Cu2O��Cu2S
2Cu2O��2SO2��2�֣���2Cu2O��Cu2S 6Cu��SO2����2�֣�
6Cu��SO2����2�֣�
��4��2.2��10-4?��2�֣�
��5����110��ʱ�������ʵĻ�ѧʽΪCuSO4��xH2O�����������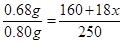 �����x=3,�ù������ʵĻ�ѧʽΪCuSO4��3H2O������ϵʽ2�֣����2�֣���4�֣����������ⷨ���۷֣�
�����x=3,�ù������ʵĻ�ѧʽΪCuSO4��3H2O������ϵʽ2�֣����2�֣���4�֣����������ⷨ���۷֣�
�����������1������CuI��Ksp��С���Ҽ������KI��Һ����������CuClҲ��ת��ΪCuI,������������CuI
��2��Cu+�����������������绯��Ӧ��2Cu+=Cu2++Cu�����Է�����Ӧ2CuH+2H+= Cu2++ Cu+2H2��
��3��������Ϣ��ʾ��ע����Ԫ��ȼ�պ�����SO2,���������غ㶨�ɣ�д�����̡�����
��4����pH = 6֪C(OH-)=10-8mol/L,����Ksp=c��Cu2+��C(OH-)2��ʽ�ȵý��
��5������
�����Ѷȣ�һ��