1、选择题 一定条件下,浓度都是1 mol・L-1的两种气体X2和Y2,在密闭容器中反应,生成气体Z,4 s后,X2、Y2、Z的浓度分别是0.4 mol・L-1、0.8 mol・L-1、0.4 mol・L-1,若用X、Y表示Z的化学式,该反应的化学方程式为
A.X2+2Y2===2XY2
B.2X2+Y2===2X2Y
C.3X2+Y2===2X3Y
D.X2+3Y2===2XY3
参考答案:C
本题解析:根据题意X2、Y2、Z的浓度变化量分别是(mol/L)1-0.4=0.6、1-0.8=0.2、0.4,则根据变化量之比是相应的化学计量数之比可知,X2、Y2、Z的化学计量数分别是3、1、2,所以答案选C。
点评:该题是高考中的常见题型,属于基础性试题的考查。试题基础性强,侧重对学生基础知识的巩固和训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确物质的变化量之比和化学计量数之比的关系,然后灵活运用即可。
本题难度:一般
2、填空题 (8分)在一定温度下,体积为2 L的密闭容器中,NO2和N2O4之间发生反应:2NO2 (g) (红棕色) N2O4(g) (无色),如图所示。
N2O4(g) (无色),如图所示。
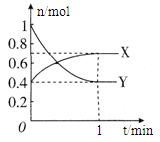
(1)曲线??(填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。
(2)若升高温度,则v(正)??,v(逆)??。(填“加快”或“减慢”)。
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=18 mol/(L・min),乙中v(N2O4)=0.2 mol/(L・s),则?中反应更快。
(4)在0到1 min中内用X表示该反应的速率是?,该反应达限度时,Y的转化率?,反应开始时与反应达平衡状态时的压强之比为?。
参考答案:

本题解析:(1)由方程式N2O4(g)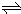 2NO2?(g),可知反应中NO2?的物质的量变化较大,则Y表示NO2的物质的量随时间的变化曲线,故答案为:Y;
2NO2?(g),可知反应中NO2?的物质的量变化较大,则Y表示NO2的物质的量随时间的变化曲线,故答案为:Y;
(2)温度升高,正逆反应速率都增大,故答案为:加快;加快;
(3)甲中v(NO2)=0.3mol?L-1?min-1,乙中v?(N2O4)=0.2mol?L-1?min-1,v(NO2)=2v(N2O4)=0.4mol?L-1?min-1,
则乙反应较快,故答案为:乙;
(4)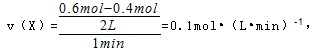
该反应达最大限度时,Y的转化率为:
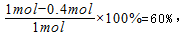
开始时:n(X)+n(Y)=0.4mol+1mol=1.4mol,
平衡时:n(X)+n(Y)=0.7mol+0.4mol=1.1mol,
在相同条件下,气体的压强之比等于物质的量之比,
则反应开始时与反应达平衡状态时的压强之比为1.4mol:1.1mol=14:11,
故答案为:0.1mol?(L?min)-1;60%;14:11;。
本题难度:一般
3、选择题 把0.6 molX气体和0.4 molY气体混合于2L容器中,使它们发生如下反应:3X(g)+Y(g) nZ(g) +2W(g);
nZ(g) +2W(g);
5 min 末已生成0.2 molW,若测知以Z浓度来表示的反应速率为0.01 mol・L-1・min-1,则上述反应中Z气体的计量系数n 的值是
A.1
B.2
C.3
D.4
参考答案:A
本题解析:
本题难度:简单
4、选择题 右图中的曲线是在其他条件一定时反应:2NO(g)+O2(g) 2NO2(g)(正反应放热)中NO的最大转化率与温度的关系。图上标有A、B、C、D、E五点,其中表示未达到平衡状态,且v正>v逆的点是(?)
2NO2(g)(正反应放热)中NO的最大转化率与温度的关系。图上标有A、B、C、D、E五点,其中表示未达到平衡状态,且v正>v逆的点是(?)
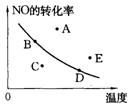
A.A或E?B.C? C.B? D.D
参考答案:B
本题解析:根据图像可知,曲线表示平衡线,即曲线上任意1点都表示一定条件下的平衡状态,因此A、E、C三点不是平衡状态。C点要达到平衡状态,则在温度不变的条件下,NO的转化率是升高的,即反应是向正反应方向进行的,也就说正反应速率大于逆反应速率,而A和E则正好是相反的,所以答案选B。
本题难度:一般
5、选择题 已经建立化学平衡的某可逆反应,当条件改变时化学平衡向正反应方向移动,下列叙述正确的是①生成物的质量分数一定增加 ②生成物的产量一定增加? ③反应物的转化率一定增加 ④反应物的浓度一定减小? ⑤正反应速率一定比逆反应速率大
A ①②③④⑤? B? ②④⑤? C ②⑤? D? ⑤
参考答案:C
本题解析:略
本题难度:简单