1、选择题 常温下,对于1 L 0.005 mol・L-1硫酸表述中正确的是( )
A.由水电离出的c(H+)=1.0×10-12 mol・L-1
B.加水稀释后,溶液中所有离子的浓度均减少
C.2c(H+)=c(SO42-)+c(OH-)
D.滴加稀氨水使pH=7,则c(NH4+)=c(SO42-)
2、选择题 对pH=3的醋酸溶液和pH=3的HCl溶液等体积混和后,溶液的PH值?
A.PH<3
B.PH>3
C.PH="3"
D.无法确定
3、填空题 有50mLNaOH溶液,向其中逐渐通入一定量的CO2,随后取此溶液稀释.后向溶液中逐滴加入0.1mol/L的HCl溶液,产生的CO2气体体积(标况)与所加入的盐酸的体积之间的如下图所示:
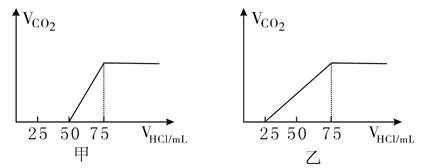
试分析NaOH在吸收CO2气体后,在甲所得溶液中存在的溶质是??,其物质的量之比是?, 产生的CO2气体体积(标况)是?. 在乙所得溶液中存在的溶质是?,其物质的量之比是?, 产生的CO2气体体积(标况)是?。
4、填空题 (7分)(1)室温下,把1 mL 0.1 mol・L-1的H2SO4加水稀释成2 L溶液,在此溶液中由水电离产生的H+,其浓度接近于?
(2)室温时,将0.1 mol/L盐酸和0.07mol/L氢氧化钡溶液1:5(体积比)混合后,该混合溶液的pH=_______
(3)某温度时,0.1 mol・L-1NaOH溶液的pH=12。该温度下,10体积pH=a的某强酸与1体积pH=b的某强碱混合后,溶液呈中性,则a和b满足的关系____________________
5、选择题 在常温下,pH = 9的NaOH溶液和CH3COONa两种溶液中,假设由水电离产生的OH─离子浓度分别为a和b,则a与b的关系为
A.a>b
B.a=10-4b
C.b =10-4 a
D.a =b