1、选择题 在H2O2分解实验中,当加入少量MnO2粉末时,H2O2的分解速率增大。该实验中使H2O2分解速率增大的主要因素是
A.温度
B.催化剂
C.反应物的接触面积
D.反应物的浓度
2、选择题 下列说法正确的是
A.向等体积的20%的H2O2溶液和10%的H2O2溶液中分别滴加等体积的0.1mol?L―1 FeCl3溶液和0.1 mol?L―1CuCl2溶液,前者产生气泡快,这个实验可以充分证明催化剂具有选择性
B.利用水解反应可以制取某些无机化合物如TiO2、SnO2等
C.将0.1 mol?L―1醋酸加水稀释,溶液中各离子浓度均减小
D.室温下同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7
3、选择题 关于化学反应2A(g)+B(g)?3C(g)+D(g),下列反应速率表示反应最快的是( )
A.v(A)=1.4mol?L-1?s-1
B.v(B)=0.6mol?L-1?s-1
C.v(C)=1.5mol?L-1?s-1
D.v(D)=1.6mol?L-1?min-1
4、填空题 某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
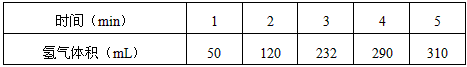
(1)哪一时间段(指0~1.1~2.2~3.3~4.4~5 min)反应速率最大_______________,原因是
_____________________________ 。
(2)哪一段时段的反应速率最小_______________,原因是__________________________。
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
你认为可行的是(填编号)_________________。
(4)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率____________(设溶液体积不变,要写出计算过程)。
5、选择题 100mL6mol/L的H2SO4跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成H2的总量,可向反应物中加入适量 (? )
A.Na2CO3(s)
B.水
C.Na2SO4(s)
D.(NH4)2SO4(s)