1��ѡ���� ��H2O2�ֽ�ʵ���У�����������MnO2��ĩʱ��H2O2�ķֽ���������ʵ����ʹH2O2�ֽ������������Ҫ������
A���¶�
B������
C����Ӧ��ĽӴ����
D����Ӧ���Ũ��
�ο��𰸣�B
��������������ܼӿ컯ѧ��Ӧ���ʣ����Լ�������MnO2��ĩʱH2O2�ֽ�����������Ϊ������
�����Ѷȣ���
2��ѡ���� ����˵����ȷ����
A����������20%��H2O2��Һ��10%��H2O2��Һ�зֱ�μӵ������0.1mol?L��1 FeCl3��Һ��0.1 mol?L��1CuCl2��Һ��ǰ�߲������ݿ죬���ʵ����Գ��֤����������ѡ����
B������ˮ�ⷴӦ������ȡijЩ����������TiO2��SnO2��
C����0.1 mol?L��1�����ˮϡ�ͣ���Һ�и�����Ũ�Ⱦ���С
D��������ͬŨ�ȡ�ͬ�����ǿ����ǿ����Һ��Ϻ���Һ��pH��7
�ο��𰸣�B
���������ѡ��A����ȷ����Ϊ˫��ˮ��Ũ�Ȳ�ͬ������ֱ�ӱȽϴ����Ĵ�������������������ʣ����ڵ���ƽ�⣬ϡ�ʹٽ����룬������Һ��OH����Ũ��������ģ�ѡ��C����ȷ��ѡ��D����ȷ����Ϊ����ȷ�������Ԫ������ѡB��
�����Ѷȣ�һ��
3��ѡ���� ���ڻ�ѧ��Ӧ2A��g��+B��g��?3C��g��+D��g�������з�Ӧ���ʱ�ʾ��Ӧ�����ǣ�������
A��v��A��=1.4mol?L-1?s-1
B��v��B��=0.6mol?L-1?s-1
C��v��C��=1.5mol?L-1?s-1
D��v��D��=1.6mol?L-1?min-1
�ο��𰸣����ڷ�Ӧ A+3B�T2C����ת��ΪB��ʾ�����ʽ��бȽϣ�
A��VA=1.4 mol/��L?s��=84mol/��L?min������Ӧ����֮�ȵ����������֮�ȣ���VB=0.5VA=42mol/��L?min����
B��VB=0.6mol/��L?s��=36mol/��L?min����
C��VC=1.5mol/��L?s��=90mol/��L?min������Ӧ����֮�ȵ����������֮�ȣ���VB=13VC=30mol/��L?min����
D��VD=1.6mol/��L?min������Ӧ����֮�ȵ����������֮�ȣ���VB=VD=1.6mol/��L?min����
��ѡA��
���������
�����Ѷȣ���
4������� ijѧ��Ϊ��̽��п�����ᷴӦ�����е����ʱ仯������100mLϡ�����м���������п�ۣ�����ˮ�������ռ���Ӧ�ų���������ʵ���¼���£��ۼ�ֵ����
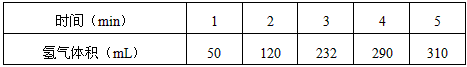
��1����һʱ��Σ�ָ0��1��1��2��2��3��3��4��4��5 min����Ӧ�������_______________��ԭ����
_____________________________ ��
��2����һ��ʱ�εķ�Ӧ������С_______________��ԭ����__________________________��
��3�������Ӧ̫���ң�Ϊ�˼�����Ӧ���ʶ��ֲ����ٲ����������������������зֱ����������������Һ��
A������ˮ B��NaCl��Һ C��Na2CO3��Һ D��CuSO4��Һ
����Ϊ���е��ǣ����ţ�_________________��
��4����2��3����ʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����____________������Һ������䣬Ҫд��������̣���
�ο��𰸣���1��2��3 min����÷�Ӧ�Ƿ��ȷ�Ӧ��2��3 minʱ�¶ȸ�
��2��4��5 min����Ϊ4��5 minʱH+Ũ��С
��3��AB
��4��0.1 mol/(L��min)
���������
�����Ѷȣ�һ��
5��ѡ���� 100mL6mol/L��H2SO4������п�۷�Ӧ��һ���¶��£�Ϊ�˼�����Ӧ���е����ʣ����ֲ�Ӱ������H2������������Ӧ���м������� (? )
A��Na2CO3(s)
B��ˮ
C��Na2SO4(s)
D��(NH4)2SO4(s)
�ο��𰸣�B
�����������
�����Ѷȣ���