1、选择题 下述实验设计能够达到目的的是?(?)
编号
| 实验目的
| 实验设计
|
A
| 除去CO2中少量的SO2
| 将混合气体通过饱和Na2CO3溶液
|
B
| 除去Cu粉中混有的CuO
| 向混合物中滴加适量稀硝酸
|
C
| 证明钠的金属活动性比铝强
| 向AlCl3溶液中投入金属钠
|
D
| 证明H2CO3酸性比H2SiO3强
| 将CO2通入Na2SiO3溶液中
|
?
参考答案:D
本题解析:略
本题难度:一般
2、实验题 (10分)为了比较氯和碘单质氧化性的强弱,可先制取氯气,并将氯气通入碘化钾淀粉溶液中。下图是本实验所需的仪器和药品:图中A.B.C.D.E.F分别表示玻璃导管或仪器接口。

请回答下列问题:
(1)气体流向从左到右。实验前,上述各仪器装置的正确连接顺序是(填各接口的字母符号);D从E处插入烧瓶后,_____________接_____________,_____________接_____________。
(2)写出制备 的反应方程式:______?。
的反应方程式:______?。
某学生用含0.4molHCl的浓盐酸和足量MnO2反应制 得到的
得到的 总小于
总小于 (标况下)为什么?___________________?
(标况下)为什么?___________________?
(3)实验完成后,装置1中的溶液为_____________色,再向其中滴加足量 溶液颜色是否褪去?_____________(填“是”或“不是”),装置②中NaOH溶液的作用是:______? .
溶液颜色是否褪去?_____________(填“是”或“不是”),装置②中NaOH溶液的作用是:______? .
(4)工业上,可用 制备漂白粉,请写制备漂白粉的离子反应方程式:
制备漂白粉,请写制备漂白粉的离子反应方程式:
____________??。
参考答案:(10分)?
(1)(2分)F.B.A.C
(2)(2分)
浓盐酸随着反应的进行浓度变稀后,将不再反应, 浓盐酸具有挥发性。(1分)
(3)(3分)蓝?是?吸收剩余的Cl2
(4)(2分)
本题解析:略
本题难度:简单
3、计算题 通常情况下,CO与O2的混合气体m L,用电火花引燃后体积变为n L(在相同条件下测定)。
(1)试确定原混合气体中CO与O2的体积。
(2)若反应后的气体密度在相同条件下为氢气的15倍时,试确定反应气体的组成及体积之比。
参考答案:(1)(A)当两者恰好完全作用时,V(CO)=2(m-n) L V(O2)=(m-n) L;
(B)当CO过量时,过量的CO的体积=m L-[2(m-n) L+(m-n) L]=(3n-2m) L,原混合物中V(O2)=(m-n) L V(CO)=(3n-2m) L+2(m-n) L=n L;
(C)当O2过量时,过量的O2的体积=m L-[2(m-n) L+(m-n) L]=(3n-2m) L;原混合物中V(CO)=2(m-n) L,V(O2)=(3n-2m) L+(m-n) L=(2n-m) L;
(2)CO2与CO的体积比为1∶7。
本题解析:由反应:
2CO + O2====2CO2 ΔV
2? 1? 2? 1
2(m-n)? (m-n)? (m-n)
可知:(A)当两者恰好完全作用时,V(CO)=2(m-n) L
V(O2)=(m-n) L
(B)当CO过量时,过量的CO的体积=m-[2(m-n)+(m-n)]=(3n-2m) L
原混合物中V(O2)=(m-n) L
V(CO)=(3n-2m) L+2(m-n) L=n L
(C)当O2过量时,过量的O2的体积=m L-[2(m-n) L+(m-n) L]=(3n-2m) L
原混合物中V(CO)=2(m-n) L
V(O2)=(3n-2m) L+(m-n) L=(2n-m) L
若反应后的气体密度在相同条件下为氢气的15倍时,混合气体的平均相对分子质量是30,由于产物中肯定有CO2,它的相对分子质量大于30,所以另一种气体的相对分子质量必小于30,另一种气体只能是CO(也就是说O2不可能有余),该混合气体的组成可用下法求得:
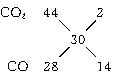
可得V(CO2)∶V(CO)=1∶7
本题难度:简单
4、实验题 兴趣小组的学生根据Mg与CO2反应原理推测钠也能在CO2中燃烧,为了确定其产物并进行实验论证,某同学设计了下列装置进行实验(已知PdCl2能被CO还原得到黑色的Pd)。请回答下列问题
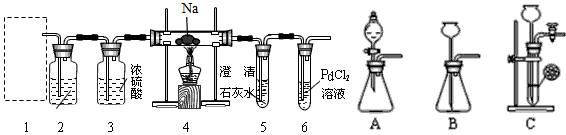
(1)上图装置2中应盛放___________溶液(写化学式)。
(2)为了使反应随开随用,随关随停,上图方框内应选用__________装置(填上图字母代号)。
(3)检查装置的气密性完好并装好药品后,在点燃酒精灯前,应先进行1装置的操作,待装置_______(填数字编号)中出现__________现象时,再点酒精灯,这步操作的目的是____________________
(4)①若装置6中有黑色沉淀生成,装置4中残留固体(只有一种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为______________________________。
②若装置6中溶液无明显现象,装置4中残留固体(有两种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为______________________________。
(5)指导老师认为,不仅要检验残留固体中是否有碳酸钠还要检验其中是否有氧化钠和碳。当确认钠充分反应后,请你设计一个简单实验,验证装置4中的残留固体中是否有Na2O和C:________________________________________________________________________________
参考答案:(1)饱和NaHCO3?
(2)C
(3)5;澄清的石灰水变浑浊;驱除系统内的空气
(4)①2Na+2CO2==Na2CO3+CO;②4Na+3CO2==2Na2CO3+C
(5)将残留固体溶于水,若有黑色不溶颗粒,则说明有碳生成;在所得水溶液中加入过量BaCl2溶液,有沉淀生成,说明有Na2CO3生成;过滤,用pH试纸检验滤液,若滤液呈碱性,则残留固体中含有Na2O
本题解析:
本题难度:困难
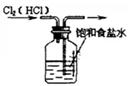
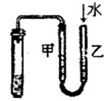
5、选择题 如图所示的实验中,能达到实验目的的是
| 
| 
| 
|
①除去Cl2中的HCl杂质
| ②用铜和稀硝酸制取少量NO
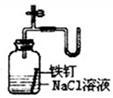
| ③证明铁生锈时空气参与反应
| ④检验装置气密性
|
?
A.①②③④? B.③④? C.②③④? D.①④
参考答案:B
本题解析:氯化氢极易溶于水,则除去Cl2中的HCl杂质可以选择饱和食盐水,但应该是长口进,短口出,①不正确;NO极易被氧化生成NO2,所以不能用排空气法收集,②不正确;实验③中铁生锈时如果空气参与反应,则U形瓶中但液面会发生变化,据此可以判断,③正确;根据检验装置气密性的方法可知,选项④正确,答案选B。
点评:化学实验常用仪器的使用方法和化学实验基本操作是进行化学实验的基础,对化学实验的考查离不开化学实验的基本操作,所以该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确及灵活运用知识解决实际问题的能力。
本题难度:一般