1、选择题 在接触法制硫酸的有关问题中,下列叙述不正确的是
A.燃烧黄铁矿制取SO2的化学方程式是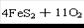


B.含SO2的炉气在进行氧化反应前必须净化,其目的就是为了除尘、以防催化剂中毒
C.用98.3%的浓H2SO4吸收SO3制取发烟硫酸,用稀H2SO4吸收SO3制较浓的H2SO4
D.SO2氧化时必须使用催化剂(例如V2O5等),催化剂的作用是提高SO2的氧化速率,缩短到达平衡所需的时间,但使用催化剂不会提高SO2的转化率
参考答案:C
本题解析:略
本题难度:简单
2、选择题 把SO2通入下列各组物质的混合液中,有白色沉淀产生的是
A.Ba(NO3)2、HCl
B.BaCl2、NaCl
C.NH4Cl、CaCl2
D.MgCl2、(NH4)2SO4
参考答案:A
本题解析:Ba(NO3)2、HCl混合溶液具有强氧化性,当通入二氧化硫后会生成硫酸钡沉淀,其他选项均不反应所以答案选A。
本题难度:简单
3、选择题 向FeCl3和BaCl2的酸性混合溶液中通入SO2气体,有白色沉淀生成。此沉淀是?(?)

A.BaSO4
B.FeS
C.BaSO3
D.S
参考答案:A
本题解析: 此题隐含了Fe3+的强氧化性,容易误选C
此题隐含了Fe3+的强氧化性,容易误选C
本题难度:一般
4、计算题 (10分) 向氢氧化钠溶液中慢慢地通入二氧化硫气体,反应生成正盐,当继续通入过量二氧化硫时,正盐便转化成酸式盐。
⑴写出上述反应的化学方程式①?
②?
⑵标准状态下,向100mL2mol/L的NaOH溶液中通入3.36L二氧化硫气体,反应后溶液中溶质的成分为?。
⑶试计算,在标准状态下,100mL2mol/L的NaOH溶液中最多可吸收多少体积二氧化硫气体?
参考答案:(10分)⑴SO2+2NaOH?Na2SO3+H2O? 2分
Na2SO3+SO2+H2O?2NaHSO3 ?2分
⑵Na2SO3 、NaHSO3? 2分
⑶当NaOH溶液反应吸收最多体积二氧化硫气体时,反应为
SO2? +? NaOH ??NaHSO3
1mol? 1mol
0.2mol? x? x=0.2mol
V(SO2)=22.4L/mol×0.2mol=4.48L? 4分
本题解析:略
本题难度:一般
5、选择题 下列说法错误的是?
A.HNO3酸化后的BaCl2试液加入某溶液中有白色沉淀生成,不能判断该溶液中一定存在SO42-离子
B.将SO2气体通入Ba(OH)2溶液中,有白色沉淀生成
C.将SO2气体通入BaCl2溶液中,有白色沉淀生成
D.将SO2气体通入用硝酸酸化过的BaCl2溶液中,有白色沉淀生成
参考答案:C
本题解析:①SO2,SO32-都具有还原性,能被HNO3氧化为SO42-;②常见不溶水也不溶于酸的盐类有BaSO4,AgX,重金属硫化物。A,D溶液中均加入HNO3,都可能生成BaSO4↓;A原溶液中有Ag+,生成沉淀也可能是AgCl,或是原有SO32-,故不能判</PGN0090B.TXT/PGN>断一定有SO42-;B中反应为:Ba2++2OH-+SO2=BaSO3↓+H2O能形成BaSO3↓,而C中Ba2+,Cl-与SO2不会形成BaSO3↓,因SO2+H2OH++HSO3-,HSO3-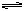 H++SO32-通入SO2溶液中产生SO32-,也产生了H+,故BaSO3↓不能存在。
H++SO32-通入SO2溶液中产生SO32-,也产生了H+,故BaSO3↓不能存在。
本题难度:一般