1、计算题 (8分)某研究性学习小组用48.0克铜屑与氧化铜的混合物与硫酸和硝酸的混酸100 ml溶液反应制取五水硫酸铜晶体,混酸中硝酸的还原产物为NO,反应过程中不产生SO2,反应后溶液中只有硫酸铜。若在固体混合物中铜屑的质量分数为0.4,试计算:(1)最终制得晶体的质量。(2)混酸中两溶质的物质的量浓度。
2、选择题 中学所学的A、B、C三种物质都是由H、O、S、Na中的三种元素组成的强电解质。A、B的水溶液均呈碱性,测得pH相等的A、B溶液c(A)<c(B);C的水溶液呈酸性。有关说法正确的是
A.A是Na2SO3?
B.? B溶于溴水中,不可能生成沉淀
C.? B、C反应的离子方程式可能是:SO3-+2H+→ SO2↑+H2O
D.?若A、B两溶液的pH=9,则两溶液中水电离的OH-的物质的量浓度之比为1:1
3、实验题 已知盐酸加到品红溶液中,使品红溶液的红色加深。试推测:
 (1)向品红溶液中通过量SO2的过程中的现象为__________;加热后的现象为_______。
(1)向品红溶液中通过量SO2的过程中的现象为__________;加热后的现象为_______。
 (2)向品红溶液中通入过量Cl2的过程中,观察到的现象为____________。
(2)向品红溶液中通入过量Cl2的过程中,观察到的现象为____________。
 (3)向品红溶液中通入物质的量比为1∶1且足量的SO2和Cl2后现象为___________。
(3)向品红溶液中通入物质的量比为1∶1且足量的SO2和Cl2后现象为___________。
4、选择题 用如图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应,下列有关说法不合理的是(?)
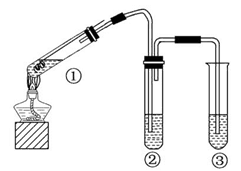
A.上下移动①中铜丝可控制SO2的量
B.②中选用品红溶液验证SO2的生成
C.③中选用NaOH溶液吸收多余的SO2
D.为确认CuSO4生成,向①中加水,观察颜色
5、选择题 已知某物质X能发生如下转化:
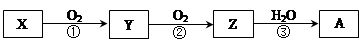
下列有关上述转化关系中物质及其反应的叙述错误的是
A若X?N2或NH3(催化氧化),则A为硝酸
B若X为S 或H2S(完全燃烧),则A为硫酸
C若X为非金属单质或非金属氢化物,则A不一定能与金属铜反应生成Y
D反应①和②一定为氧化还原反应,反应③一定为非氧化还原反应