1������� ��ˮ�̺��ŷḻ����Դ���ڻ�ѧʵ������ģ��Ӻ�ˮ����ȡ��Ҫ�Ĺ�ҵԭ���Ȼ���ʱ����������²������̣�
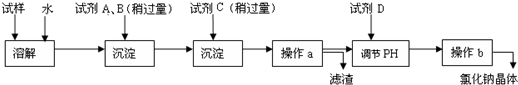
��ش��������⣺
��1�������ṩ���Լ���ѡ���Լ�C��______?��Na2CO3 ��BaCl2 ��ϡ����
��2������b���õ�����Ҫ����Ϊ�ƾ��ơ�______�����żܺͲ�������
��3���������õ��Ȼ����������������������������������ԺͲⶨ�������������������ͼ�������������һ�����������ʵ��Ŀ��װ�ã������ӿڵ���ȷ����˳���ǣ�

A��______��______��______��B��______��______��______��
��4��д��ͨ��C���ձ��������������ӷ�Ӧ����ʽ______
��5������Ȼ�����Һʱ�����ӷ���ʽΪ______
��װ��ı���ʳ��ˮΪ75mL����ͨ��Դһ��ʱ�䣬ֹͣͨ��������Ϊ8.4mL����״��������U�ι��ڵ���Һ��Ͼ��ȣ���
pHԼΪ______����������ǰ����Һ����仯�ɺ��Բ��ƣ�����������ȫ���ݳ���
��6������ȷ��ȡ���������������Ӧ��ȡ�IJ�����______��
�ο��𰸣���1��þ���������������ӳ��������������ʯ������Խ�þ���ӳ���������������ñ����ӳ���������������Ȼ������Խ���������ӳ����������ȳ�þ���ӣ������ȳ���������Ӷ��У���������̼������ӳ������������Ӽ���̼����ת��Ϊ���������Ǽ����̼����Ҫ���ڼ�����Ȼ���֮������̼���ƻ��ȥ��Ӧʣ����Ȼ��������Ӷ������ˣ��ڽ��й��ˣ�����ټ��������ȥ��Ӧʣ������������Ӻ�̼������ӣ����������Լ���˳��Ϊ��ʯ���顢�Ȼ�����̼���ơ�������Ȼ�����ʯ���顢̼���ơ����ᣬ�����Լ�C��Na2CO3���ʴ�Ϊ���٣�
��2���Ȼ�����Һͨ�������ᾧ�õ��Ȼ��ƣ�������Ҫ������Ϊ�ƾ��ơ����������żܺͲ��������ʴ�Ϊ��������
��3���������������������ˮ�������������Ƕ̽�����������A��G����װ�е��۵⻯����Һ��ϴ��ƿ��������ʱ������Ҫ�����̳�������B��D������Ҫ����β����������E��C���ʴ�Ϊ��G��F��H��D��E��C��
��4�����������������Ʒ�ӦCl2+NaOH=NaCl+NaClO+H2O�����ӷ���ʽΪ��Cl2+2OH-�TCl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-�TCl-+ClO-+H2O��
��5��ͨ�����Ϸ���֪����Ӧ�����Ȼ��ƺ�ˮ���������������������������ƣ�����ʽΪ��2NaCl+2H2O?ͨ��?.?Cl2��+H2��+2NaOH�����ӷ���ʽΪ��2Cl-+2H2O?ͨ��?.?Cl2��+H2��+2OH-���ʴ�Ϊ��2Cl-+2H2O?ͨ��?.?Cl2��+H2��+2OH-��
���ⱥ��ʳ��ˮ�ķ���ʽ��2NaCl+2H2O?���?.?2NaOH+H2��+Cl2������������H2�����Ϊ8.4mL��0.000375molʱ�������������Ƶ����ʵ���Ϊ0.00075mol��������Һ��NaOH�����ʵ���Ũ��=0.00075mol0.075L�T0.01mol/L�����������ӵ�Ũ��Ϊ
1��10?-140.01=1��10-12mol/L��PH=12���ʴ�Ϊ��12��
��6����ˮ��������������ķ�������Ͳ��Һ����ƿҺ����ƽ������ʱ��������Ͳ��Һ����ƽ��������װ�ûָ�������ʱ���ж�ȡ���ݣ�
�ʴ�Ϊ����Ͳ��Һ����ƿҺ����ƽ������ʱ��������Ͳ��Һ����ƽ��������װ�ûָ�������ʱ���ж�ȡ���ݣ�
���������
�����Ѷȣ�һ��
2������� ������һ�������Դ����������ȡ�봢����������Դ����������о��ȵ㡣
��֪��CH4(g)��H2O(g)=CO(g)��3H2(g)��H ����206.2 kJ��mol��1
CH4(g)��CO2(g)=2CO(g)��2H2(g)��H ����247.4 kJ��mol��1
2H2S(g)=2H2(g)��S2(g)��H ����169.8 kJ��mol��1
(1)�Լ���Ϊԭ����ȡ�����ǹ�ҵ�ϳ��õ����ⷽ����CH4(g)�� H2O(g)��Ӧ����CO2(g)�� H2(g)���Ȼ�ѧ����ʽΪ_________________________
(2)H2S �ȷֽ�����ʱ������Ӧ����ͨ��һ������������ʹ���� H2S ȼ�գ���Ŀ����________��ȼ�����ɵ� SO2�� H2S ��һ����Ӧ���������ڳ����¾�Ϊ�����壬д���÷�Ӧ�Ļ�ѧ����ʽ��___________________________
(3)H2O ���ȷֽ�Ҳ�ɵõ� H2��������ˮ�ֽ���ϵ����Ҫ���������������¶ȵĹ�ϵ��ͼ����ʾ��ͼ�� A��B ��ʾ������������______________________________________��
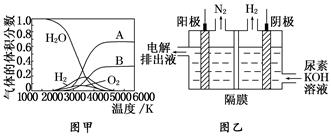
(4)�������[CO(NH2)2]�ļ�����Һ�����װ��ʾ��ͼ��ͼ��(�����и�Ĥ����ֹ����ͨ��������������Ϊ���Ե缫)�����ʱ�������ĵ缫��ӦʽΪ_____________________
(5)Mg2Cu ��һ�ִ���Ͻ� 350 ��ʱ��Mg2Cu �� H2��Ӧ������ MgCu2�ͽ���һ�ֽ���Ԫ�ص��⻯��(���������������Ϊ 0.077)��Mg2Cu �� H2��Ӧ�Ļ�ѧ����ʽΪ_____________________________________
�ο��𰸣�(1)CH4(g)��2H2O(g)=CO2(g)��4H2(g)��H����165.0 kJ��mol��1
(2)ΪH2S�ȷֽⷴӦ�ṩ����
2H2S��SO2=2H2O��3S(��4H2S��2SO2=4H2O��3S2)
(3)H��O(����ԭ�ӡ���ԭ��)
(4)CO(NH2)2��8OH����6e��=CO ��N2����6H2O
��N2����6H2O
(5)2Mg2Cu��3H2��,MgCu2��3MgH2
������������⿼�黯ѧ��Ӧ����������ѧ������ܵ�ת����Ԫ�ػ��������֪ʶ�����ڿ��鿼�����ۺ�����������
(1)��������Ӧ���α��Ϊ�٢ڢۣ����ݸ�˹���ɣ��ɷ�Ӧ�١�2����Ӧ�ڼ���������Ӧ���Ȼ�ѧ����ʽ��CH4(g)��2H2O(g)=CO2(g)��4H2(g)��H����165.0 kJ��mol��1��
(3)��ͼ��A��B�����������������Ϊ2��1�����ȷ��AΪHԭ�ӣ�BΪOԭ�ӡ�
(4)H2������Һ�е�H���������ŵ�õ��ģ���������������N2����������������Ӧ���ڼ��Ի����µĵ缫��ӦʽΪ��CO(NH2)2��8OH����6e��=CO ��N2����6H2O��
��N2����6H2O��
(5)��Mg2Cu��ΪMgCu2����֪Mg�����½��������������⻯�������һ�ֽ���Ԫ�ر�ΪMg���ٸ������������������Ϊ0.077����Mg��H���ʵ���֮��Ϊ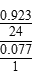 ��
�� ������ѧʽΪMgH2����Ӧ�Ļ�ѧ����ʽΪ��2Mg2Cu��3H2��,MgCu2��3MgH2��
������ѧʽΪMgH2����Ӧ�Ļ�ѧ����ʽΪ��2Mg2Cu��3H2��,MgCu2��3MgH2��
�����Ѷȣ�����
3������� ��ͼ��ʾװ���У��ס��ҡ��������ձ����ηֱ�ʢ��100?g?5.00%��NaOH��Һ��������CuSO4��Һ��100?g?10.00%��K2SO4��Һ���缫��Ϊʯī�缫��

(1)��ͨ��Դ������һ��ʱ���ñ���K2SO4��Ũ��Ϊ10.47%������c�缫�������ӣ��ݴ˻ش����⣺
�ٵ�Դ��N��Ϊ________����
�ڵ缫b�Ϸ����ĵ缫��ӦΪ_________________��
����ʽ����缫b�����ɵ������ڱ�״���µ������________________��
�ܵ缫c�������仯��________g��
(2)���ǰ�����Һ���ᡢ���Դ�С�Ƿ����仯��������ԭ��
����Һ___________________________________��
����Һ___________________________________��
����Һ___________________________________��
(3)�����������ͭȫ����������ʱ����ܷ�������У�Ϊʲô��
________________________________________________________
�ο��𰸣�(1)��������4OH����4e��==2H2O��O2�� ����ˮ���ٵ�������100?g��(1��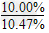 )��4.5?g
)��4.5?g
����O2�������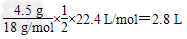 �� ��16
�� ��16
(2)����������Ϊ����ˮ�����٣���Һ��NaOHŨ����������������Ϊ������OH������O2����Һ��H��Ũ�����ӣ�����Դ�Сû�б仯����ΪK2SO4��ǿ��ǿ���Σ�Ũ�����Ӳ�Ӱ����Һ�������
(2)�ܼ������У���ΪCuSO4��Һ��ת��ΪH2SO4��Һ����ӦҲ�ͱ�Ϊˮ�ĵ�ⷴӦ
���������
�����Ѷȣ�һ��
4��ѡ���� �ò��缫���100mL?HNO3��?AgNO3?�Ļ����Һ��ͨ��һ��ʱ����������ռ���2.24L���壨��״��������ԭ�����Һ��Ag+�����ʵ���Ũ��Ϊ��������
A��1mol?L-1
B��2?mol?L-1
C��2.5?mol?L-1
D��3?mol?L-1
�ο��𰸣����缫Ϊ���Ե缫�����HNO3��AgNO3?�Ļ����Һ��ͨ��һ��ʱ����������ռ���2.24L���壨��״������
n�����壩=2.24L22.4L/mol=0.1mol��
����������4OH--4e-=2H2O+O2����֪������0.1molO2ת��0.4mol���ӣ�
���ݵ����غ��֪������ת��0.4mol���ӣ���
2H++2e-=H2��
?0.2mol 0.1mol
? 2Ag++2e-=2Ag
0.2mol 0.2mol
��n��Ag+��=0.2mol��
��ԭ�����Һ��Ag+�����ʵ���Ũ��Ϊ0.2mol0.1L=2mol/L��
��ѡB��
���������
�����Ѷȣ�һ��
5��ѡ���� ��ͼ��ʾ��װ�ã�C��D��E��F��X��Y���Ƕ��Ե缫������Դ��ͨ��װ�ã�������Y���������ɫ���������˵����ȷ����

A����ԴB��������
B�����ף�װ�õ�C��D�缫���е������ɣ��������ʵ���֮��Ϊ2:1
C�����ã�����װ�ø�ͭ������HӦ�����������Һ����������Һ
D�������ң��е����̪��Һ����F�������ȳ��ֺ�ɫ
�ο��𰸣�D
�����������
�����Ѷȣ���