?
�ο��𰸣�������
���������������Ŀ�������DZ�ʾ��ƽ�⡱ʱ������������ѹǿ�����¶ȣ��仯��ϵ���ߡ��ء��ٵ���δ��ƽ��״̬����ӦҪ��������ƽ��״̬�����У��Դ��ж�ij�����������Ĵ�С��ϵ���Ƚϣء�����������ʿ���������ѹǿ�ĸߵͣ����¶ȵĸߵͣ���
�����Ѷȣ���
2��ѡ���� �� 4 mol A ����� 2 mol B ������ 2 L �������л�ϲ���һ�������·������·�Ӧ��2A��g����B��g�� 2C��g������ 2 s���룩���� C ��Ũ��Ϊ 0.6 mol��L��1 ���������м���˵���� 2C��g������ 2 s���룩���� C ��Ũ��Ϊ 0.6 mol��L��1 ���������м���˵����
�� ������ A ��ʾ�ķ�Ӧ��ƽ������Ϊ 0.3 mol��L��1��S��1
�� ������ B ��ʾ�ķ�Ӧ��ƽ������Ϊ 0.6 mol��L��1��S��1
�� 2 s ʱ���� A ��ת����Ϊ70��
�� 2 s ʱ���� B ��Ũ��Ϊ 0.7 mol��L��1��
������ȷ����
A���٢�
B���٢�
C���ڢ�
D���ۢ�
�ο��𰸣�B
���������?2A��g��?��? B��g��? ?2C��g�� ?2C��g��
��ʼ���ʵ�����? 4mol? 2mol? 0
ת�����ʵ�����? 1.2mol? 0.6mol? 1.2mol
ƽ�����ʵ�����? 2.8mol? 1.4mol? 1.2mol
��������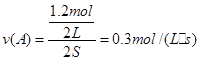 ?�� ?��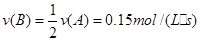
��2 s ʱ���� A ��ת����Ϊ��1.2/4=30�G?��2 s ʱ���� B ��Ũ��Ϊ 1.4/2="0.7" mol��L��1
���ѡB
�����Ѷȣ�һ��
3��ѡ���� ������Ƭ��l00 mL 0.01 mol��L��ϡ���ᷴӦ����Ӧ����̫����Ϊ�˼ӿ�˷�Ӧ���ʶ����ı�H2�IJ���������ʹ�����·����е�
�ټ�H2O �ڼ�KNO3��Һ �۵��뼸��Ũ���� �ܼ����������� �ݼ�NaCl��Һ
���뼸������ͭ��Һ �������¶�(����������ӷ�) �����10 mL 0.1 mol��L����
A���٢ޢ�
B���ۢݢ�
C���ۢߢ�
D���ۢܢޢߢ�
�ο��𰸣�C
����������ټ�ˮ������Ũ�Ƚ��ͣ���Ӧ���ʼ��������ڼ�KNO3��Һ��������Һ����������ڣ�����������������٣����۵��뼸��Ũ���ᣬʹ��Һ��������Ũ������Ӧ���ʼӿ죬���������̶������Բ��������������䣬��ȷ���ܼ������ۣ�������ĽӴ��������Ӧ���ʼӿ죬�������������ӣ��������������ӣ����ݼ�NaCl��Һ�����ˮ��ͬ����Ӧ���ʼ�������������ͭ��Һ�����û�ͭ����ͭ�γ�ԭ��أ��ӿ췴Ӧ���ʣ��������������٣��������������٣����������¶ȣ���Ӧ���ʼӿ죬�����������䣬��ȷ��������Ũ���������������ʵ������䣬���Է�Ӧ���ʼӿ죬�����������䣬��ȷ����ѡC��
�����Ѷȣ�һ��
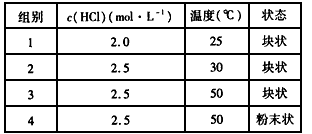
4��ѡ���� ����������������������ڲ�ͬ��ʵ�������½��з�Ӧ���ⶨ�ڲ�ͬʱ��t�����������V�����ݣ��������ݻ��Ƶõ���ͼ��ʾ���ߣ�������a��b��c��d����Ӧ��ʵ����������
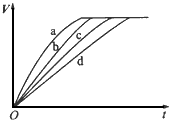 ? ? 
[? ]
A.4.3.2.1
B.1.2.3.4
C.3.4.2.1
D.1.2.4.3
�ο��𰸣�A
���������
�����Ѷȣ�һ��
5������� �ѳ�ȥ����Ĥ��þ��Ͷ�뵽ʢ��ϡ������Թ��У����������������ʵı仯�����ͼ��ʾ��
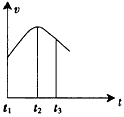
(1)�����������Т������Ũ�ȣ���þ���ı��������������ѹǿ����Cl-��Ũ�ȣ�Ӱ�췴Ӧ���ʵ�������__________������ţ���
(2) t1��t2���ʱ仯����Ҫԭ����________________��
(3)t2��t3���ʱ仯����Ҫԭ����_________________��
�ο��𰸣�(1)�٢�
(2)��Ӧ�����зų��������Է�Ӧ���ʵ�Ӱ���Ũ�Ƚ��͵�Ӱ����ܵķ�Ӧ��������
(3)Ũ�ȱ�С��Ũ�ȶԷ�Ӧ���ʵ�Ӱ���Ϊ��Ҫ���أ���ʹ��Ӧ���ʼ���
���������
�����Ѷȣ�һ��
|