1、选择题 下图是表示:2X(g) +Y(g)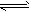 Z(g)+2R(g) △H<0的气体反应速率(υ)与时间(t)的关系,t1时开始改变条件,则所改变的条件符合曲线的是
Z(g)+2R(g) △H<0的气体反应速率(υ)与时间(t)的关系,t1时开始改变条件,则所改变的条件符合曲线的是
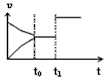
[? ]
A.减少Z物质
B.升高温度
C.加大压强
D.使用催化剂
2、选择题 影响化学反应速率的因素很多,下列措施肯定不能加快化学反应速率的是( )
A.降低温度
B.升高温度
C.使用催化剂
D.增加反应物浓度
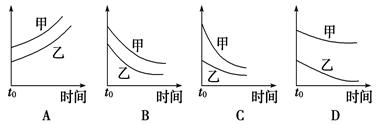
3、选择题 下列表格中的各种情况,可以用下面对应选项中的图象曲线表示的是
选项
| 反应
| 纵坐标
| 甲
| 乙
|
A
| 外形、大小相近的金属和水反应
| 反应速率
| Mg]
| Na
|
B
| 4 mL 0.01 mol/L的KMnO4溶液,分别和不同浓度的H2C2O4(草酸)溶液各2mL反应
| 0.1 mol/L的H2C2O4溶液
| 0.2 mol/L的H2C2O4溶液
|
C
| 5 mL 0.1 mol/L Na2S2O3溶液和5 mL 0.1 mol/L H2SO4溶液反应
| 热水
| 冷水
|
D
| 5 mL 4%的过氧化氢溶液分解放出O2
| 无MnO2粉末
| 加MnO2粉末
|
?
4、选择题 (9分)在2 L密闭容器内,800℃时反应2SO2(g)+O2(g) 2SO3(g)体系中,n(SO2)随时间的变化如下表:
2SO3(g)体系中,n(SO2)随时间的变化如下表:
时间(s)
| 0
| 1
| 2
| 3
| 4
| 5
|
n(SO2)(mol)
| 0.020
| 0. 010
| 0.008
| 0.007
| 0.007
| 0.007
|
(1)上述反应________(填“是”或“不是”)可逆反应,在第 5 s时,SO2的转化率为________;
(2)如图所示,表示SO3变化曲线的是_____,用O2表示从0 s~2 s内该反应的平均速率:v=__;
 ?
?
(3)能说明该反应已达到平衡状态的是________。
a.v(SO3)=2v(O2) b.混合气体中SO2的体积分数保持不变
c.v逆(SO2)=2v正(O2)? d.容器内密度保持不变
5、填空题 将1.0 mol X气体和1.0 mol Y气体混合于2 L的密闭容器中,发生反应2X(g)+Y(g) 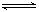 2Z(g)+2W(g),2min末,测得生成了0.4 mol W。
2Z(g)+2W(g),2min末,测得生成了0.4 mol W。
(1)前2min以X表示的平均反应速率为 ;
(2)下列叙述能说明该反应已达到化学平衡状态的是 。
A.单位时间里,消耗2 mol X,同时生成2 mol W
B.单位时间里,消耗2 mol X,同时也消耗了2 mol Z
C.反应混合物中各物质的浓度相等
D.反应混合物中各物质的浓度不再改变