1、填空题 (10分)如图表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨结构中的某一种的某一部分。
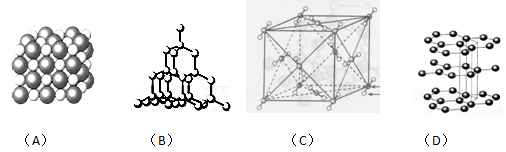
(1)其中代表金刚石的是(填编号字母,下同)?,金刚石属于?晶体。
(2)其中代表石墨的是?,其晶体中碳原子呈平面?结构排列。
(3)其中代表NaCl的是?,晶体中Na+与Cl-之间通过?键结合起来。
(4)代表干冰的是?,它属于?晶体,CO2分子间通过?结合起来。
(5)上述物质中前三种熔点由高到低的排列顺序为?。
参考答案:(1);B;原子?(2)D;层状?(3)A;离子键?
(4)C;分子;范德华力(或分子间作用力);
(5)(B)>(A)>(C)
本题解析:考查晶体的有关判断。只含分子的晶体是分子晶体。原子间以共价键相互结合,并向空间扩展,形成三维网状结构的晶体是原子晶体。阳离子和阴离子通过离子键结合而成的晶体是离子晶体。所以NaCl、CsCl、干冰、金刚石分别属于离子晶体、离子晶体、分子晶体和原子晶体。石墨属于混合型晶体,同一层内靠共价键结合,层和层之间靠分子间作用力结合。一般情况下原子晶体的熔点高于离子晶体的,离子晶体高于分子晶体的。
本题难度:一般
2、选择题 氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为
[? ]
A.NH3中氮原子为sp2杂化,而CH4中碳原子是sp3杂化
B.NH3中N原子形成三个杂化轨道,CH4中C原子形成4个杂化轨道
C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强
D.NH3分子中有三个σ键,而甲烷分子中有四个σ键
参考答案:C
本题解析:
本题难度:简单
3、选择题 NaCl的晶胞如图,每个NaCl晶胞中含有的Na+离子和Cl-离子的数目分别是
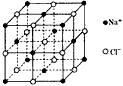
[? ]
A.14,13
B.1,1
C.4,4
D.6,6
参考答案:C
本题解析:
本题难度:一般
4、选择题 常见的离子晶体类型有5种,如右图是其中一种空间构型,则该晶体中x、y的离子个数之比可能为
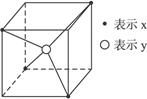
A.4∶1
B.2∶1
C.3∶1
D.1∶2
参考答案:D
本题解析:此晶体中独占的X个数为4×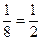 ,独占的Y为1,所以其离子个数之比为12∶1=1∶2。
,独占的Y为1,所以其离子个数之比为12∶1=1∶2。
本题难度:简单
5、选择题 下列物质固态时一定是分子晶体的是(?)
A.酸性氧化物
B.碱性氧化物
C.含氧酸
D.非金属单质
参考答案:C
本题解析:酸性氧化物在固态时可以是原子晶体,例如二氧化硅为原子晶体,故A错误;碱性氧化物在固态时一般是离子晶体,例如氧化钙、氧化钡,故B错误;含氧酸在固态时一定是分子晶体,故C正确;非金属单质在固态不一定为分子晶体,例如石墨为混合型晶体,B为原子晶体,故D错误。
点评:本题考查了分子晶体,属于对化学基本知识的考查,本题要掌握的是二氧化硅为酸性氧化物,但是其为原子晶体,本题难度中等。
本题难度:一般