1、填空题 雷尼镍(Raney-Ni)是一种历史悠久、应用广泛的催化剂,由镍-铝合金为原料制得。
(1)元素第一电离能:Al________Mg(选填:“>”、“<”、“=”)
(2)雷尼镍催化的一实例为: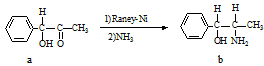
化合物b中进行sp3杂化的原子有:______________。
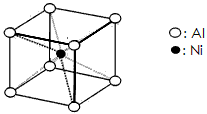
(3)一种铝镍合金的结构如下图,与其结构相似的化合物是:_________
(选填序号:a.氯化钠 b.氯化铯 c.石英 d.金刚石)。
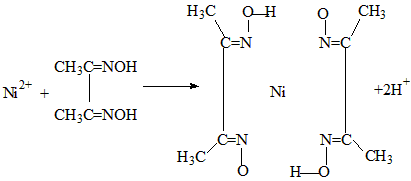
(4)实验室检验Ni2+可用丁二酮肟与之作用生成腥红色配合物沉淀。
①Ni2+在基态时,核外电子排布式为:______________。
②在配合物中用化学键和氢键标出未画出的作用力(镍的配位数为4)。
参考答案:(1)<
(2)C、N、O
(3)b
(4)①1s22s22p63s23p63d8或[Ar]3d8②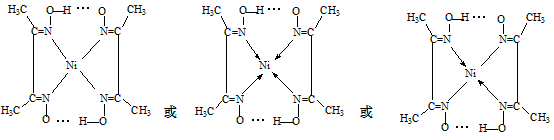
本题解析:
本题难度:一般
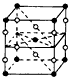
2、选择题 F2和Xe在一定条件下可以生成XeF2、XeF4和XeF6三种氟化氙,它们都是极强的氧化剂(其氧化性依次递增),都极易水解,其中:6XeF4+12H2O = 2XeO3+4Xe↑+24HF +3O2↑。下列推测正确的是
[? ]
A.XeF2分子中各原子均达到8电子稳定结构
B.某种氟化氙的晶体结构单元如上图,可推知其化学式为XeF6
C.XeF4按已知方式水解,每生成4 molXe,转移16 mol电子
D.XeF2加入水中,在水分子作用下将重新生成Xe和F2
参考答案:C
本题解析:
本题难度:一般
3、选择题 下列关于晶体的说法正确的组合是(? )
① 分子晶体中都存在共价键?
② 在晶体中只要有阳离子就一定有阴离子
③ 金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低?
④ 离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键?
⑤ 氯化钠熔化时离子键被破坏
⑥ SiO2晶体中每个硅原子与两个氧原子以共价键相结合?
⑦ 晶体中分子间作用力越大,分子越稳定?
A.①②③⑥? B.①②④? C.③⑤⑥? D.③⑤
参考答案:D
本题解析:略
本题难度:简单
4、选择题 有下列离子晶体空间结构示意图:●为阳离子M,○为阴离子N,化学式为M2N的晶体结构为(?)
A.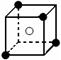
B.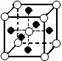
C.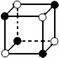
D.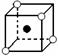
参考答案:D
本题解析:根据晶胞的结构并依据均摊法可知,A中阳离子和阴离子的个数分别是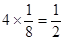 个和1个;B阳离子和阴离子的个数分别是
个和1个;B阳离子和阴离子的个数分别是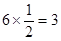 个和
个和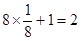 个;C中阳离子和阴离子的个数分别是
个;C中阳离子和阴离子的个数分别是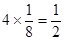 个和
个和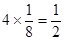 个;D阳离子和阴离子的个数分别是
个;D阳离子和阴离子的个数分别是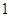 个和
个和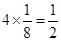 个,所以答案选D。
个,所以答案选D。
点评:该题是高考中的常见题型,属于基础性试题的考查,侧重对学生基础知识的巩固和训练,意在提高学生的应试能力。该题的关键是利用好均摊法,难度不大,有利于培养学生的逻辑推理能力和空间想象能力。
本题难度:一般
5、选择题 普通玻璃和水晶的根本区别在于
[? ]
A.外形不一样
B.普通玻璃的基本构成粒子无规则性地排列,水晶的基本构成粒子按一定规律作周期性的有序排列
C.水晶有固定的熔点,普通玻璃无固定的熔点
D.水晶可用于能量转换,普通玻璃不能用于能量转换
参考答案:B
本题解析:
本题难度:简单