1、简答题 36、1996年诺贝化学奖授予对发现C60有重大贡献的三位科学家.C60分子是形如球状的多面体(如图),该结构的建立基于以下考虑:
①C60分子中每个碳原子只跟相邻的3个碳原子形成化学键;
②C60分子只含有五边形和六边形;
③多面体的顶点数、面数和棱边数的关系,遵循欧拉定理:顶点数+面数-棱边数=2
据上所述,可推知C60分子有12个五边形和20个六边形,C60分子所含的双键数为请回答下列问题:
(1)固体C60与金刚石相比较,熔点较高者应是______,理由是:______.
(2)试估计C60跟F2在一定条件下,能否发生反应生成C60F60(填“可能”或“不可能”)______,并简述其理由:______.
(3)通过计算,确定C60分子所含单键数.?C60分子所含单键数为______.
(4)C70分子也已制得,它的分子结构模型可以与C60同样考虑而推知.通过计算确定C70分子中五边形和六边形的数目.
C70分子中所含五边形数为______,六边形数为______.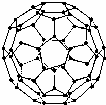
参考答案:解(1)金刚石属原子晶体,是空间立体网状结构;C60是分子晶体,为足球结构,所以金刚石的熔点大于C60.
故答案为:金刚石;金刚石属原子晶体,而固体C60不是,故金刚石熔点较高.
(2)该分子中含有碳碳单键和双键,双键能发生加成反应,所以可能.
故答案为:可能;因C60分子含30个双键,与极活泼的F2发生加成反应即可生成C60F60 .
(3)由欧拉定理计算键数(即棱边数):60+(12+20)-2=90
该分子中含双键30个,所以单键数为:C60分子中单键为:90-30=60
(4)设C70分子中五边形数为x,六边形数为y.依题意可得方程组:
本题解析:
本题难度:一般
2、选择题 下列判断正确的是?(? )
)
A.非金属氧化物一定是酸酐
B.酸酐一定是非金属氧化物
C.晶体中一定存在化学键
D.碱性氧化物一定是金属氧化物
参考答案:D
本题解析:略
本题难度:简单
3、选择题 下列关于晶体的说法一定正确的是(?)
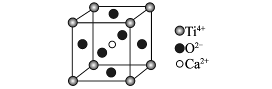
CaTiO3的晶体结构模型(图中Ca2+、O2-、
Ti4+分别位于立方体的体心、面心和顶点)
A.分子晶体中都存在共价键
B.CaTiO3晶体中每个Ti4+与12个O2-相邻
C.SiO2晶体中每个硅原子与两个氢原子以共价键相结合
D.金属晶体的熔点都比分子晶体的熔点高
参考答案:B
本题解析:有些单原子分子晶体中不存在共价键,如稀有气体构成的晶体,A错;因在晶体中Ti4+位于顶点而O2-位于面心,所以CaTiO3晶体中每个Ti4+与12个O2-相邻,B正确;SiO2晶体、Si原子与4个O原子以共价键结合,C错;金属晶体中有些比分子晶体的熔点低,如汞常温下为液体,D错。
本题难度:简单
4、选择题 下列叙述中正确的是
A.晶体与非晶体的根本区别在于是否具有规则的几何外形
B.晶体具有物理性质各向异性
C.晶体、非晶体均具有固定的熔点
D.由玻璃制成规则的玻璃球体现了晶体的自范性
参考答案:B
本题解析:A、晶体与非晶体的根本区别在于是构成固体的粒子在微观空间里是否呈现周期性的有序排列,A不正确;B、晶体具有物理性质各向异性,B正确;C、非晶体没有固定的熔点,C不正确;D、晶体的自范性指的是在适宜条件下,晶体能够自发地呈现封闭的规则的多面体外形的性质,这一适宜条件一般指的是自动结晶析出的。由玻璃制成规则的玻璃球是非晶体,不能体现晶体的自范性,D不正确,答案选A。
本题难度:简单
5、选择题 膦(PH3)又称为磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,它的分子呈三角锥形。以下有关
PH3的叙述正确的是
[? ]
A.PH3是非极性分子
B.PH3分子中磷原子上有一对有孤对电子
C.PH3是一种强氧化剂
D.PH3分子中P-H键是非极性键
参考答案:B
本题解析:
本题难度:一般