1、计算题 油画置于空气中,天长日久就会生成黑色的PbS从而使油画的色彩变暗,若用H2O2来“清洗”,则可使PbS转变为白色的PbSO4,从而使油画“复原”。?
(1)请写出“清洗”反应的化学方程式,此反应体现了H2O2的什么性质??
(2)若有0.100 mol的PbS参与反应,则在此反应中发生转移的电子的物质的量为_________mol。?
2、选择题 向某盐溶液中加入BaCl2溶液,再加入稀HNO3至溶液呈酸性,有白色沉淀产生,该溶液中可能有( )?
A.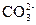
B.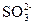
C.Ag+
D.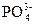 ?
?
3、选择题 下列实验能证明SO2存在的是(?)
①能使澄清的石灰水变浑浊 ②能使湿润的蓝色石蕊试纸变红 ③能使湿润的品红试纸褪色 ④通入足量的NaOH溶液,再加BaCl2溶液有白色沉淀生成 ,该沉淀溶于稀盐酸 ⑤通入氯水能使氯水褪色,再滴加BaCl2溶液有白色沉淀生成
A.都不能证明
B.③④⑤能证明
C.③⑤能证明
D.只有⑤能证明
4、实验题 分某同学为探究铜跟浓硫酸的反应情况,用下图所示装置进行了有关实验

(1)B是用来收集实验中生成的气体的装置,但未将导管画全,请在答题卷上把导管补充
完整?。
(2)请写出铜跟浓硫酸反应的化学方程式?。
(3)实验中D中的现象?。
(4)实验中,该同学取6.4g铜片和12mL 18mol・L-1H2SO4溶液放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余;该同学根据所学的化学知识判断还会有一定量H2SO4的剩余,下列药品中能够用来验证反应停止后的烧瓶中确有剩余的H2SO4的是?填字母编号)。
a.BaCl2溶液? b.Ba(NO3)2溶液? c.银粉? d.Na2CO3粉末
(5)若将16g铜与50mLH2SO4物质的量浓度为一定值的浓硫酸反应,铜完全溶解。请回答:
①反应中产生的气体在标准状况下的体积为?L。
②该反应中被还原的H2SO4的物质的量为?mol。
③待产生的气体全部释放后,向溶液中滴加VmL a mol・L-1NaOH溶液,恰好使溶液中?
的Cu2+全部转化为沉淀,则原浓硫酸中H2SO4的物质的量浓度=?mol・L-1。
5、选择题 在硫酸的工业制法中,下列生产操作与生产操作的主要原因
的说明都正确的是(?)
A.硫铁矿燃烧前需要粉碎,因为大块的硫铁矿不能燃烧
B.从沸腾炉出来的炉气需要净化,因为炉气中SO2会与杂质反应
C.SO2氧化为SO3时需要使用催化剂,这样可以提高SO2的转化率
D.用98.3%的浓硫酸吸收,目的是防止形成酸雾,以便使SO3吸收完全