1、选择题 已知硫酸溶液的质量分数越大时,其溶液的密度越大,将3x%与x%的两种硫酸溶液等体积混合后,溶液的质量分数(?)
A.大于2x%
B.小于2x%
C.等于2x%
D.无法确定
参考答案:A
本题解析:本题有两种解法。解法1:估算法。假设两种硫酸溶液等质量混合,混合后溶液的质量分数等于2x%。因为3x%溶液的密度大,所以等体积混合相当于等质量混合后又与少量的3x%溶液混合,混合后的溶液其质量分数必然大于2x%。本题答案为A。
解法2:设3x%的硫酸溶液密度为ρ1,x%的硫酸溶液的密度为ρ2,两者体积均为V mL,则混合后溶液的质量分数为:
a%= =
=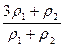 ×x%
×x%
因为ρ1>ρ2,所以ρ1+ρ2>2ρ2
故2ρ1+ρ1+ρ2>2ρ2+2ρ1
即3ρ1+ρ2>2(ρ1+ρ2)
a%>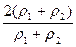 ・x%=2x%
・x%=2x%
本题的正确选项为A。
本题难度:简单
2、选择题 在通常情况下能大量共存,并且可以用浓硫酸干燥的一组气体是?( )
A.SO2 .H2S、O2
B.CO、H2、Cl2
C.NO、H2、O2
D.HCl、CO、NH3
参考答案:B
本题解析:略
本题难度:一般
3、选择题 将SO2和X气体分别通入BaCl2溶液,未见沉淀生成,若同时通入,有沉淀生成,则X气体不可能是?
A.CO2
B.NH3
C.C12
D.H2S
参考答案:A
本题解析:A 、SO2和CO2的原理是类似的,都因为违背强酸制弱酸的原则而不能反应.因此不能生成沉淀.
B、中通入氨气后,和SO2反应生成亚硫酸铵,之后发生复分解反应生成亚硫酸钡沉淀.
C、氯气将亚硫酸根氧化成硫酸根,所以会有沉淀.
D、硫酸氢和二氧化硫反应生成硫沉淀.
点评:本题属于简单题,掌握弱酸不能制强酸是解题的关键。
本题难度:一般
4、实验题 (6分)下图为浓硫酸与铜反应的实验装置图。

(1)浓硫酸与铜反应的化学方程式为??。
(2)实验中,当产生的气体进入盛有品红溶液的仪器b中时,品红溶液将?,原因是?。
参考答案:(6分)Cu + 2H2SO4(浓) ?CuSO4 +SO2 ↑+2H2O,褪色,SO2具有漂白性。
?CuSO4 +SO2 ↑+2H2O,褪色,SO2具有漂白性。
本题解析:浓硫酸具有强氧化性,可将铜氧化为硫酸铜,而部分硫酸被还原为二氧化硫:Cu + 2H2SO4(浓) ?CuSO4 +SO2 ↑+2H2O;
?CuSO4 +SO2 ↑+2H2O;
由于二氧化硫具有漂白性,可与品红结合生成无色化合物,故可使品红试液褪色。
本题难度:一般
5、选择题 研究发现,空气中少量的NO2能参与硫酸型酸雨的形成,反应过程如下:
①SO2+NO2→SO3+NO?②SO3+H2O→H2SO4?③2NO+O2→2NO2
NO2在上述过程中的作用,与H2SO4在下列变化中的作用相似的是(?)
A.加入少量H2SO4使淀粉水解
B.碳酸钠与硫酸反应
C.向铜和双氧水的混合物中加入硫酸
D.潮湿的氯气通过盛有浓H2SO4的洗气瓶
参考答案:A
本题解析:略
本题难度:一般