1、选择题 下列说法错误的是(?)
A.蒸发和蒸馏都是利用了混合物各组分沸点的不同
B.食盐水的蒸发和自来水的蒸馏都能用到的仪器有铁架台、酒精灯、石棉网等
C.分液时,将分液漏斗上口的玻璃塞打开的目的是为了平衡分液漏斗内外的气压,便于液体流下
D.过滤时玻璃棒靠在三层滤纸一边
参考答案:B
本题解析:略
本题难度:简单
2、实验题 (8分)实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH+6HCHO===3H++6H2O+(CH2)6N4H+[滴定时,1 mol(CH2)6N4H+与1 mol H+相当,也消耗1 mol OH-],然后用NaOH标准溶液滴定反应生成的酸。某兴趣小组用甲醛法进行了如下实验:步骤Ⅰ 称取样品1.500 g。
步骤Ⅱ 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤Ⅲ 移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。(1)根据步骤Ⅲ填空:
①用NaOH标准溶液滴定滴定锥形瓶中溶液时,左手控制?式滴定管,右手摇动锥形瓶,眼睛注视______________?_。直到因加入一滴NaOH溶液后,溶液由无色变为红色,并且______________?为止
②碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数________(填“偏高”、“偏低”或“无影响”)。
③移取25.00 mL样品的滴定管,移取前尖嘴处有气泡,移取后气泡消失,则滴定时用去NaOH标准溶液的体积? (填“偏大”、“偏小”或“无影响”)
(填“偏大”、“偏小”或“无影响”)
(2)滴定结果如下表所示:
滴定次数
| 待测溶液的体积/mL
| 标准溶液的体积/mL
|
滴定前刻度
| 滴定后刻度
|
第一次
| 25.00
| 1.02
| 20.99
|
第二次
| 25.00
| 2.00
| 22.03
|
第三次
| 25.00
| 0.00
| 22.00
|
若NaOH标准溶液的浓度为0.1010 mol/L,则该样品中氮的质量分数为________。
参考答案:
本题解析:略
本题难度:一般
3、实验题 已知SO2、SiO2、CO2等氧化物化学物质具有一定的相似性。用下图所示装置进行Mg与SO2反应的实验。

(1)选择制取SO2的合适试剂?(填编号);
①20%的HNO3溶液②80%的H2SO4溶液③Na2SO3固体④CaSO3固体
(2)在方框中画出B的装置图并注明试剂;
(3)实验后对C装置玻璃管中的固体成分进行分析,未检测到单质硫,则Mg与SO2反应的产物除MgO外另一种是?(填化学式),请用实验加以证明?。
参考答案:( 1)②③(2分)(2)
1)②③(2分)(2)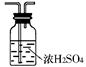 (2分,其它合理答案也给分)
(2分,其它合理答案也给分)
(3)MgS(2分);取少量固体于试管中,加入稀硫酸,放出有臭鸡蛋气味的气体(2分,其它合理答案也给分)
本题解析:略
本题难度:一般
4、选择题 为探究一溴环己烷( )与NaOH的醇溶液共热发生的是水解反应还是消去反应,甲、乙、丙三位同学分别设计如下三个实验方案:甲:向反应混合液中滴入稀硝酸中和NaOH,然后再滴入AgNO3溶液,若有浅黄色沉淀生成则可证明发生了消去反应。乙:向反应混合液中滴入溴水,若溶液颜色很快褪去,则可证明发生了消去反应。丙:向反应混合液中滴入酸性KMnO4溶液,若溶液颜色变浅,则可证明发生了消去反应。其中正确的是
)与NaOH的醇溶液共热发生的是水解反应还是消去反应,甲、乙、丙三位同学分别设计如下三个实验方案:甲:向反应混合液中滴入稀硝酸中和NaOH,然后再滴入AgNO3溶液,若有浅黄色沉淀生成则可证明发生了消去反应。乙:向反应混合液中滴入溴水,若溶液颜色很快褪去,则可证明发生了消去反应。丙:向反应混合液中滴入酸性KMnO4溶液,若溶液颜色变浅,则可证明发生了消去反应。其中正确的是
[? ]
A.甲
B.乙
C.丙
D.上述实验方案都不正确
参考答案:D
本题解析:
本题难度:简单
5、实验题 某探究小组用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素。实验条件作如下限定:所用KMnO4酸性溶液的浓度可选择0.01 mol?L-1、0.001 mol?L-1,?催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K。每次实验KMnO4酸性溶液的用量均为4 mL、H2C2O4溶液(0.1 mol?L-1)的用量均为2mL。
(1)配平化学方程式:
______KMnO4 +____H2C2O4 +_____H2SO4 → ____K2SO4 +_____MnSO4 +_____CO2 +______H2O
(2)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
实验编号
| T/K
| 催化剂的用量/ g
| KMnO4酸性溶液的浓度/mol?L-1
| 实验目的
|
①
| 298
| 0.5
| 0.01
| (Ⅰ)实验①和②探究KMnO4酸性溶液的浓度对该反应速率的影响;
(Ⅱ)实验①和③探究温度对该反应速率的影响;
(Ⅲ)实验①和______探究催化剂对该反应速率的影响
|
②
| ?
| ?
| ?
|
③
| ?
| ?
| ?
|
④
| ?
| 0
| ?
|
(3)在完成探究催化剂对该反应速率影响的实验时发现,未加催化剂的情况下,刚开始一段时间,反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快。
针对上述实验现象,同学认为高锰酸钾与草酸溶液的反应放热,导致溶液温度升高,反应速率加快,从影响化学反应速率的因素看,你猜想还可能是________________
若用实验证明你的猜想。除酸性高锰酸钾溶液,草酸溶液外,还需要选择的试剂最合理的是_______
A.硫酸钾? B.硫酸锰? C.二氧化锰? D.水
(4)某同学对实验①和②分别进行三次实验,测得以下实验数据(从混合振荡均匀开始计时):
KMnO4酸性溶液
的浓度?/?mol?L-1
| 溶液褪色所需时间?t / min
|
第1次
| 第2次
| 第3次
|
0.01
| 14
| 13
| 11
|
0.001
| 6
| 7
| 7
|
计算用0.001?mol?L-1?KMnO4酸性溶液进行实验时KMnO4的平均反应速率?(忽略混合前后溶液体积的变化)。
(4)?若不经过计算,直接看表中的褪色时间长短来判断浓度大小与反应速率的关系是否可行?_________。若不可行(若认为可行则不填),请设计可以通过直接观察褪色时间长短来判断的改进方案_____________________________________
参考答案:(11分)(1) 配平化学方程式:(2分,全对才给分)
2KMnO4 +5H2C2O4 +3H2SO4 → 1K2SO4 +2MnSO4 +10CO2 +8H2O
(1)?请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:(每一行1分,共3分)
实验编号
T/K
催化剂的用量/ g
KMnO4酸性溶液的浓度/mol?L-1
实验目的
①
298
0.5
0.01
(Ⅰ)实验①和②探究KMnO4酸性溶液的浓度对该反应速率的影响;
(Ⅱ)实验①和③探究温度对该反应速率的影响;
(Ⅲ)实验①和④探究催化剂对该反应速率的影响
②
298
0.5
0.001
③
323
0.5
0.01
④
298
0
0.01
(3)生成的Mn2+催化反应的进行(1分),B(1分)
(4)1×10-4mol/L.min (1分)?
(5)不可行(1分)。取过量的体积相同、浓度不同的草酸溶液分别同时与体积相同、浓度相同的KMnO4溶液反应(2分)
本题解析:(1)在酸性条件下,高锰酸根离子能和草酸发生氧化还原反应生成二价锰离子、二氧化碳和水,根据电子的得失守恒可知,离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。
(2)要得出反应物浓度、温度、催化剂对反应速率影响的结论至少要完成:①取不同浓度KMnO4溶液,在相同温度下进行反应;②取同浓度KMnO4溶液,在不同温度下进行反应;③取同浓度KMnO4溶溶,在同温度且有催化剂的条件下进行反应;④取同浓度KMnO4溶液,在同温度且不使用催化剂的条件下进行反应等3个实验来进行对比。
(3)根据反应的方程式可知,生成物中有Mn2+生成,这说明引起反应速率加快的原因还可能是生成的Mn2+催化反应的进行,据此可知,如果要验证假设,则可以选择试剂硫酸锰,答案选B。
(4)①反应开始时:c(KMnO4)= ,反应时间:△t=(6min+7min+7min)÷3=6.7min,所以KMnO4的平均反应速率ν(KMnO4)=
,反应时间:△t=(6min+7min+7min)÷3=6.7min,所以KMnO4的平均反应速率ν(KMnO4)= 。
。
②由题中数据知浓度大的褪色时间反而长,因颜色是由KMnO4产生,虽然KMnO4浓度大反应快,但KMnO4的量也多,故无法比较,故不经过计算直接利用表中的褪色时间长短来判断浓度大小与反应速率的关系是不可行的;所以若想通过直接观察褪色时间长短来判断溶液浓度的大小,则必须保证KMnO4酸性溶液的浓度相同,才能判断H2C2O4溶液浓度的大小,即取过量的体积相同、浓度不同的草酸溶液分别同时与体积相同、浓度相同的高锰酸钾酸性溶液反应。
点评:该题是高考中的常见题型,所以中等难度的试题。试题综合性强,侧重对学生能力的培养和胶体方法的指导与训练,有利于培养学生规范、严谨的实验设计、评价能力,有利于提高学生的学科素养。该类试题综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。
本题难度:一般