1��ѡ���� ���ڳ��������еķ�Ӧ��Zn(s)+H2SO4(aq)= ZnSO4 (aq)+H2(g),���������в���ȷ����
A��Zn��H2SO4������������ ZnSO4��H2��������
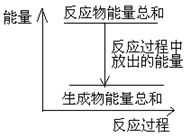
B����Ӧ������������ϵ������ͼ��ʾ
C�������÷�Ӧ��Ƴ�ԭ��أ���ZnΪ����
D�������÷�Ӧ��Ƴ�ԭ��أ�����65gп�ܽ�ʱ�������ų�11.2L����
�ο��𰸣�D
���������
����������û���Ӧ�Ƿ��ȷ�Ӧ������Ӧ�������ܺʹ��������������ܺͣ�A�ԣ�ͼ��Ҳ��ӳ����Ӧ����������������ߣ�����BҲ�ԣ���ԭ����л�ԭ���������������Բ��ϣ�ʧ���ӱ�����������C�ԣ�Zn?-?2e-?=?Zn2+������32.5g�������ʵ���Ϊ0.5mol��п�ܽ�ʱ����������2H+?+?2e-?=?H2��������0.5molH2������ڱ�״����Ϊ11.2L������Ŀδ˵�����ڱ�״���£�����D���ԣ�ѡD��
�����Ѷȣ�һ��
2��ѡ���� ��֪��H2O(g)===H2O(l)��?��H����Q1 kJ��mol��1
C2H5OH(g)===C2H5OH(l)��?��H����Q2 kJ��mol��1
C2H5OH(g)��3O2(g)===2CO2(g)��3H2O(g)?��H����Q3 kJ��mol��1
��ʹ46 gҺ̬�ƾ���ȫȼ�գ����ָ������£���ų�������Ϊ(����)
A��(Q1��Q2��Q3) kJ
B��(Q2��3Q1��Q3) kJ
C��(0.5Q1��1.5Q2��0.5Q3) kJ
D��(3Q1��Q2��Q3) kJ
�ο��𰸣�D
������������ݸ�˹���ɿ�֪������H2O(g)===H2O(l)����C2H5OH(g)===C2H5OH(l)�͢�C2H5OH(g)��3O2(g)===2CO2(g)��3H2O(g)���ӣ����١�3���ۣ��ڵõ�C2H5OH(l)��3O2(g)===2CO2(g)��3H2O(l)�����ԡ�H����(3Q1��Q2��Q3) kJ /mol��46gҺ̬�ƾ���1mol�����Դ���D��
�����Ѷȣ���
3��ѡ���� ������ͼ�������仯ʾ��ͼ������ѡ����ȷ����
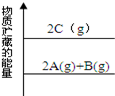
A��2A+B�T2C����H��O
B��2C�T2A+B����H��0
C��2A(g��+B(g���T2C(g����H��0
D��2A(g��+B(g���T2C(g����H��0
�ο��𰸣�C
���������A��B�������ʵľۼ�״̬������C����Ӧ������������������������������Ӧ����Ϊ���ȣ���ȷ��D������ѡC��
�����Ѷȣ���
4��ѡ���� �������ӷ���ʽ��ȷ����(? )
A��̼�������Һ����������������Һ��Ӧ��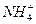 +OH-====NH3��H2O
+OH-====NH3��H2O
B��Fe(OH)3���������Һ��ϣ�Fe(OH)3+3H+====Fe3++3H2O
C����⾫��ͭ��������Ӧ�ǣ�Cu2++2e-====Cu
D��1 mol��L-1��NaAlO2��Һ��2.5 mol��L-1��HCl�����������Ȼ�ϣ�2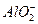 +5H+====Al(OH)3��+Al3++H2O
+5H+====Al(OH)3��+Al3++H2O
�ο��𰸣�CD
���������A���У�NaOH������Ӧ�ų�NH3��A�����B���У�Fe3+��I-���ܹ��档C����ȷ��D������HCl�������ʲ�����Al(OH)3��Ҳ��Al3+����ȷ��
�����Ѷȣ���
5��ѡ���� �����뻯ѧ��Ӧ�����仯��ص�������ȷ����
A������������һ�����ڷ�Ӧ��������
B����ͬ�����£�2mol��ԭ�������е�����С��1mol����������е�����
C�����ݸ�˹���ɣ��ɼ���ijЩ����ֱ�Ӳⶨ�Ļ�ѧ��Ӧ�ķ�Ӧ�ʱ�
D��ͬ��ͬѹ�£�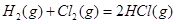 �ڹ��պ͵�ȼ������
�ڹ��պ͵�ȼ������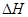 ��ͬ
��ͬ
�ο��𰸣�C
���������A������ѧ��Ӧ�Ļ������������µ����ʲ�����ͬʱ�����������ı仯���������ı仯ͨ������������ʽ���ֳ����������ȷ�Ӧ���з��ȷ�Ӧ�����ԣ��������������ܵ��ڷ�Ӧ��������Ҳ���ܸ��ڷ�Ӧ�����������B�������ӻ���Ϊԭ��ʱҪ������������Ӧ֮ԭ�ӽ�ϳɷ���ʱҪ�ͷ�������������ͬ�����£�2mol��ԭ�������е���������1mol����������е�������C��ȷ��D����ͬ��ͬѹ�£�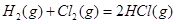 �ڹ��պ͵�ȼ������
�ڹ��պ͵�ȼ������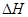 ��ͬ��ͬһ��ѧ��Ӧ�ķ�Ӧ����һ���̶���ֵ��
��ͬ��ͬһ��ѧ��Ӧ�ķ�Ӧ����һ���̶���ֵ��
�����Ѷȣ���