1、选择题 下列说法正确的是(?)
A.有能量变化的物质变化都是化学变化
B.不同形式的能量转化一定是化学变化
C.化学反应中的能量变化都是热量变化
D.物质发生化学变化一定伴随能量变化
参考答案:D
本题解析:物理变化过程中也会伴随能量的变化,A不正确;B不正确,例如太阳能转化为电能等;化学反应中的能量变化不一定都是热量变化,例如化学能也可以转化为电能,C不正确,所以正确的答案选D。
点评:该题是基础性试题的考查,侧重对学生基础知识的巩固和训练,意在培养学生灵活运用基础知识解决实际问题的能力,难度不大。
本题难度:一般
2、选择题 根据下图所示图像,写出反应的热化学方程式并回答下列问题:
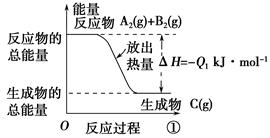
(1)反应过程①的热化学方程式为:____________________________________________。
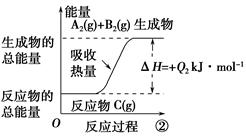
(2)反应过程②的热化学方程式为:____________________________________________。
(3)Q2与Q1的关系:Q2________Q1(填“大于”“小于”或“等于”)。
参考答案:(1)A2(g)+B2(g)=C(g) ΔH=-Q1 kJ・mol-1
(2)C(g)=A2(g)+B2(g) ΔH=+Q2kJ・mol-1 (3)等于
本题解析:本题考查的是热化学方程式的书写。图中已清楚地标明两个反应的反应物、生成物和反应热,按照书写热化学方程式的规则,不难写出相应的热化学方程式。因为两个反应方向相反,因此其反应热数值的绝对值相等,符号相反。
本题难度:一般
3、计算题 高炉炼铁是冶炼铁的主要方法。
(1)从炼铁高炉口排出的尾气中含有一定量的有毒气体?(填化学式),会污染空气。100多年前,人们曾耗巨资改建高炉,结果尾气中的该物质含量并未减少。高炉炼铁的主要反应方程式为(设铁矿石用磁铁矿)?。
(2)已知:①4Fe(s) + 3O2=2Fe2O3(s) ?ΔH1
②4Fe3O4(s)+O2(g)=6Fe2O3(s)?ΔH2?
③3Fe(s)+2O2(g)=Fe3O4(s)?ΔH3?
则ΔH2= (用含上述ΔH的代数式表示)。
(3)高铁酸钠(Na2FeO4)是铁的一种重要化合物,可用电解法制备,阳极材料为铁,其电解质溶液应选用_______ (填H2SO4、HNO3、KOH、NaOH、Na2SO4)溶液,原因是_____________,阳极反应式为_________________。
(4)某温度下,HX的电离平衡常数K为1×10-5。计算该温度下0.100mol/L的HX溶液的? H+浓度。(平衡时HX的浓度以0.100mol/L计,水的电离忽略不计,写出计算过程。)
参考答案:(16分)
(1)CO(2分)? Fe3O4(s)+4CO(g)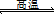 3Fe(s)+4CO2(g) (写等号扣1分,不标状态不扣分)(2分)
3Fe(s)+4CO2(g) (写等号扣1分,不标状态不扣分)(2分)
(2)3ΔH1-4ΔH3?(2分)?
(3)NaOH(2分)?酸性条件会反应,KOH会引进K元素杂质(合理也给分)(2分)
Fe-6e-+ 8OH-= FeO42-+ 4H2O (2分)
(4) ?HX? ?X-?+? H+
?X-?+? H+
初始浓度/ mol・L-1: 0.100? 0? 0
变化浓度/ mol・L-1:? a?a? a
平衡浓度/ mol・L-1: 0.100? a? a?(1分)
K= 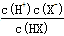 =
=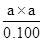 =1×10-5?∴a≈1×10-3(1+1+1分)
=1×10-5?∴a≈1×10-3(1+1+1分)
(K的表达式正确得1分,算式正确得1分,计算结果正确得1分)。
本题解析:(1)高炉炼铁原理为Fe2O3+3CO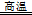 2Fe+3CO2,为了提高氧化铁的利用率及,一氧化碳一定过量,则尾气中含有的有毒气体是CO;产生上述现象的原因是高炉炼铁是可逆反应,则用磁铁矿为原料炼铁的原理为Fe3O4(s)+4CO(g)
2Fe+3CO2,为了提高氧化铁的利用率及,一氧化碳一定过量,则尾气中含有的有毒气体是CO;产生上述现象的原因是高炉炼铁是可逆反应,则用磁铁矿为原料炼铁的原理为Fe3O4(s)+4CO(g)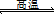 3Fe(s)+4CO2(g);(2)为了约去Fe(s),观察3个热化学方程式,发现①×3―③×4=②,则②的焓变等于①的焓变×3―③的焓变×4,即ΔH2=3ΔH1-4ΔH3;(3)阳极的主要反应物和产物是铁和高铁酸根离子,即Fe→FeO42―;铁元素由0价升为+6价,升高总数为6,则失去6个电子,则Fe―6e―→FeO42―;由于铁单质与酸能直接反应,因此不能选择酸作电解质溶液,也不能用氢离子使左右电荷守恒,只能选碱作电解质溶液,但不能选择KOH,否则引入钾离子等杂质,根据电荷守恒,则Fe―6e―+ 8OH-→FeO42―;根据氢、氧原子个数守恒,则阳极反应式为Fe-6e-+ 8OH-= FeO42-+ 4H2O;(4)依题意,该反应体系中各组分(起始、变化、平衡)浓度可以推导,则
3Fe(s)+4CO2(g);(2)为了约去Fe(s),观察3个热化学方程式,发现①×3―③×4=②,则②的焓变等于①的焓变×3―③的焓变×4,即ΔH2=3ΔH1-4ΔH3;(3)阳极的主要反应物和产物是铁和高铁酸根离子,即Fe→FeO42―;铁元素由0价升为+6价,升高总数为6,则失去6个电子,则Fe―6e―→FeO42―;由于铁单质与酸能直接反应,因此不能选择酸作电解质溶液,也不能用氢离子使左右电荷守恒,只能选碱作电解质溶液,但不能选择KOH,否则引入钾离子等杂质,根据电荷守恒,则Fe―6e―+ 8OH-→FeO42―;根据氢、氧原子个数守恒,则阳极反应式为Fe-6e-+ 8OH-= FeO42-+ 4H2O;(4)依题意,该反应体系中各组分(起始、变化、平衡)浓度可以推导,则
HX? ?X-?+? H+
?X-?+? H+
初始浓度/ mol・L-1? 0.100? 0? 0
变化浓度/ mol・L-1?a?a? a
平衡浓度/ mol・L-1?0.100―a≈0.100? a?a
K= 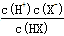 =
=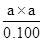 =1×10-5?∴a≈1×10-3
=1×10-5?∴a≈1×10-3
本题难度:简单
4、填空题 能源是人类生存和发展的重要支柱。研究和有效地开发新能源在能源紧缺的今天具有重要的理论意义。
(1)已知下列热化学方程式:
① H2(g)+1/2O2(g) =H2O(g)?ΔH=-241.8 kJ/mol?
② C(s)+1/2O2(g) =CO(g)?ΔH=-110.5 kJ/moL?
则水煤气能源的制取原理:C(s)+H2O(g)=H2(g)+CO (g)?ΔH=?kJ/moL
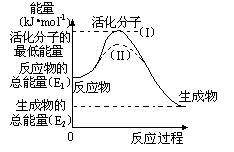
(2)研究活化能对于能源技术的革新有非常重大的实际意义。请认真观察下图,回答问题:
① 图中反应的ΔH=?kJ/mol(用含有E1、E2代数式表示)。
② 已知热化学 方程式:H2(g)+1/2O2(g) =?H2O(g)?ΔH=-
方程式:H2(g)+1/2O2(g) =?H2O(g)?ΔH=- 241.8 kJ/mol,该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为?kJ/mol。
241.8 kJ/mol,该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为?kJ/mol。
③ 图中虚线(II)与实线(I) 对于同一反应具有的意义:
??。
参考答案:(1)+131.3
(2)① ―(E1- E2)或(E2-E1)
② 409?
③ 降低反应所需的活化能,增大单位体积内活化分子的百分 数,提高反应
数,提高反应 速率。
速率。
本题解析:略
本题难度:简单
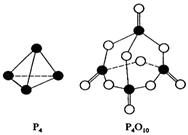
5、选择题 白磷与氧可发生如下反应:P4 + 5O2 = P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P:a kJ・mol-1、P-O:b kJ・mol-1、P=O:c kJ・mol-1、O=O:d kJ・mol-1。根据图示的分子结构和有关数据估算该反应的△H,其中正确的是
A.(6a+5d-4c-12b)kJ・mol-1
B.(4c+12b-6a-5d)kJ・mol-1
C.(4c+12b-4a-5d)kJ・mol-1
D.(4a+5d-4c-12b)kJ・mol-1
参考答案:A
本题解析:各化学键键能为P-P a kJ?mol-1、P-O b kJ?mol-1、P="O" c kJ?mol-1、O="O" d kJ?mol-1.
反应热△H=反应物总键能-生成物总键能,
所以反应P4+5O2=P4O10的反应热△H=6akJ?mol-1+5dkJ?mol-1-(4ckJ?mol-1+12bkJ?mol-1)=(6a+5d-4c-12b)kJ?mol-1,
故选:A。
点评:考查反应热与化学键键能的关系,难度中等,注意从物质能量、键能理解反应热。
本题难度:简单