1、选择题 实验室制取下列气体,其反应放热的是(?)
A.氯化铵和氢氧化钙制氨气
B.由乙醇制C2H4
C.由电石制C2H2
D.由氯酸钾制O2
参考答案:C
本题解析:略
本题难度:简单
2、选择题 已知热化学方程式:2SO2(g)+O2=2SO3(g),△H=-197kJ/mol。在相同温度和压强下,向密闭容器中通入2mol SO2和1molO2,达到平衡时放出热量Q,则下列关系式中正确的是
A.Q=197 kJ
B.Q<197×2 kJ
C.Q<197 kJ
D.Q>197 kJ
参考答案:C
本题解析:由于该反应是可逆反应,所以2mol SO2和1molO2不可能生成2mol三氧化硫,所以实际放出的热量小于197kJ,答案选C。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,主要是考查学生对反应热概念的熟悉掌握程度,有利于培养学生的逻辑推理能力。该题的关键是明确热化学方程式的含义,然后结合题意灵活运用即可。
本题难度:一般
3、选择题 下列物质加入水中,显著放热的是 ( )
A.固体NaCl
B.生石灰
C.无水乙醇
D.固体NH4NO3
参考答案:B
本题解析:生石灰溶于水生成氢氧化钙,放出大量的热,AC热效应不明显,D是吸热过程,答案选B。
本题难度:简单
4、选择题 反应A+B→C分两步进行:①A+B→X,②X→C,反应过程中能量变化如下图所示,E1表示反应A+B→X的活化能。 下列有关叙述正确的是

A.E2表示反应X→C的活化能
B.反应A+B→C的△H<0
C.X是反应A+B→C的催化剂
D.加入催化剂可改变反应A+B→C的焓变
参考答案:B
本题解析:A、E2表示反应X→C中活化分子变成生成物时放出的能量,而不能表示活化能,A不正确;B、关键图像可知,反应物A和B的总能量高于生成物C的总能量,因此反应A+B→C的△H<0,B正确;C、X是反应A+B→C的中间产物,而表示催化剂,C不正确;D、催化剂只能改变活化能,但不能改变焓变,D不正确,答案选B。
本题难度:一般
5、选择题 某可逆反应过程能量变化如图所示,下列说法中正确的是? ( )
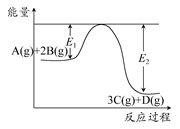
A.该反应热化学方程式为A(g)+2B(g)  3C(g)+D(g) ΔH>0
3C(g)+D(g) ΔH>0
B.其他条件不变,升高温度,A的转化率增大
C.其他条件不变,增大压强,释放热量减少,平衡常数K减小
D.其他条件不变,加催化剂,反应速率增大,E1和E2均减小,ΔH不变
参考答案:D
本题解析:由于E2>E1,则ΔH<0,A错误;对于放热反应,升高温度,平衡逆向移动,A的转化率减小,B错误;K只与温度有关,增大压强,K不变,C错误;催化剂能降低E1,E2也相应减小,v增大,但ΔH不变。
本题难度:一般