1��ѡ���� ����ϡ�����ڳ��������н��з�Ӧ��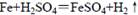 �����������в���ȷ����
�����������в���ȷ����
A���÷�Ӧ�ķ�Ӧ������������ϵ��������ͼ��ʾ

B�������÷�Ӧ��Ƴ�ԭ��أ�����������22��4L����ʱ����56g���ܽ�
C�������÷�Ӧ��Ƴ�ԭ��أ���Һ��SO42-��Fe�缫�ƶ�
D�������÷�Ӧ��Ƴ�ԭ��أ����������ķ�Ӧ�ǣ�Fe -2e =Fe2+
�ο��𰸣�B
��������� A��������ϡ�����Ƿ��ȷ�Ӧ����ȷ��B����56g���ܽ⣬����������״����22��4L���壬����C��ԭ����У���������������ȷ��D�����������������ķ�Ӧ�ǣ�Fe -2e =Fe2+����ȷ��
�����Ѷȣ�һ��
2��ѡ���� Ϊ�����úȼ�յ���Ч�ʲ�����SO2���̳��Դ�������Ⱦ�����˲�ȡ�Ĵ�ʩ��(? )
A��ͨ������Ŀ���
B����ú������ú��
C����ú�Ƴɶ��ú��
D����ú����������ת��Ϊ����ȼ��
�ο��𰸣�BD
�������������ú������������ĽӴ��棬ȼ�ջ����֡�
�����Ѷȣ���
3��ʵ���� ������ͼ��ʾװ�òⶨ�к��ȵ�ʵ�鲽�����£�
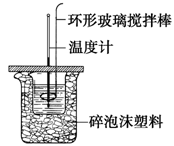
����һ������Ͳ��ȡ50ml 0.50 mol?L��1���ᵹ��С�ձ��У���������¶�t1��
�����������һ��Ͳ��ȡ50ml 0.55 mol?L��1 NaOH��Һ��������һ�¶ȼƲ�����¶�t2��
����������NaOH��Һ����С�ձ��У��跨ʹ֮��Ͼ��ȣ���û��Һ����¶�t3��
�ش��������⣺
��1���������е���NaOH��Һ����ȷ������__________��
A���ز�������������? B����������������? C��һ��Ѹ�ٵ���
��2��ʹ������NaOH��Һ��Ͼ��ȵ���ȷ������________������ţ���
A����������ձ�? B���ҿ�ӲֽƬ�ò���������
C�����¶ȼ�С�Ľ���?D���������¶ȼ��ϵĻ��β������������ؽ���
��3��___________����ܡ����ܡ�����Ba��OH��2��Һ���������NaOH��Һ��������к��ȣ�������________________________________________��
��4���ڷ�Ӧ������Ϊ�з��������������HCl�ڷ�Ӧ�лӷ������õ��к���_______���ƫ����ƫС�����䡱����
�ο��𰸣���1��C?��2��D
��3������, ��Ϊ������Ba��OH��2��Һ��Ӧ����BaSO4�����������Ȼ�Ӱ�췴Ӧ�ķ�Ӧ�ȡ���4�� ƫС
�����������1�����к��ȵIJⶨʵ���У������������ƵĴ���Խ�࣬��ʧ������Խ�ࡣ��˲������е���NaOH��Һ����ȷ������һ��Ѹ�ٵ��룬��ѡC��
��2��A����������ձ�����ʹҺ�彦����A����ȷ��B���ҿ�ӲֽƬ�ò�������������ʹ������ʧ��B����ȷ��C���¶ȼ�ֻ�ܲ����¶ȣ������������裬C����ȷ��D���������¶ȼ��ϵĻ��β������������ؽ���������ȷ�IJ�����D��ȷ����ѡD��
��3������������Ba��OH��2��Һ��Ӧ����BaSO4�����������Ȼ�Ӱ�췴Ӧ�ķ�Ӧ�ȣ����Բ�����Ba��OH��2��Һ���������NaOH��Һ��������к��ȡ�
��4���ڷ�Ӧ������Ϊ�з��������������HCl�ڷ�Ӧ�лӷ��������������٣���˲�õ��к���ƫС��
�����Ѷȣ�һ��
4��ѡ���� ��֪��Ӧ����101kPaʱ��2C��s��+O2��g���T2CO��g����H=-221kJ/mol
��ϡ��Һ�У�H+��aq��+OH-��aq���TH2O��l����H=-57.3kJ/mol��
���н�����ȷ���ǣ�������
A��̼��ȼ����С��110.5kJ/mol
B���ٵķ�Ӧ��Ϊ221kJ/mol
C��ϡ������ϡNaOH��Һ��Ӧ���к���Ϊ-57.3kJ/mol
D��ϡ������ϡNaOH��Һ��Ӧ����1molˮ���ų�������С��57.3kJ
�ο��𰸣�A���ɷ�Ӧ�ٿ�֪��1mol̼ȼ������CO�ų�������Ϊ110.5 kJ��COȼ�����ɶ�����̼�����ų���������1mol̼��ȫȼ�շų�����������110.5 kJ������̼��ȼ���ȴ���110.5 kJ/mol����A����
B����Ӧ�Ȱ������ţ��ٵķ�Ӧ��Ϊ-221 kJ?mol-1����B����
C���к�����ϡ��Һ��ǿ���ǿ�Ӧ����1molˮ�ų�����������H=-57.3 kJ/mol������ϡ������ϡNaOH��Һ��Ӧ���к���Ϊ-57.3 kJ/mol����C��ȷ��
D��������������ʣ�����������������ϡ������ϡNaOH��Һ��Ӧ����1molˮ���ų�������С��57.3 kJ����D��ȷ��
��ѡ��CD��
���������
�����Ѷȣ�һ��
5��ѡ���� ��ͼ��ʾ��N4���ӽṹ����������ƣ�����������ṹ����֪����1molN��N������193kJ����������1molN��N������941kJ������������˵����ȷ����
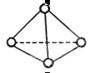
A��N4��һ�ֺ��Ǽ��Թ��ۼ������ͻ�����
B��1mol N4����ת��ΪN2ʱҪ�ų�724kJ����
C��N4�ǵ�����һ��ͬλ��
D��N4�Ľṹ��N2���Գƣ����N4��N2���ȶ�
�ο��𰸣�B
���������N4��N��ɣ���һ�ֵ��ʣ������������ɲ�ͬԪ����ɵĴ������A������N4=2N2��Ӧ�У����ݷ�Ӧ�ȵ��ڷ�Ӧ���ܼ��ܼ�ȥ�������ܼ��ܣ���1molN4����ת��ΪN2�����ջ�ų�������Ϊ��6��193kJ-2��941kJ=-724kJ����˵���÷�Ӧ���ȣ��ҷų�724kJ��������B��ȷ��Ϊ����Ĵ𰸣�N4��N2������NԪ���γɵIJ�ͬ���ʣ���Ϊͬ�������壬��C������1molN4����ת��ΪN2�ų�724kJ������˵��N4������N2���ߣ���N4��N2���ȶ�����D������Ĵ�ѡ��B��
���������⿼���˻�ѧ��Ӧ�������ı仯���ÿ����Ǹ߿��ij������㣬�����ѶȲ���
�����Ѷȣ�һ��