1��ѡ���� ����ӵ���Ѿ���Ϊ��һ��ʵ�û������أ��õ�ؾ��������ܶȴ�ѹ�ߵ����ԡ�����ӵ�طŵ�ʱ�ĵ缫��ӦʽΪ ������Ӧ��C6Li��xe-==C6Li1-x+xLi+ ��C6Li��ʾ�ԭ��Ƕ��ʯī�γɵĸ��ϲ��ϣ�������Ӧ��Li1-xMO2+xLi++xe-==LiMO2��LiMO2��ʾ��﮵Ĺ��ɽ���������������й�˵����ȷ����
[? ]
A������ӵ�س��ʱ��ط�ӦΪC6Li+Li1-xMO2==LiMO2+C6Li1-x
B����ط�Ӧ�У�ﮡ�п������Ǧ��ʧȥ1 mol���ӣ�����������ĵ�����С
C������ӵ�طŵ�ʱ����ڲ�Li+���ƶ�
D������ӵ�س��ʱ������ӦΪC6Li1-x+xLi++xe-==C6Li
�ο��𰸣�BD
���������
�����Ѷȣ�һ��
2������� ȼ�ϵ��������ȼ�ϣ���CO��H2��CH4�ȣ���������Ӧ������Ӧ�����Ļ�ѧ��ת��Ϊ���ܵ�װ�ã�ͨ��������������Ϊ�������Һ��
��1��������й��ڼ��飨CH4��ȼ�ϵ�ص���գ�
�ټ�����������Ӧ�Ļ�ѧ����ʽΪ��
����֪ȼ�ϵ�ص��ܷ�ӦʽΪCH4+2O2+2KOH==K2CO3+3H2O���������һ���ĵ缫��ӦΪCH4+10OH--8e-="=" CO32-+7H2O������缫��ȼ�ϵ�ص� ���������������������һ���缫�ϵĵ缫��ӦʽΪ��
�����ŵ�ز��Ϸŵ磬�������Һ�ļ��� �����������С�����䡱��
��ͨ������£�����ȼ�ϵ�ص����������� ������ڡ�����С�ڡ����ڡ�������ȼ�յ����������ʡ�
��2���ݱ��������Ħ��������MOTOROLA����˾�з���һ���ɼ״��������Լ�ǿ�����������Һ�������ֻ���أ����������������غ�﮵�ص�10����������ʹ��1���³��һ�Ρ��ٶ��ŵ�����У��״���ȫ����������CO2�������������CO32����
�ٸõ�ط�Ӧ�������ӷ���ʽΪ____________________________
�ڼ״���____��������Ӧ��������������ڷŵ��������Һ��pH��____����ͻ����������䣩��
�ο��𰸣���11�֣���1����CH4+O2 CO2+2H2O ��2�֣� ��
CO2+2H2O ��2�֣� ��
�ڸ��� ��1�֣��� 2O2+4H2O+8e-==8OH- ��2�֣�
�ۼ�С ��1�֣� �� �ܴ��ڣ�1�֣�
��2����2CH3OH+3O2+4OH��=2CO32��+6H2O ��2�֣���
�ڸ� ��1�֣��� �½���1�֣�
�����������1���ټ�����������Ӧ���ɶ������Ѻ�ˮ���ʷ���ʽΪCH4+O2 CO2+2H2O��
CO2+2H2O��
��CH4ʧȥ���ӣ�����������Ӧ���Ǹ�����O2���������õ����ӣ�������ԭ��Ӧ���缫��ӦʽΪ2O2+4H2O+8e-==8OH-��
�۸��ݷ�Ӧʽ��֪��KOH������Ӧ���ʵ������Һ�ļ��Լ�С��
�ܼ���ȼ�ջ��˷Ѵ������������ʼ���ȼ�ϵ�ص����������ʴ��ڼ���ȼ�յ����������ʡ�
��2���ٸ������и����ķ�Ӧ���������õ�ط�Ӧ�������ӷ���ʽΪ2CH3OH+3O2+4OH��=2CO32��+6H2O��
�ڼ״�ʧȥ���ӣ���ѧ�����ߣ�����������Ӧ���ʼ״��ڸ���������Ӧ��ǿ������˷�Ӧ���ʵ���ڷŵ��������Һ��pH�����͡�
���㣺ȼ�ϵ�� ���͵�Դ
���������⿼�����ȼ�ϵ�غ����͵�Դ�����֪ʶ����Ŀ�Ѷȴ���Ϥԭ��صĹ���ԭ���ǽ���Ĺؼ���ע�����֪ʶ��ѧϰ�����ռ�Ӧ�á�
�����Ѷȣ�һ��
3��ѡ���� �߹���LaNi5H6 (��Ļ��ϼ�Ϊ0�ۣ�����Ѿ����ڻ�϶����������ܷ�Ӧ���£�LaNi5H6+6NiO(OH)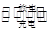 LaNi5+6Ni(OH)2
LaNi5+6Ni(OH)2
����������ȷ����
A�����ʱ����Ͻ�������
B���ŵ�ʱÿת��6mol���ӣ���6moLNiO(OH)������
C�����ʱ������ΧpH����
D���ŵ�ʱ������Ӧ��LaNi5H6+6OH--6e-=LaNi5+6H2O