1、选择题 误食铜、铅或汞中毒后,应采取的急救措施是
A.服用大量的葡萄糖水
B.服用大量的牛奶
C.服用大量的食盐水
D.用服适量的食醋
参考答案:B
本题解析:分析:根据重金属盐中毒的原理判断,重金属盐能使人中毒,实际上是重金属离子使人体中蛋白质发生变性.
解答:A.服用大量的葡萄糖水不与重金属盐反应,不能缓解蛋白质变性,故A错误;
B.服用大量的牛奶,牛奶含有大量蛋白质,能缓解蛋白质变性有效解毒,故B正确.
C.服用大量的食盐水不与重金属盐反应,不能缓解蛋白质变性,故C错误;
D.用服适量的食醋不与重金属盐反应,不能缓解蛋白质变性,故D错误;
故选:B.
点评:本题主要考查蛋白质的性质,题目难度不大,明确重金属中毒的原理是解题的关键.
本题难度:简单
2、选择题 将30mL?0.5mol/L?NaCl溶液加水稀释到500mL,稀释后溶液中NaCl的物质量浓度为
A.0.03mol/L
B.0.3mol/L
C.0.05mol/L
D.0.04mol/L
参考答案:A
本题解析:分析:根据稀释定律可知,溶液稀释前后溶质的物质的量不变,据此计算.
解答:令稀释后溶液中NaCl的物质量浓度为c,则:
30mL×10-3L×0.5mol/L=500mL×10-3L×c
解得c=0.03mol/L.
故选A.
点评:本题考查物质的量浓度有关计算,难度较小,关键清楚稀释定律,溶液稀释前后溶质的物质的量不变.
本题难度:简单
3、选择题 为了除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种试剂过滤后,再加入适量的盐酸,这种试剂是
A.NH3?H2O
B.NaOH
C.Na2CO3
D.MgCO3
参考答案:D
本题解析:分析:Fe3+易水解生成沉淀,可通过调节溶液pH的方法促进Fe3+的水解,注意不能引入新的杂质.
解答:A.加入氨水混入氯化铵杂质,且生成氢氧化镁沉淀,故A错误;
B.加入NaOH易生成氢氧化镁沉淀,且混入NaCl杂质,故B错误;
C.加入碳酸钠,易混入NaCl杂质,故C错误;
D.加入碳酸镁,与氢离子反应,可起到调节溶液pH的作用,促进铁离子的水解生成氢氧化铁沉淀而除去,且不引入新的杂质,故D正确.
故选D.
点评:本题考查物质的分离和提纯,注意根据铁离子易水解的性质用调节溶液pH的方法除杂,注意不能引入新的杂质.
本题难度:简单
4、选择题 质量分数为n的NaOH溶液,其物质的量浓度为amol/L,加热蒸发水使其质量分数变为2n,此时,该溶液中的物质的量浓度为bmol/L,则a与b的关系正确的是
A.b>2a
B.b<2a
C.b=2a
D.a=2b
参考答案:A
本题解析:分析:氢氧化钠溶液浓度越大密度越大,令质量分数为n的NaOH溶液的密度为xg/ml,质量分数为2n的NaOH溶液的密度为yg/ml,根据c=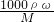 表示质量分数为n的NaOH溶液及质量分数为2n的NaOH溶液的物质的量浓度,据此结合密度x<y判断.
表示质量分数为n的NaOH溶液及质量分数为2n的NaOH溶液的物质的量浓度,据此结合密度x<y判断.
解答:令质量分数为n的NaOH溶液的密度为xg/ml,质量分数为2n的NaOH溶液的密度为yg/ml,则:
质量分数为n的NaOH溶液的物质的量浓度为a=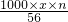 mol/L;
mol/L;
质量分数为2n的NaOH溶液的物质的量浓度为b= mol/L,
mol/L,
氢氧化钠溶液浓度越大,密度越大,所以x<y,故b>2a.
故选A.
点评:本题考查物质的量浓度计算、物质的量浓度与质量分数关系等,难度不大,理解物质的量浓度定义.
本题难度:简单
5、选择题 设nA为阿伏加德罗常数的数值,下列说法正确的是
A.常温下,4g?CH4含nA个C-H共价键
B.1?mol?Fe与足量稀HNO3反应,转移个2nA个电子
C.1L?0.1?mol/L?NaHCO3溶液中含有0.1nA个HCO3-
D.常温常压下,22.4L的NO2和CO2混合气体含有2nA个O原子
参考答案:A
本题解析:分析:A、质量换算物质的量结合甲烷分子结构计算碳氢键;
B、足量稀硝酸与铁反应生成三价铁;
C、碳酸氢根离子水解;
D、依据气体摩尔体积的应用条件是标准状况分析;
解答:A、4g CH4物质的量为0.25mol,分子中含C-H共价键4×0.25×nA=nA个,故A正确;
B、稀硝酸过量,生成硝酸铁,转移电子应该是3 nA个电子,故B错误;
C、碳酸氢根离子水解,应该是小于0.1nA个HCO3-;故C错误;
D、条件错误,应为标准状况,故D错误;
故选A.
点评:本题考查了阿伏伽德罗常数的应用,主要考查了质量换算物质的量计算微粒数,氧化还原反应的产物分析,盐类水解的应用气体摩尔体积的条件应用,题目难度中等.
本题难度:一般