1��ѡ���� ����ʵ���ܻ�óɹ�����
[? ]
A. �ú��ᾧˮ�Ĵ����ƺͼ�ʯ�ҹ����Ƽ�������
B. ����м����ˮ����������屽
C. �ڱ�����Һ�е�������ϡ��ˮ���ְ�ɫ����
D. ��ͭ˿�ھƾ����ϼ��Ⱥ�����������ˮ�Ҵ��У�ͭ˿�ָ���ԭ���ĺ�ɫ
�ο��𰸣�D
���������
�����Ѷȣ�һ��
2������� һ��ѧ�о���ѧϰС���ij��������ӡˢ��·������÷�Һ����̽��������ԭ����2Fe3++Cu�T2Fe2++Cu2+�����밴Ҫ���������̽�����森
[̽��Ŀ��]
�ӷ�Һ�л���ͭ�������µõ�FeCl3��Һ��
[���ϻ�Ϥ]
��3Fe2++NO3-+4H+�T3Fe3++NO��+2H2O
���йؽ������Ӵӿ�ʼ������������ȫʱ��Һ��pH��
Fe3+��2.7��3.7Cu2+��5.2��6.4Fe2+��7.6��9.6
[̽��˼·]
��1����ȷ����Һ����ɼ����������ӵ�Ũ�ȣ�
��2��ѡ������Լ�����ͭ�������µõ�FeCl3��Һ��
[ʵ��̽��]
ȡ���η�Һ���Թ��м�ˮϡ�ͺμ�KSCN��Һ����Ѫ��ɫ����֪��Һ�г�����Fe2+��Cu2+�⣬������Fe3+��
��ͬѧȡ10mL��Һ�������м���������AgNO3��Һ���õ��ij��������ˡ�ϴ�ӡ��������8.61g����ͬѧ��ȡ10mL��Һ������ij�Լ���pH����4.0��ʹ����Fe3+ת��ΪFe��OH��3��������Fe2+��Cu2+�����ڷ�Һ�У����������ˡ�ϴ�ӡ����գ���ȴ����ص�0.32g��
ͨ�������֪��Һ��c��Fe3+��=______mol/L��c��Fe2+��=______mol/L��c��Cu2+��=______mol/L��
[��������]
��λ���1L��Һ�к��е�ͭ�������µõ�FeC13��Һ��
��ͬѧ��ΪӦ�������Һ�м���wg����[w=c��Cu2+����1L��56g/mol]��ʹ֮��ַ�Ӧ�û���ͭ�����ˣ��ý���ͭ��������Һ�м���������ϡ���ᣬ��Fe2+ȫ������ΪFe3+��������β�����������ɴ�ʵ��Ŀ�ģ���Щͬѧ��Ϊ��ͬѧ�ķ��������У��������۱�ͬѧ�ķ�������Щ����֮��������һ��������
��1��______��2��______��3��______
��С��ͬѧ�������۵õ��ĺ����������в��������մﵽ��Ԥ��Ŀ�ģ������������ԣ�
[��չ����]
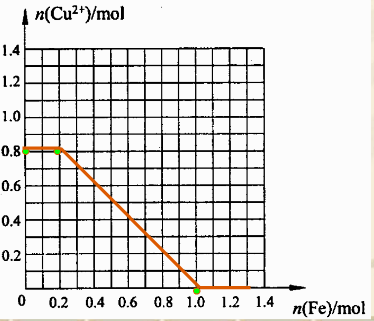
�뻭��1L��Һ�м������۵����ʵ������Һ��ͭ���ӵ����ʵ����Ĺ�ϵ���ߣ�������ͼ����㣬��ͭ���ӵ����ʵ�������һ��ʱ���������۵�������______g��

�ο��𰸣�[ʵ��̽��]��ͬѧʵ������ĵ���8.61g����Ϊ�Ȼ��������ʵ�����0.06mol����Cl-���ʵ���Ϊ0.06mol����ͬѧpH����4.0ʱ��ֻ��Fe3+�������ҳ�����ȫ������Ϊ�������������յõ�0.32gFe2O3�����ʵ���Ϊ0.002mol������Ԫ���غ��֪Fe3+�����ʵ���Ϊ0.004mol��c��Fe3+��=0.004mol0.01L=0.4 mol?L-1����2Fe3++Cu�TCu2++2Fe2+��֪2n��Cu2+��=n��Fe2+�����ɵ���غ��֪��3n��Fe3+��+2n��Cu2+��+2n��Fe2+��=n��Cl-������n��Cu2+��+n��Fe2+��=12��0.06mol-0.004mol��3��=0.024mol��n��Cu2+��+n��Fe2+��=n��Cu2+��+2n��Cu2+��=0.024mol����ã�n��Cu2+��=0.008mol��c��Cu2+��=0.008mol0.01L=0.8 mol?L-1����
n��Fe2+��=2n��Cu2+��=0.016mol��c��Fe2+��=0.016mol0.01L=1.6 mol?L-1��
�ʴ�Ϊ��0.4��1.6��0.8��
[��������]��������������֪��c��Fe3+��=0.4 mol?L-1��c��Cu2+��=0.8 mol?L-1������wg���ۣ������������㣬��Һ���в�����ͭ���ӣ�ʹ������������������Ӧ��������������������ӣ�
�ʴ�Ϊ���������۲��㣬��Һ���в�����Cu2+����HNO3�������������µ�����NO3-��
[��չ����]������1L��Һ����n��Fe3+��=0.4mol��n��Cu2+��=0����8mol�����ȷ���Fe+2Fe3+=3Fe2+ ����Cu2++Fe=Fe2++Cu��0.4molFe3+����0.2molFe����ʱn��Cu2+��=0.8mol���õ����꣨0.2��0.8����Ȼ��Cu2++Fe=Fe2++Cu��Ӧ�������������ʵ�����Cu2+���ٵ����ʵ�����ȣ��ɵõ����¼������꣨0.4��0.6������0.6��0.4����0.8��0.2������1.0��0�����������Ϲ�ϵ���Ի���1L��Һ�м������۵����ʵ������Һ��ͭ���ӵ����ʵ����Ĺ�ϵ���ߣ�
 ��
��
��ͭ�������ʵ�����Ϊ0.4molʱ�������������ʵ���Ϊ0.6mol������Ϊ0.6mol��56g/mol=33.6g��
�ʴ�Ϊ�� ��33.6��
��33.6��
���������
�����Ѷȣ���
3��ѡ���� ����ʵ�鷽���У����ܲⶨNa2CO3��NaHCO3�������Na2CO3��������
[? ]
A.ȡa�˻�����ּ��ȣ�����b��
B.ȡa�˻����������ϡ�����ַ�Ӧ�����ȡ����ɡ����գ���b�˹���
C.ȡa�˻����������ϡ�����ַ�Ӧ���ݳ������ü�ʯ�����գ�����b��
D.ȡa�˻����������Ba(OH)2��Һ��ַ�Ӧ�����ˡ�ϴ�ӡ���ɣ���b�˹���
�ο��𰸣�C
���������
�����Ѷȣ�һ��
4��ѡ���� ����װ�û�������ܴﵽʵ��Ŀ�ĵ���
[? ]
A.�����ſ������ռ�CO2?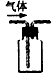
B.ʵ������ȡNH3
C.ʵ������ȡFe(OH)2? 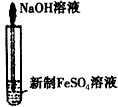
D.ʵ��������������? 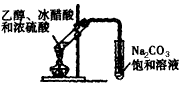
�ο��𰸣�D
���������
�����Ѷȣ�һ��
5������� ijУ��ѧ�о���С�飬���������ṩ��ʵ��װ�ú��Լ���ij��ȼú����Ԫ�ؽ��ж��ԺͶ�����⣬�Իش�
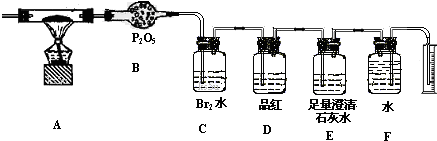
��1����ȼú���ȼ�գ��������徭��ѧ������Ҫ����CO2��H2O��SO2��N2�������壬���ȼúһ�����е�Ԫ��Ϊ______
��2����ȡ��ȼú��ƷWg��ͨ�봿��ʹ����ȼ�գ�����ȼú����������Ԫ�ص�������������������װ�ý���ʵ�飺
��ָ������װ����B��C��D��E������B______?C______? D______?E______
Ϊ�˲����Ӧ���ݣ��������²���������CO2��C��D�е��ܽ⣩
a��ʵ��ǰ��������ƽ�Ƶ�B��C��D��E�������ֱ�ΪW1��W2��W3��W4
b��ʵ����ɺ�Ƶ�B��C��D��E�������ֱ�Ϊm1��m2��m3��m4
c��ͨ����ȷʵ���������Fװ�ò���ռ��������ΪV?L
��Ϊ��ȷ����F���ռ����������������ȷ��ʵ�������______
�۲ⶨȼú�е�����������������۲쵽��ˮ����ȫ��ɫ��Ʒ�첻��ɫʱ��ȼú�к���Ԫ�ص����������ı���ʽΪ______
���۲쵽______����ʱ�������ⶨȼú����Ԫ�ص�����������
�ο��𰸣���1��ȼ��ʱ��ú�Ϳ����е�������Ӧ�������������뷴Ӧ�����������غ㶨�ɣ�ȼ��ǰ��Ԫ��������ͬ������ú�к���C��H��S��N��Ԫ�أ����ܺ�����Ԫ�أ�
�ʴ�Ϊ��C��H��S��N��
��2����ʵ��Ŀ���Ǽ��ú����Ԫ�ص��������������Ա������ն���������ˮ���������Ӧ��SO2+Br2+2H2O=H2SO4+2HBr��D��Ʒ����Һ������������Ƿ��䰲ȫ���գ�E�г���ʯ��ˮ�������ն�����̼������ˮ���ռ������еĵ��������ⶨ�����������ȻB������������������ˮ��P2O5+3H2O=2H3PO4��
�ʴ�Ϊ���������壻����SO2������SO2�Ƿ���ȫ�����գ�����CO2��
��Fƿ�е����¶ȡ�ѹǿ���ⶨ��ֻ�����������¶ȡ�ѹǿ��ʵ���������¶ȡ�ѹǿ��ͬʱ���ⶨʵ�黷�����¶Ⱥ�ѹǿ�����ʵ�鲽������ȴ������Һ���������
�ʴ�Ϊ����������ȴ��ԭ�����¶ȶ���ʱ��ʹFװ����ƿ�й���Һ������Ͳ��ˮ����ƽ������ʱ�����밼Һ����ƽ��
����ˮ����ȫ��ɫ��Ʒ�첻��ɫ��˵����ˮ�ѽ�����������ȫ���գ��ʿ�������C�з�Ӧǰ��������ȷ�����յĶ��������������m��SO2��=��m2-W2��g��m��S��=��m2-W2��g��3264=(m2-W2)2g���أ�S��=(m2-W2)2gWg��100%=m2-w22w��100%��
��Ʒ����ɫʱ��˵����������û�б���ˮ��ȫ���գ���Cװ�þ�������С�ڶ����������������ⶨú���������������
�ʴ�Ϊ��m2-w22w��100%����ˮ��ɫ��Ʒ����ɫʱ��
���������
�����Ѷȣ�һ��