1、填空题 (6分)铁及其化合物之间的相互转化可用下式表示:

回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液实现上述①的转化,要求产物纯净。可选用的试剂是?(选填序号);
a.Cl2? b.Fe? c.HNO3? d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺。精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+===Cu2++5Fe2++2S(CuFeS2中S为-2价)。
则下列说法正确的是?(选填序号);
a.从物质的组成来看,黄铜矿属于合金
b.反应中,所有铁元素均被还原
c.反应中,CuFeS2既作氧化剂又作还原剂
d.当转移1 mol e-?时,有46 g CuFeS2参加反应
(3)高铁酸钾是一种新型、高效的绿色净水剂,其净水原理是??。
参考答案:(6分)
(1)d(2分)?(2)d(2分)
(3)高铁酸钾具有强氧化性,可以杀菌、消毒(1分),同时生成的Fe3+离子转化为Fe(OH)3胶体,能加速悬浮物沉降,起净化作用(1分)。
本题解析:(1)要使产物纯净,必须物质间发生反应后,没有杂质生成。A项有氯离子杂质生成,错误;b项铁与稀硫酸反应生成二价铁离子,不能把二价铁离子转化为三价铁离子,错误;c项硝酸能氧化二价铁离子生成三价铁离子,但溶液中还有杂质硝酸根离子,错误;d项双氧水能氧化二价铁离子生成三价铁离子,同时有水生成,水是原溶液的成分,所以不是杂质,正确。故选d。
(2)a项合金是由两种或两种以上的金属与非金属经一定方法所合成的具有金属特性的物质,所以黄铜矿不是合金,错误;b项CuFeS2中铁元素的化合价为+2价,生成物中Fe2+的化合价为+2价,所以不是所有铁元素均被还原,错误;c项CuFeS2中只有S元素的化合价只有降低,其他元素的化合价不变,所以CuFeS2只作还原剂,错误;d项根据反应CuFeS2+4Fe3+=Cu2++5Fe2++2S,在这个反应中转移4mol电子,生成184g?CuFeS2。则转移1 mol e-?时,有? 46g?CuFeS2参加反应。故d正确。
(3)高铁酸钾( K2FeO4)中Fe的化合价是+6价,具有强氧化性,能杀菌消毒,其还原产物Fe3+水解生成氢氧化铁胶体,能吸附水中杂质,所以高铁酸钾作为水处理剂发挥的作用是净水、消毒。
点评:本题考查了铁盐和亚铁盐的相互转化,难度不大,注意二价铁离子和三价铁离子的检验是高考的热点,三价铁离子能使KSCN变红色。
本题难度:一般
2、选择题 等质量的下列物质与足量稀硝酸反应,放出NO物质的量最多的是
A.FeO
B.Fe2O3
C.FeSO4
D.Fe3O4
参考答案:A
本题解析:根据化学式可算出四种物质中+2价Fe含量最大的是FeO,所以等质量的四种物质与足量稀硝酸反应,放出NO物质的量最多的是FeO,故A项正确。
本题难度:一般
3、填空题 (10分)过渡金属元素氧化物应用研究是目前科学研究的前沿之一,回答下列问题:

Ⅰ、二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。有关甲醛、苯、及水说法正确的是_____________。
A.苯分子中含有碳碳键的键能较大,不易发生化学反应
B.苯不能使酸性KMnO4溶液褪色,说明其分子中不含碳碳双键
C.甲醛的沸点比甲酸低,主要原因是甲酸分子间可以形成氢键
D.水分子稳定性高,是因为水分子间能形成氢键
Ⅱ、2007年诺贝尔物理学奖为法国科学家阿尔贝・费尔和德国科学家彼得・格林贝格尔共同获得,以表彰他们在巨磁电阻效应(CMR效应)研究方面的成就。某钙钛型复合氧化物(如右图),以A原子为晶胞的顶点,A位可以是+2价的Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应。
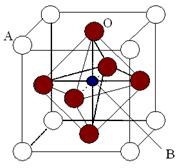
用A、B、O表示这类特殊晶体的化学式__________。(A、B为元素代号,O为氧元素)
⑵已知La为+3价,当被钙等二价元素A替代时,可形成复合钙钛矿化合物La1-xAxMnO3, (x < 0.1),此时一部分锰转变为+4价。导致材料在某一温度附近有反铁磁-铁磁、铁磁-顺磁转变及金属-半导体的转变,则La1-xAxMnO3中三价锰与四价锰的物质的量之比为:____________。(用含x的代数式表示)
⑶26Fe3+的核外电子排布式为:?。
⑷下列有关说法正确的是__________________。
A.镧、锰、氧分别位于周期表f、d、p区
B.晶体铬属于体心立方堆积,其堆积方式如右图:
C.锰的电负性为1.59 ,Cr的电负性为1.66,说明锰的金属性比铬强
参考答案:I、 ABC(2分,答对2个给1分,全对给2分)?
Ⅱ、(1)ABO3(2分)?(2)(1-x)/x(2分)
(3)[Ar]3d5?(2分)?(4)AC(2分)
本题解析:I:水分子稳定性高,是因为O元素的非金属性较强,共价键比较牢固,而水分子间的氢键只影响水的熔、沸点,而不影响水分子的稳定性。
II:该晶胞为立方体结构,其中A位于立方体顶点平均每个晶胞占A为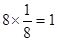 ,O位于体心平均每个晶胞占O为
,O位于体心平均每个晶胞占O为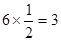 ,B位于体心平均每个晶胞占B为1,所以化学式为ABO3;
,B位于体心平均每个晶胞占B为1,所以化学式为ABO3;
La1-xAxMnO3中其化合价如图所示: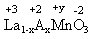 ,则根据正负化合价为0可求得y=3+x;+y为Mn的平均化合价,设+3价Mn物质的量为a mol 、+4价Mn物质的量为b mol;所以有等式a+b=1;3a+4b=3+x;解得
,则根据正负化合价为0可求得y=3+x;+y为Mn的平均化合价,设+3价Mn物质的量为a mol 、+4价Mn物质的量为b mol;所以有等式a+b=1;3a+4b=3+x;解得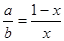
(3) 26Fe3+的核外电子排布式为:[Ar]3d5
(4)该图为面心立方最密堆积
本题难度:简单
4、选择题 下表中,对第Ⅰ、Ⅱ栏判断都正确的是
| ? | 第Ⅰ栏 | 第Ⅱ栏 | 判断
A.
铁与稀硫酸反应可生成氢气
铁丝在氧气中点燃生成Fe3O4
Ⅰ对;Ⅱ对
B.
Na2CO3溶液中,c(Na+)=2c(CO32-)
21H原子的中子数和质子数相等
Ⅰ对;Ⅱ错
C.
Na2O2与H2O反应的化学方程式为
Na2O2+H2O=2NaOH+O2↑
常温下可用铝罐贮存浓硝酸
Ⅰ对;Ⅱ对
D.
用AgNO3溶液和稀硝酸可区分Na2CO3、NaBr溶液
25℃时,改变醋酸溶液的浓度,醋酸的电离平衡常数也改变
Ⅰ对;Ⅱ对
|
A.A
B.B
C.C
D.D
参考答案:A、金属Fe与稀硫酸反应可生成氢气和硫酸亚铁,所以Ⅰ正确,铁丝在氧气中点燃生成Fe3 O4,所以Ⅱ正确,故A正确;
B、碳酸钠中,碳酸根离子水解,所以钠离子浓度是碳酸根浓度的2倍还要多,所以Ⅰ错误,在21H原子中,质量数=质子数+中子数,即21H原子的中子数和质子数相等,均为1,所以Ⅱ正确,故B错误;
C、Na2O2与H2O反应的化学方程式为2Na2O2 +2H2O=4NaOH+O2↑,所以Ⅰ错误,常温下金属铝遇到浓硝酸发生钝化,常温下可用铝罐贮存浓硝酸,所以Ⅱ正确,故C错误;
D、硝酸酸化的硝酸银和Na2CO3、NaBr溶液反应时,溴化钠中会出现淡黄色沉淀,现象碳酸钠中没有此现象,所以Ⅰ正确,弱电解质的电离平衡常数只受温度的影响,改变醋酸溶液的浓度,醋酸的电离平衡常数不会改变,所以Ⅱ错误,故D错误.
故选A.
本题解析:
本题难度:简单
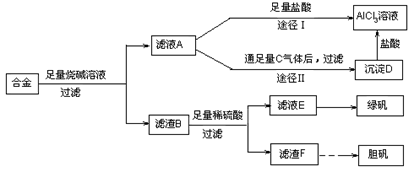
5、填空题 (15分)某化学兴趣小组用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体和胆矾晶体,以探索工业废料的再利用。其实验方案如下:
请回答下列问题:
(1)由滤液A制得AlCl3溶液有途径Ⅰ和Ⅱ两条,你认为合理的是?,理由是:
?。
(2)从滤液E中得到绿矾晶体的实验操作是?。
(3)请用一个总反应式表示由滤渣F制备胆矾晶体过程中发生的变化:?
?。
(4)有同学提出可将方案中最初溶解合金的烧碱改用盐酸,重新设计方案,也能制得三种物质,你认为后者的方案是否更合理?,理由是?
?。
参考答案:(1)途径Ⅱ更合理;因为滤液A是NaAlO2溶液,按途径I直接向A加入盐酸得到的AlCl3溶液中含有大量的NaCl杂质;按途径II,通入c(CO2)气体,得D[Al(OH)3]沉淀,将Al(OH)3溶解于盐酸中得到的是纯净的AlCl3溶液。所以途径II更合理(2)蒸发浓缩、冷却结晶、洗涤、干燥(3)2Cu + O2 + 2H2SO4+8H2O 2CuSO4・5H2O (4)后者的方案不合理?因为该方案不符合实验方案设计的简约性原则,即操作步骤多、消耗试剂量更大、时间长。
2CuSO4・5H2O (4)后者的方案不合理?因为该方案不符合实验方案设计的简约性原则,即操作步骤多、消耗试剂量更大、时间长。
本题解析:(1)偏铝酸钠和过量的盐酸反应生成氯化铝和氯化钠的混合物,而向偏铝酸钠中通入足量的二氧化碳,会得到纯净的氢氧化铝沉淀,再用盐酸溶解,所得溶液的成分只有氯化铝,故答案为:Ⅱ;因为滤液A是偏铝酸钠和氢氧化钠溶液,按途径I直接向A中加入盐酸得到的AlCl3溶液中含有大量的氯化钠杂质;按途径II通入二氧化碳气体,得Al(OH)3沉淀,将Al(OH)3溶解于盐酸中得到的是纯净的AlCl3溶液;(2)将混合液来制备绿矾时应先将溶液加热浓缩、然后冷却结晶,洗涤干燥后即可得到绿矾,故答案为:蒸发浓缩、冷却结晶、洗涤、干燥。(3)由矿渣制备胆矾,故矿渣为铜。铜不能和稀硫酸反应,铁可以和硫酸反应,所以滤渣F是金属铜,Cu中加入稀硫酸可以制备胆矾晶体,反应方程式为:2Cu+2H2SO4+8H2O+O2=2CuSO4?5H2O,(4)在实验方案一中,酸的量的控制上没有过高的要求,只需过量即可,但是方案二中,需要的是适量的酸,这很难控,故答案为:不合理;因为该方案操作步骤多、时间长,消耗试剂量大。
本题难度:一般