1、填空题 (1)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈________(填“酸性”、“中性”或“碱性”),溶液中c(Na+)________c(CH3COO-)(填“>”、“=”或“<”)。
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈________(填“酸性”、“中性”或“碱性”),溶液中c(Na+)________c(CH3COO-)(填“>”、“=”或“<”)。
(3)物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中CH3COO-和Na+浓度相等,则混合后溶液呈________(填“酸性”、“中性”或“碱性”),醋酸体积________氢氧化钠溶液体积(填“大于”、“等于”或“小于”)。
参考答案:(1)碱性 > (2)酸性 < (3)中性 大于
本题解析:(1)CH3COOH与NaOH恰好完全反应,溶液呈碱性,c(Na+)>c(CH3COO-)。
(2)pH=3的醋酸的物质的量浓度大于1.0×10-3mol/L,故混合后CH3COOH剩余,溶液呈酸性,c(Na+)<c(CH3COO-)。
(3)由电荷守恒可知,当c(CH3COO-)=c(Na+)时溶液呈中性,CH3COOH略过量,故醋酸的体积大于氢氧化钠溶液的体积。
本题难度:一般
2、选择题 某溶液中FeCl3的水解反应已达平衡.FeCl3+3H2O 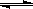 ?Fe(OH)3+3HCl若要使FeCl3的水解程
?Fe(OH)3+3HCl若要使FeCl3的水解程 度增大,应采取的方法是
度增大,应采取的方法是
A.加入NaHCO3
B.加入AgNO3
C.加FeCl3固体
D.加热
参考答案:AD
本题解析:略
本题难度:一般
3、选择题 氯化铵晶体溶于重水(D2O)中,溶液呈现酸性,下列叙述的原因中正确的是(?)
A.NH4+水解生成NH3・H2O和HD2O+
B.NH4+水解生成NH3・DHO和HD2O+
C.NH4+水解生成NH3・D2O和HD2O+
D.NH4+水解生成NH3・DHO和D3O+
参考答案:D
本题解析:氯化铵是强酸弱碱盐,NH4+水解显酸性。水解的实质是NH4+结合水电离出的OH-生成一水合氨,在重水中则结合OD-生成NH3・DHO。在重水中氢离子是以D3O+形式存在。所以正确的答案是D。
本题难度:一般
4、选择题 在蒸发皿中加热蒸干并灼烧,下列物质的溶液,可以得到该固体物质的是
A.氯化铝
B.碳酸氢钠
C.高锰酸钾
D.硫酸铁
参考答案:D
本题解析:A错,热蒸干氯化铝溶液,铝离子会水解生成氢氧化铝,灼烧生成氧化铝;
B错,碳酸氢钠不稳定受热易分解为碳酸钠,加热后得到的固体为碳酸钠;
C错,高锰酸钾受热不稳定易分解为锰酸钾、二氧化锰。
D正确,硫酸铁溶液中虽然+3铁离子要发生水解,但水解后生成的氢氧化铁与硫酸会继续反应,最终得到硫酸铁固体。
本题难度:一般
5、选择题 下列电解质溶液的有关叙述正确的是(? )
A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7
B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大
C.含1 mol KOH的溶液与1 mol CO2完全反应后,溶液中c(K+)= c(HCO3-)
D.在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)= c(CH3COO-)
参考答案:D
本题解析:未知是几元强酸和几元强碱,A错误;硫酸钡沉淀中加入硫酸钠固体,Ksp(BaSO4)不变,c(SO42-)增大,c(Ba2+)减小,B错误;含1 mol KOH的溶液与1 mol CO2完全反应后生成KHCO31mol,HCO3-水解,所以c(K+)>c(HCO3-),C错误;CH3COONa溶液中CH3COO-水解使得c(Na+)> c(CH3COO-),向其中加入适量CH3COOH使CH3COO-+H2O CH3COOH+OH-平衡向左移动,c(CH3COO-)增大,D正确。
CH3COOH+OH-平衡向左移动,c(CH3COO-)增大,D正确。
点评:盐类水解不容忽视。
本题难度:一般