1、选择题 某物质灼烧时,火焰呈黄色,下列判断中正确的是
A.该物质一定不含钾元素
B.该物质一定是金属钠
C.该物质一定是钠的化合物
D.该物质一定含钠元素
参考答案:D
本题解析:分析:焰色反应是某些金属或它们的化合物在无色火焰中灼烧时使火焰呈现特征的颜色的反应;某物质灼烧时,火焰呈黄色,说明是含钠元素的物质,可以是钠单质,也可以是含钠元素的化合物;
解答:A、金属K是在高温下用Na还原得到的,所以实验中用的K中会混有微量的Na,灼烧时火焰容易呈黄色,因此钾元素的焰色反应必须隔着钴玻璃观察为紫色火焰,故A错误;
B、焰色反应是钠元素的性质,可以是金属钠,也可以是含钠元素的化合物,故B错误;
C、焰色反应是钠元素的性质,可以是金属钠,也可以是含钠元素的化合物,故C错误;
D、该物质一定含有钠元素,故D正确;
故选D.
点评:本题考查了焰色反应的概念应用,理解焰色反应的实质是金属元素的性质.
本题难度:一般
2、选择题 两种气态烃的混合气体0.1mol,完全燃烧后生成0.16molCO2和3.6g水,则混合气体是
A.一定有丙炔
B.一定是甲烷和乙烯
C.一定没有乙烷
D.一定有乙炔
参考答案:C
本题解析:分析:n(H2O)=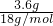 =0.2mol,即0.1mol混合烃完全燃烧生成0.16molCO2和0.2molH2O,
=0.2mol,即0.1mol混合烃完全燃烧生成0.16molCO2和0.2molH2O,
则混合烃的平均分子式为C1.6H4,根据平均分子式进行判断.
解答:n(H2O)=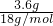 =0.2mol,即0.1mol混合烃完全燃烧生成0.16molCO2和0.2molH2O,
=0.2mol,即0.1mol混合烃完全燃烧生成0.16molCO2和0.2molH2O,
则混合烃的平均分子式为C1.6H4,烃中C原子数小于1.6的只有甲烷,则一定含有甲烷,CH4分子中含4个氢原子,故另一种分子中一定含4个氢原子,且其碳原子数大于1.6,故可能是C2H4或C3H4,一定没有C2H6或C2H2,二者的H原子不等于4,
故选C.
点评:本题考查混合烃组成的判断,题目难度中等,本题关键是能够正确分析有机物完全燃烧生成的CO2和H2O的物质的量关系,根据平均分子式进行判断.
本题难度:一般
3、选择题 常温下,不可能与NaHCO3溶液反应生成气体的物质是
A.酸
B.碱
C.盐
D.氧化物
参考答案:B
本题解析:分析:根据能与NaHCO3溶液反应并放出气体的溶液为酸性来回答.
解答:A、酸如盐酸能与NaHCO3反应:HCl+NaHCO3=NaCl+CO2↑+H2O,故A正确;
B、NaHCO3溶液与碱如NaOH溶液反应:NaHCO3+NaOH=Na2CO3+H2O,无气体放出,故B错误;
C、NaHSO4溶液呈酸性,属于盐类,能与NaHCO3反应:NaHSO4+NaHCO3=Na2SO4+CO2+H2O,故C正确;
D、NaHCO3溶液与氧化物(三氧化硫或是二氧化氮反应),如向NaHCO3溶液中加入三氧化硫,发生反应:H2O+SO3+2NaHCO3=Na2SO4+2CO2↑+2H2O,故D正确;
故选B.
点评:本题主要考查了酸式盐的性质,酸式盐既可以与酸反应也可以与碱反应,但硫酸氢盐为强酸的酸式盐只能与碱反应,溶液显酸性.
本题难度:简单
4、选择题 向物质的量浓度均为1mol/L的下列溶液中通入SO2,一定不会出现沉淀或浑浊的是
A.Ba(OH)2
B.Ba(NO3)2
C.Na2S
D.BaCl2
参考答案:D
本题解析:分析:A、SO2和Ba(OH)2 反应生成BaSO3沉淀;
B、SO2溶于水生成H2SO3,而亚硫酸电离的H+和硝酸根组成了硝酸,能将+4的S氧化成SO42-,而形成BaSO4沉淀;
C、S2-和SO2发生氧化还原反应,生成S单质沉淀;
D、SO2溶于水生成的H2SO3是弱酸,不会与强酸的钡盐发生复分解反应.
解答:A、SO2为酸性氧化物,Ba(OH)2 反应生成BaSO3白色沉淀和水,故A错误;
B、SO2溶于水生成H2SO3,而亚硫酸电离的H+和硝酸根组成了硝酸,硝酸具有强氧化性,能将+4的S氧化成SO42-,而形成BaSO4白色沉淀,故B错误;
C、S2-具有还原性,SO2具有氧化性,S2-和SO2发生氧化还原反应,生成S淡黄色沉淀,故C错误;
D、SO2溶于水生成的H2SO3是弱酸,因为弱酸不能制强酸,SO2不能和BaCl2发生反应,所以不会出现沉淀,故D错误;
故选D.
点评:本题考查二氧化硫的性质,二氧化硫为酸性氧化物,溶于水生成亚硫酸、亚硫酸为多元弱酸,并且二氧化硫还具有漂白性、氧化性和还原性,解题时要认真分析.
本题难度:困难
5、选择题  下表各组物质中,物质之间通过一步反应就能实现如图所示转化的是
下表各组物质中,物质之间通过一步反应就能实现如图所示转化的是
A.A
B.B
C.C
D.D
参考答案:D
本题解析:分析:A.Al和NaOH生成NaAlO2而不是Al(OH)3;
B.CH3CH2OH和CH3COOH反应生成乙酸乙酯,不能生成乙醛;
C.NaHCO3与CO2不反应;
C.Cl2和Fe反应生成FeCl3,FeCl3与Fe反应生成FeCl2,Cl2与FeCl2反应生成FeCl3.
解答:A.Al和NaOH生成NaAlO2而不是Al(OH)3,如a为AlCl3可符合,故A错误;
B.CH3CH2OH和CH3COOH反应生成乙酸乙酯,不能生成乙醛,故B错误;
C.NaHCO3与CO2不反应,故C错误;
D.Cl2和Fe反应生成FeCl3,FeCl3与Fe反应生成FeCl2,Cl2与FeCl2反应生成FeCl3,符合转化关系,故D正确.
故选D.
点评:本题考查无机物的推断,题目侧重于元素化合物的考查,注意把握相关物质的性质,题目难度不大.
本题难度:困难