1、填空题 [化学―选修2:化学与技术](15分)
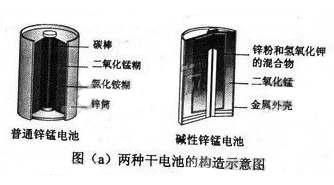
锌锰电池(俗称干电池)在生活中的用量很大。两种锌锰电池的构造图如图(a)所示。
回答下列问题:
(1)①普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH。该电池中,负极材料主要是____________________,电解质的主要成分是__________,正极发生的主要反应是________________________________________________________。
②与普通锌锰电池相比,碱性锌锰电池的优点及其理由是_______。
(2)图(b)表示回收利用废旧普通锌锰电池的一种工艺(不考虑废旧电池中实际存在的少量其他金属)。
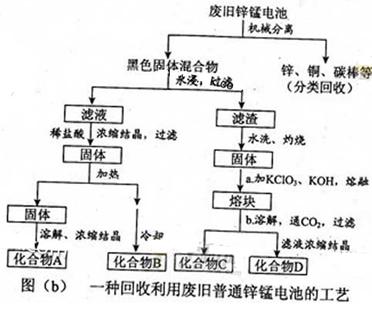
①图(b)中产物的化学式分别为A_______,B________。
②操作a中得到熔块的主要成分是K2MnO4。操作b中,绿色的K2MnO4溶液反应后生成紫色溶液和一种黑褐色固体,该反应的离子方程式为_______。
③采用惰性电极电解K2MnO4溶液也能得到化合物D,则阴极处得到的主要物质是____。(填化学式)
参考答案:
(1)①Zn? NH4Cl? MnO2+NH4++e-=" MnOOH+" NH3
②碱性电池不易发生电解质的泄露,因为消耗的负极改装在电池的内部,碱性电池的使用寿命较长,因为金属材料在碱性电解质中比在酸性电解质中的稳定性提高。
(2)①ZnCl2? NH4Cl?②3MnO42-+2CO2=2MnO4-+MnO2↓+2CO32-?③H2
本题解析:
(1)根据化学方程式Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH,锌是负极材料,氯化铵是电解质的主要成分,二氧化锰和铵根离子在正极发生反应, MnO2+NH4++e-=" MnOOH+" NH3。与普通锌锰电池相比,碱性锌锰电池的优点及其理由是碱性电池不易发生电解质的泄露,因为消耗的负极改装在电池的内部,碱性电池的使用寿命较长,因为金属材料在碱性电解质中比在酸性电解质中的稳定性提高。
(2)废电池经机械分离后,加水溶解后再加稀盐酸,浓缩结晶得到氯化铵和氯化锌。氯化铵不稳定,受热易分解,所以B为氯化铵,A为氯化锌。绿色的K2MnO4溶液发生反应后生成紫色的高锰酸钾溶液和黑褐色的二氧化锰,该反应的离子方程式为3MnO42-+2CO2=2MnO4-+MnO2↓+2CO32-。采用惰性电极电解K2MnO4溶液,阴极氢离子得电子生成氢气。
【考点定位】化学与技术、原电池原理、电极方程式的书写
本题难度:一般
2、选择题 微生物燃料电池因具有原料广泛、操作条件温和、清洁高效和资源利用率高、无污染等特点而被人们所重视.以用葡萄糖作底物的燃料电池为例,其正负极反应式如下:
正极反应:6O2+24H++24e- 12H2O
12H2O
负极反应:C6H12O6+6H2O-24e- 6CO2↑+24H+
6CO2↑+24H+
则有关该电池的下列说法正确的是
[? ]
A.该电池的工作环境是高温条件
B.作为负极的葡萄糖(C6H12O6)在变化中失去电子,被还原
C.该电池的电解质溶液是强酸性溶液,如浓硫酸或硝酸等
D.该电池的总反应为C6H12O6+6O2 6CO2+6H2O
6CO2+6H2O
参考答案:D
本题解析:
本题难度:一般
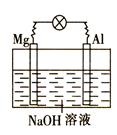
3、选择题 如图所示,将镁片、铝片平行插入一定浓度的NaOH溶液中,用导线连接成闭合回路,该装置在工作时,下列叙述中正确的是?
 ?
?
A.镁比铝活泼,镁失去电子被氧化成Mg2+。
B.铝是电池的负极,开始工作时溶液中会立即有白色沉淀生成
C.该装置的内、外电路中,均是电子的定向移动形成电流
D.该装置开始工作时,铝片表面的氧化膜可不必处理
参考答案:D
本题解析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。镁的金属性强于铝的,但镁和氢氧化钠溶液不反应,而金属铝可以,所以铝是负极,镁是正极,A不正确;氢氧化钠溶液是过量的,得不到氢氧化铝白色沉淀,B不正确;溶液中靠离子的定向运动,C不正确;金属铝表面含有氧化膜氧化铝,但氧化铝是两性氧化物,能溶于氢氧化钠溶液中,不必处理,D正确,答案选D。
点评:该题是中等难度的试题,试题设计新颖,注重答题的灵活性,有利于培养学生的逻辑推理能力和发散思维能力。该题的关键是在明确原电池工作原理的基础上,灵活运用,有利于提高学生的应试能力,提升学生的学科素养。
本题难度:一般
4、选择题 下列有关电池的说法错误的是?
A.手机上用的锂离子电池属于二次电池
B.铅蓄电池中负极为铅,电解质是硫酸
C.氢氧燃料电池正极输入氢气,负极输入空气
D.锌锰干电池即使不用,长久放置也会失效
参考答案:C
本题解析:锂离子电池可以反复充放电,属于二次电池,A正确;铅蓄电池中负极为铅,正极是二氧化铅,电解质是硫酸,B正确;原电池中负极失去电子,正极得到电子。则氢氧燃料电池正极输入空气,负极输入氢气,C不正确。干电池中的电解质溶液易与锌反应减小电解质的量和电极材料的量,所以锌锰干电池即使不用,长久放置也会失效,D正确,答案选C。
点评:该题紧密联系生活实际,基础性强,难度不大,有利于调动学生的学习兴趣,激发学生的学习积极性。
本题难度:简单
5、选择题 镍氢电池的总反应为 H2+2NiO(OH) 2Ni(OH)2,根据此反应式判断,此电池放电时,正极上发生反应的物质是(? )。
2Ni(OH)2,根据此反应式判断,此电池放电时,正极上发生反应的物质是(? )。
A.NiO(OH)
B.Ni(OH)2
C.H2
D.H2和NiO(OH)
参考答案:A
本题解析:此电池放电时,是把化学能转化为电能,相当于原电池装置,所以原电池中正极发生还原反应,元素化合价降低,NiO(OH)中Ni元素的化合价由+3价降为+2价,因此正极上发生反应的物质是NiO(OH),答案选A。
本题难度:一般