1��ѡ���� �ö��Ե缫���һ��Ũ�ȵ�CuSO4��Һһ��ʱ�����0.1molCu2��OH��2CO3ǡ��ʹ��Һ�ָ���ԭ����״̬����������������ת�Ƶ�������ʵ���Ϊ��������
A��0.2mol
B��0.4mol
C��0.5mol
D��0.6mol
�ο��𰸣��������ͭʱ�����Σ�2CuSO4+2H2O?ͨ��?.?2Cu��+O2��+2H2SO4����Σ�2H2O?ͨ��?.?2H2��+O2����
���ֻ���յ�һ�εĵ�⣬��Ӧֻ��Ҫ����CuO��CuCO3�Ϳ��ԣ��������ڼ������Cu2��OH��2CO3���൱�ڶ������һ��ˮ��0.1molH2O������0.1mol��ˮ��Ӧ���ǵڶ��εķ�Ӧ���У��ý�ת����0.4mol���ӣ���һ��ת����0.2mol���ӣ������ܹ�ת�Ƶ���0.6mol��
��ѡD��
���������
�����Ѷȣ���
2��ѡ���� ���й��ڵ������Һ��������ȷ����
A���к�pH���������ͬ����������ᣬ����NaOH�����ʵ���֮����1��2
B��pH=13�İ�ˮ��ˮϡ�ͺ���Һ���������ӵ�Ũ�Ⱦ�����
C��Ũ�Ⱦ�Ϊ0.1 mol��L��1��������Һ��pH�ɴ�С����˳��Ϊ��NaOH>Na2CO3>NaHSO4>(NH4)2SO4��
D��0.1 mol��L��1���������Һ�У�����Ũ�ȴ�С˳��Ϊ�� c(NH4+)>c(SO42��)>c(H��) >c(OH��)
�ο��𰸣�D
���������A�����к͵����������pH���������ͬ��������Һ�е������Ӷ���ͬ��������NaOH�����ʵ���֮����1��1���ʴ�
B��pH=13�İ�ˮ�к���H+? NH4+ OH-��������Һ�������OH-Ũ�ȼ�С��������Һ������H+��OH-�˻��Ƕ�ֵ������������Ũ������
C��Ũ�Ⱦ�Ϊ0.1 mol��L��1��������Һ������̼���Ƴʼ��ԣ����������ܵ����������Ũ�ȴ���笠�����ˮ�������������Ũ�ȣ������������Ƶ�������ǿ��pH��С��pH�ɴ�С����˳��Ϊ��NaOH>Na2CO3>(NH4)2SO4> NaHSO4��
D��0.1 mol��L��1�������(NH4)2SO4��Һ�У���Һ�����ԣ�����Ũ�ȴ�С˳��Ϊ�� c(NH4+)>c(SO42��)>c(H��) >c(OH��)���ʶԡ�
������������Ҫ����������Ũ�ȴ�С�ıȽϣ����������ܷ���ˮ���ǽ���Ĺؼ���
�����Ѷȣ�һ��
3��ѡ���� ��ⷨ�������Ժ�����ˮ����Ҫ����Cr2O72-��ʱ�����������������������������д��ڷ�ӦCr2O72+6Fe2++14H+�T2Cr3++6Fe3++7H2O�����Cr3+��Cr��OH��3��ʽ��ȥ������˵������ȷ���ǣ�������
A��������ӦΪFe-2e-�TFe2+
B������������ҺpH����仯
C����������Fe��OH��3��������
D����·��ÿת��12?mol���ӣ������1?mol?Cr2O72-����ԭ
�ο��𰸣�A��Fe����������Ϊ���Ե缫��Feʧ���ӣ�����������Ӧ�����������ӣ�������ӦΪFe-2e-�TFe2+����A��ȷ��
B���ɷ�ӦʽCr2O72+6Fe2++14H+�T2Cr3++6Fe3++7H2O��֪���������������������ӣ���Һ�����Լ�������ҺpH����B����
C������������ԭ��Ӧ����Һ�е������ӵõ����Ӽ��٣�ͬʱ��������������Fe��OH��3�������ɣ���C��ȷ��
D��Fe-2e-=Fe2+����ת�Ƶ�����12mol��Ҫ6molFe���ٸ����ܹ������Ĺ�ϵʽ����6Fe��12e-��6Fe2+��Cr2O72-���ʱ���ԭ��Cr2O72-�����ʵ���Ϊ1mol����D��ȷ��
��ѡB��
���������
�����Ѷȣ���
4��ѡ���� ����������(Ni2O3)������������ܵ�أ����ⷨ�Ʊ��������£���NaOH��NiCl2��ҺpH��7.5���ӷ����������ƺ���е�⡣�������в�����Cl2������������������ClO-���Ѷ���������Ϊ������������˵����ȷ����
[? ]
A������������������
B��������������������Һ��pH����
C��������Ӧ����ʽΪ��2Cl-��2e-��Cl2
D��1 mol������ȫ��ת��Ϊ������ʱ�����·��ͨ����1 mol����
�ο��𰸣�CD
���������
�����Ѷȣ�һ��
5������� 25����12�֣���չ���⼼��������ȼ�ϵ���ƹ�Ӧ�õĹؼ����о�����Һ����һ�����õĴ������ʣ��䴢�������ɴ�17.6% ��������������Һ��������ֽ��������������Ϊȼ�Ϲ�������ȼ�ϵ�ء������ֽⷴӦ���Ȼ�ѧ����ʽ���£�
2NH3(g)  N2 (g) + 3H2(g) ��H =" +92.4" kJ��mol-1
N2 (g) + 3H2(g) ��H =" +92.4" kJ��mol-1
��ش��������⣺
(1) �����Է��ֽ�ķ�Ӧ������ ��������¡��������¡����κ������¡���
(2) ��֪��2H2(g)+O2(g)=2H2O(g) ��H =" -" 483.6 kJ��mol-1
NH3(l) NH3(g) ��H =" +23.4" kJ��mol-1
NH3(g) ��H =" +23.4" kJ��mol-1
��Ӧ4NH3(l)+3O2(g)=2N2(g)+6H2O(g)�Ħ�H = ��
(3) �о��������������ɼ��ٰ����ķֽ⡣ͼ1Ϊij�¶��µ������IJ�ͬ�����ֱ����Ũ�Ȱ����ֽ����������ij�ʼ���ʡ�
�ٲ�ͬ���������£������ֽⷴӦ�Ļ�������� ����д�����Ļ�ѧʽ)��
�ں��£�T1������ʱ����Ni���ֽ��ʼŨ��Ϊc0�İ�������ʵʱ���ֽ�����а�����Ũ�ȡ������ð�����ת���ʦ�(NH3)��ʱ��t�仯�Ĺ�ϵ���ߣ���ͼ2��������ͼ2�л��������¶�ΪT1��Ru���ֽ��ʼŨ��Ϊc0�İ��������Ц�(NH3) ��t�仯�����������ߣ���עRu-T1����
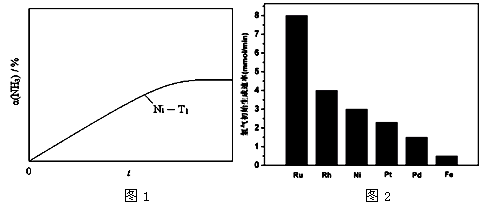
���������Ӧ�¶���ߵ�T2������ͼ2��������һ��Ru���ֽ��ʼŨ��Ϊc0�İ��������Ц�(NH3) ~ t�����������ߣ���עRu-T2��
(4) ��Pt�缫��Һ�����е��Ҳ�ɲ���H2��N2�������ĵ缫��Ӧʽ�� ��
����֪��Һ����2NH3(l)  NH2�� + NH4����
NH2�� + NH4����
�ο��𰸣�(1) ����
(2) -1172.4 kJ��mol-1
(3) ��Fe
�� ��ͼ����Ru-T1
�� ��ͼ���� Ru-T2

(4) 2NH3 + 2e��= H2 + 2NH2�� ����2NH4++2e��= H2 +2NH3��
�����������1����������������Ӧ�ķ������ɴٽ��������Է��ֽ⣻��2��2NH3(g)  N2 (g) + 3H2(g)����H =" +92.4" kJ��mol-1��2H2(g)+O2(g)=2H2O(g)����H =" -" 483.6 kJ��mol-1��NH3(l)
N2 (g) + 3H2(g)����H =" +92.4" kJ��mol-1��2H2(g)+O2(g)=2H2O(g)����H =" -" 483.6 kJ��mol-1��NH3(l) NH3(g)����H =" +23.4" kJ��mol-1�ۣ�3����+4����-3����="-1172.4" kJ��mol-1����3����ͬ���������£���������������Խ�٣�����Ļ�ܾ�Խ���¶Ȳ��䣬ʹ��Ru����������Ӧ�ٶȼӿ죬���ﵽƽ��ʱ������Ũ����ȣ��¶����ߣ�ʹ��ͬһ�ִ�������Ӧ���ʼӿ죬����������࣬������ת��������4�������ǵõ��ӵķ�Ӧ�����ʱ�����õ��ӡ�
NH3(g)����H =" +23.4" kJ��mol-1�ۣ�3����+4����-3����="-1172.4" kJ��mol-1����3����ͬ���������£���������������Խ�٣�����Ļ�ܾ�Խ���¶Ȳ��䣬ʹ��Ru����������Ӧ�ٶȼӿ죬���ﵽƽ��ʱ������Ũ����ȣ��¶����ߣ�ʹ��ͬһ�ִ�������Ӧ���ʼӿ죬����������࣬������ת��������4�������ǵõ��ӵķ�Ӧ�����ʱ�����õ��ӡ�
���㣺�Ȼ�ѧ����ʽ����ؼ��㡢�缫����ʽ����д
��������������Ѷȣ��ؼ���Ҫ�����Ȼ�ѧ����ʽ�ļ���͵缫����ʽ����д��
�����Ѷȣ�����