| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ���ܽᡶԭ���ԭ��������Ԥ�⣨2019�����°棩(��)
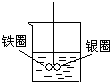 �ο��𰸣���Ȧ����Ȧ���ӽ�������ͭ��Һ�У���װ�ù�����ԭ��أ��ϻ��õĽ������������ϲ����õĽ�������������������ʧ���������������ӽ�����Һ��������Ȧ�������٣���Ȧ��ͭ���ӵõ�������ͭ���ʸ�������Ȧ�ϣ�������Ȧ�������ӣ����Թ۲쵽�������ǣ���Ȧ������б�� ��������� �����Ѷȣ��� 2��ѡ���� �й�����ͼ��ʾԭ��أ�������װ�к�������KCl������Һ������������ȷ���� �ο��𰸣�C ��������� �����Ѷȣ�һ�� 3��ѡ���� ��ͼװ���з�����Ӧ�����ӷ���ʽΪ��Zn+2H+�TZn2++H2��������˵��������ǣ������� |

�ο��𰸣�A�������װ���ǵ��أ���п�������������������Һ���ᣬ������пʧ���ӣ������������ӵõ��ӣ��������ӷ�Ӧ����ʽ�����������缫������ͬ����A����
B����װ�ÿ����ǵ��أ��������Һ��ϡ���ᣬп�����������ʱ��������пʧ���ӣ������������ӵõ��ӣ��������ӷ�Ӧ����ʽ����B��ȷ��
C����װ�ÿ�����ԭ��أ��������ҺΪϡ���ᣬп�������������������ӵõ��ӣ������ķ�Ӧ�������ӷ���ʽ����C��ȷ��
D����װ�ÿɿ�����ͭ-пԭ��أ��������Һ��ϡ���ᣬ������пʧ���ӣ����������ӵõ��ӣ��������ӷ���ʽ����D��ȷ��
��ѡA��
���������
�����Ѷȣ���
4������� ��пƬ��ͭƬ����ij�ֵ������Һ�У�пƬ��ͭƬ�õ����������γ�ԭ���װ�á�
(1)���������Һ��ϡ���ᣬ����������Ӧ����________�����п����ͭ������ͭ�������ķ�Ӧ
____________����____________���õ�ص��ܷ�Ӧ����ʽ��____________________��
(2)���������Һ������ͭ��Һ���ڵ����е�������_____������______����ͭ���ϵĵ缫��Ӧ����ʽ��
____________________���õ���ܷ�Ӧ����ʽ��____________________��
�ο��𰸣�(1)п��2H++2e-=H2������ԭ��Ӧ��Zn+2H+=Zn2++H2��
(2)п��ͭ��Cu2++2e-=Cu��Zn+Cu2+= Zn2++Cu
���������
�����Ѷȣ�һ��
5��ѡ���� ?����������ԭ��Ӧ�� 2Ag��(aq)��Cu(s)��Cu2��(aq)��2Ag(s)��Ƶ�ԭ�����ͼ��ʾ����ش��������⣺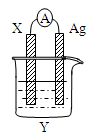
��1���缫X�IJ�����______���������ҺY��________��
��2�����缫Ϊ��ص�____���������ĵ缫��ӦʽΪ_______? ___��X�缫�Ϸ����ĵ缫��ӦΪ_____________________�����Ӧ���ͣ�
��3�����·�еĵ����Ǵ�_______�缫����________�缫��
��4������1.6gͭ�ܽ�ʱ����������_________________��
�ο��𰸣���1��Cu��AgNO3
��2��������?Ag++e-=Ag��?������Ӧ
��3��X����Cu����Ag
��4��5.4g
�����������ԭ��ص��ܷ�Ӧ����ʽ�У����ϼ����ߵ������������������ԭ����У�ͭ���������������Ļ����Դ�����������ˣ��������ǿ���ѡ��������̼�����ܷ�Ӧʽ���������Ӳ��뷴Ӧ�������ڵ������Һ�лẬ�������ӡ���˵������Һ�����ǿ���ѡ����������������������������Ӧ���缫��ӦʽΪ?Ag++e-=Ag�����ӵ����������Ǹ���ָ������������Ӧ��ͭ��������1.6�˵�ͭ�൱��0.025Ħ����ͭ����ʧȥ0.025����2����0.05Ħ���ĵ��ӡ����ݵ�ʧ����������ȿ�֪��������Ӧ�õ�0.05Ħ���ĵ�����?Ag++e-=Ag��֪��õ�0.05Ħ����������������Ϊ0.05����108����5.4�ˡ�
�����Ѷȣ�һ��
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ֪ʶ�㽲�⡶���Ľṹ��.. | |
| �����Ŀ |