1、选择题 下列实验操作中正确的是( )
A.进行蒸馏操作时,加热前应先通冷凝水,蒸馏结束后继续通冷凝水一段时间
B.进行蒸馏操作时,应使温度计水银球处于蒸馏烧瓶中溶液液面以下
C.进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
D.四氯化碳萃取碘水中的碘在分液操作时,水从分液漏斗下口放出,碘的四氯化碳溶液从分液漏斗上口放出
2、实验题 过氧化尿素是一种新型漂白、消毒剂,漂白、消毒效果优于H2O2和过氧乙酸,某工业用过氧化尿素的部分参数列于下表。
分子式
| 外观
| 热分解温度
| 熔点
| 水溶性(20℃)
|
CO(NH2)2・H2O2
| 白色晶体
| 45℃
| 75―85℃
| 500g・L―1
|
?
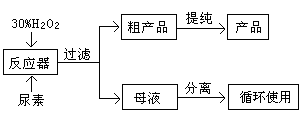
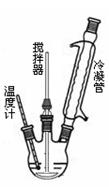
合成过氧化尿素的流程及反应器的示意图如下:
 ?
?
请回答下列问题:
(1)写出合成过氧化尿素的化学方程式:?。
(2)反应器里冷凝管中冷水从?(填“上”或“下”)口流入;反应器的加热方式是?。
①直接加热;②水浴加热;③蒸气浴加热;④冰浴
(3)搅拌器选用的材料是玻璃而不是铁质或铝质材料的原因是?,
(4)从母液中分离出H2O2和尿素,采用的是减压蒸发、冷却结晶的方法,其原因是?。
(5)活性氧含量的高低直接决定产品的质量,合格产品中活性氧的含量≥16%(相当于其中含H2O234%)。为了确定所得产品合格与否,质检员称取干燥样品2.000g,溶解于水,在250mL容量瓶中定容,准确量取其中25.00mL溶液于锥形瓶中,加入1mL 6mol/LH2SO4,然后用0.1000mol/L KMnO4标准溶液滴定样品中的H2O2(KMnO4溶液不与尿素反应),至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液6.000mL:
完成并配平下列化学方程式:
?MnO4―+?H2O2+?H+=?Mn2++?H2O+??
②KMnO4溶液应盛放在?滴定管中,若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量?(填“偏高”、“偏低”或“不变”);
③根据滴定结果确定产品质量?(填“合格”或“不合格”),活性氧的质量分数为?。
3、选择题 下列实验设计方案中,可行的是( )
A.用加入适量铜粉的方法除去Mg(NO3)2溶液中混有的AgNO3
B.分液操作时,首先要打开分液漏斗的上口活塞,或使活塞上的小孔与上口部的小孔对准,然后进行分液
C.蒸馏操作时,冷凝水的方向应当由下口进上口出
D.蒸馏时,应使温度计水银球应插入蒸馏烧瓶液体中
4、选择题 下列物质的分离或鉴别正确的是
A.除去混在氯化钠固体中的氯化铵或单质碘均可用加热升华的方法
B.若FeCl2溶液中含有I-杂质,可用过量的Cl2氧化后进行萃取分液
C.从海水中提取溴,一般是向浓缩后的海水中通入Cl2,再鼓入热空气或水蒸汽将溴分离出来
D.鉴别固体Na2CO3和NaHCO3,可以分别配成溶液,再加入澄清石灰水
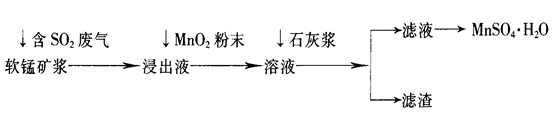
5、简答题 工业上常利用低品位软锰矿浆(主要成分是MnO2)来吸收含SO2的废气,最终制得硫酸锰晶体(MnSO4・H2O),其主要流程如下:
已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子。有关金属离子形成氢氧化物沉淀时溶液的pH见下表:
离子
| 开始沉淀时的pH
| 完全沉淀时的pH
|
Fe2+
| 7.6
| 9.7
|
Fe3+
| 2.7
| 3.7
|
Al3+
| 3.8
| 4.7
|
Mn2+
| 8.3
| 9.8
|
?
(1)软锰矿浆中通入含SO2废气后,发生主要反应的化学方程式为____________________。
(2)浸出液中加入MnO2粉末的目的是____________;反应的离子方程式是___________________。
(3)溶液中加入石灰浆来调节pH,其作用是_________________;pH应调节的范围是__________。
(4)滤渣的主要成分是________________________________________________(用化学式表示)。