1、选择题 氯化银在水中存在沉淀溶解平衡:AgCl(s)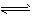 Ag+ (aq) +Cl-( aq)。现将足量的AgCl分别放入:
Ag+ (aq) +Cl-( aq)。现将足量的AgCl分别放入:
①100mL 蒸馏水中;②100mL 0.1mol/L的HCl溶液中;③100mL 0.1mol/L的AlCl3溶液中;④100mL 0.1mol/L的MgCl2溶液中。充分搅拌后,相同温度下,银离子浓度由大到小的顺序
[? ]
A.①②③④?
B.①②④③
C.④③①②
D.②①④③
参考答案:B
本题解析:
本题难度:一般
2、选择题 某溶液中大量存在四种离子:NO-3、SO2-4、H+、M,其物质的量之比为:N(NO-3):n(SO2-4):n(H+):n(M)=3:1:3:1,则M可能为?(?)
①Fe2+?②Mg2+?③Cl― ?④Ba2+
?④Ba2+
A.①②④
B.③
C.②
D.①②
参考答案:C
本题解析:略
本题难度:一般
3、简答题 25℃时,有浓度均为0.10mol/L的乙酸、乙酸钠两种溶液.请回答:两种溶液中,c(H+)<c(OH-)的是______(填“乙酸”或“乙酸钠”),其原因是______(用离子方程式表示).两种溶液等体积混合后溶液显酸性,混合后溶液中各种离子的浓度由大到小依次为______.
参考答案:醋酸电离出氢离子导致溶液呈酸性,则c(H+)>c(OH-);醋酸钠为强碱弱酸盐,醋酸根离子水解导致溶液呈碱性c(H+)<c(OH-),水解方程式为CH3COO-+H2O?CH3COOH+OH-,两种溶液等浓度等体积混合后,混合溶液呈酸性,说明醋酸电离程度大于醋酸根离子水解程度,钠离子不水解,则c(CH3COO-)>c(Na+)>c(H+)>c(OH-),
故答案为:乙酸钠;CH3COO-+H2O?CH3COOH+OH-;c(CH3COO-)>c(Na+)>c(H+)>c(OH-).
本题解析:
本题难度:一般
4、选择题 一定浓度的下列溶液,加入少量的固体NaOH后,溶液的导电能力变化不大的是
A.蒸馏水
B.醋酸
C.盐酸
D.稀氨水
参考答案:C
本题解析:A错,蒸馏水导电能力能弱,但加入氢氧化钠后溶液的导电能力变大;B错,醋酸为弱酸,加入氢氧化钠后生成醋酸钠强电解质溶液的导电能力增强;C正确,盐酸中加入氢氧化钠生成氯化钠和水,溶液中自由移动离子数目基本不变,溶液导电能力变化不大;D错,氨水为弱电解质,加入氢氧化钠后,氢氧化钠为强电解质溶液的导电能力增大;
本题难度:一般
5、填空题 回答下列问题:
Ⅰ、有下列物质:①Fe ②CO2 ③Na2O ④Cu(OH)2 ⑤MgCl2 ⑥NH4Cl ⑦H2SO4
⑧C2H5OH(酒精)(用序号作答).
上述十种物质中,其中属于电解质的有______,属于非电解质的有______.
Ⅱ、今有K2SO4和Al2(SO4)3的混合溶液,已知其中K+浓度是0.2mol?L-1,SO42-的浓度是0.7mol?L-1.
(1)写出Al2(SO4)3电离的电离方程式:______.
(2)Al3+浓度应等于______mol/L
Ⅲ、根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
(1)该反应中氧化剂是______,被氧化的是______元素.
(2)该反应中参加氧化还原的氧化剂与还原剂的物质的量之比为______.
(3)用双线桥法标出电子转移的方向与数目______.
参考答案:I.①Fe是单质,既不是电解质也不是非电解质;②CO2 本身不能电离,属于非电解质;③Na2O是化合物且熔融状态下导电,属于电解质;④Cu(OH)2是化合物且熔融状态下导电,属于电解质;⑤MgCl2是化合物,在水溶液或者熔融状态都导电,属于电解质;⑥NH4Cl是化合物溶液中导电,属于电解质; ⑦H2SO4 是化合物溶液中导电,属于电解质;⑧C2H5OH(酒精)是化合物,在水溶液和融化状态下都不导电,是非电解质,故答案为:③④⑤⑥⑦;②⑧;
II.(1)硫酸铝是强电解质完全电离,电离方程式:Al2(SO4)3=2Al3++3SO42-;
故答案为:Al2(SO4)3=2Al3++3SO42-;
(2)溶液呈中性,根据电荷守恒列关系式:C(Al3+)×3+C(K+)=2×C(SO42-),将各种离子浓度带入得:C(Al3+)×3+0.2mol?L-1=2×0.7mol?L-1.
C(Al3+)=0.4mol/L;
故答案为:0.4mol/L;
III (1)该反应氨气中的氯气中的氯元素化合价降低,所以氯气是氧化剂;氮元素化合价升高,被氧化;
故答案为:Cl2或氯气;N或氮;
(2)在反应8NH3+3Cl2=6NH4Cl+N2,3mol氯气中的氯元素化合价都降低,所以3mol氯气都做氧化剂;8mol氨气中只有2mol氨气中的氮元素化合价升高,所以做还原剂的氨气只有2mol,所以氧化剂和还原剂物质的量之比是3:2;
故答案为:3:2;
(3)根据得失电子守恒的原理用双线桥法标出电子转移的方向与数目.
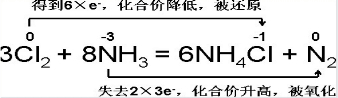 ;
;
故答案为: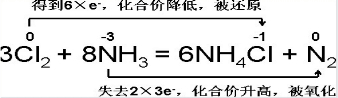 .
.
本题解析:
本题难度:一般