1、填空题 已知①25℃时,难溶电解质的溶度积常数:Ksp(CaC2O4)=2×10-9,②25℃时,100?mL?0.4?mol・L-1?H2C2O4水溶液中,用KOH固体来调节溶液pH(忽略体积变化),得到H2C2O4、HC2O4-、C2O42-三种微粒含量与溶液pH的变化关系如图所示。?
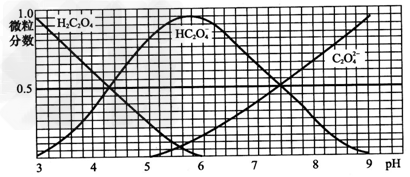
请回答下列问题:
(1)?pH=5.2时,H2C2O4、HC2O4-、C2O42-浓度从大到小依次是__________。
(2)向水中加入KHC2O4固体会使水的电离平衡向_______ 移动,解释其原因是__________。
(3)将500?mL0.2mol・L-1?H2C2O4与500?mL0.2mol・L-1 ?K2C2O4混合,关于所得溶液的下列关系式中错误的是?(? ?)
A.c(K+)>c(H+)>c(C2O42-)>c(H2C2O4)
B.c(K+)+c(H+)=2c(C2O42-)+c(HC2O4-)+c(OH-)
C.c(K+)=2c(HC2O4-)+2c(C2O42-)+2c(H2C2O4)
D.?c(C2O42-)>c(H2C2O4)>c(HC2O4-)
(4)?25℃时向1L1×10-4?moI/L?H2C2O4溶液中加入1× 10-4?mol?CaCl2固体,调节溶液pH=9,请通过计算判断是否产生白色沉淀?_________(填“是”“否”或“无法确定”)。 ?
(5)为了测定血液中的钙离子含量,通常向样品中加入K2C2O4使之转化为CaC2O4沉淀,再向过滤出的沉淀中加入 ?过量的硫酸将沉淀转化为H2C2O4,最后用高锰酸钾溶液滴定。请写出滴定时发生反应的离子方程式:_____________。
2、选择题 下列气体通入水中,不能形成电解质溶液的是
A.NH3
B.O2
C.HBr
D.HCl
3、选择题 相同温度、相同物质的量浓度的下列四种溶液
① CH3COONa ② NaHSO4 ③NaCl ④ C6H5ONa,
按pH由大到小的顺序排列正确的是
[? ]
A.④>①>③>②
B.①>③>④>②
C.①>②>③>④
D.④>③>①>②
4、选择题 下列操作不能达到预期目的是( )
A.

检查装置气密性
B.
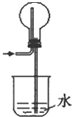
HCl的吸收
C.
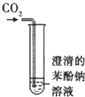
碳酸、苯酚酸性强弱比较
D.
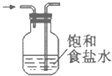
除去氯气中的氯化氢
5、选择题 下列物质中,属于电解质的是
A.CO2
B.石墨
C.K2SO4
D.NaOH溶液